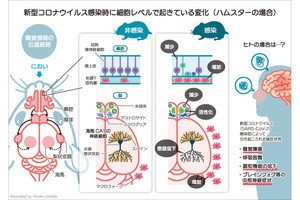
具体的には、原因のわからない自閉症のモデルとして、自然発症のBTBRマウスを対象に、1細胞RNAシーケンス(sc-RNA seq)を用いて、免疫異常の起源をYSとAGMの胚の段階まで遡り、マクロファージ(ミクログリア)と末梢免疫細胞が分化している場所を特定したほか、YSとAGMにおける二次造血の1細胞レベルにおける解析から、発生初期段階における希少な前駆細胞内の分子レベルでの病理学的メカニズムを特定することに成功し、これらの病態の根底にヒストン脱アセチル化酵素「HDAC1」を介した転写制御の共通メカニズムを見出したとする。
-
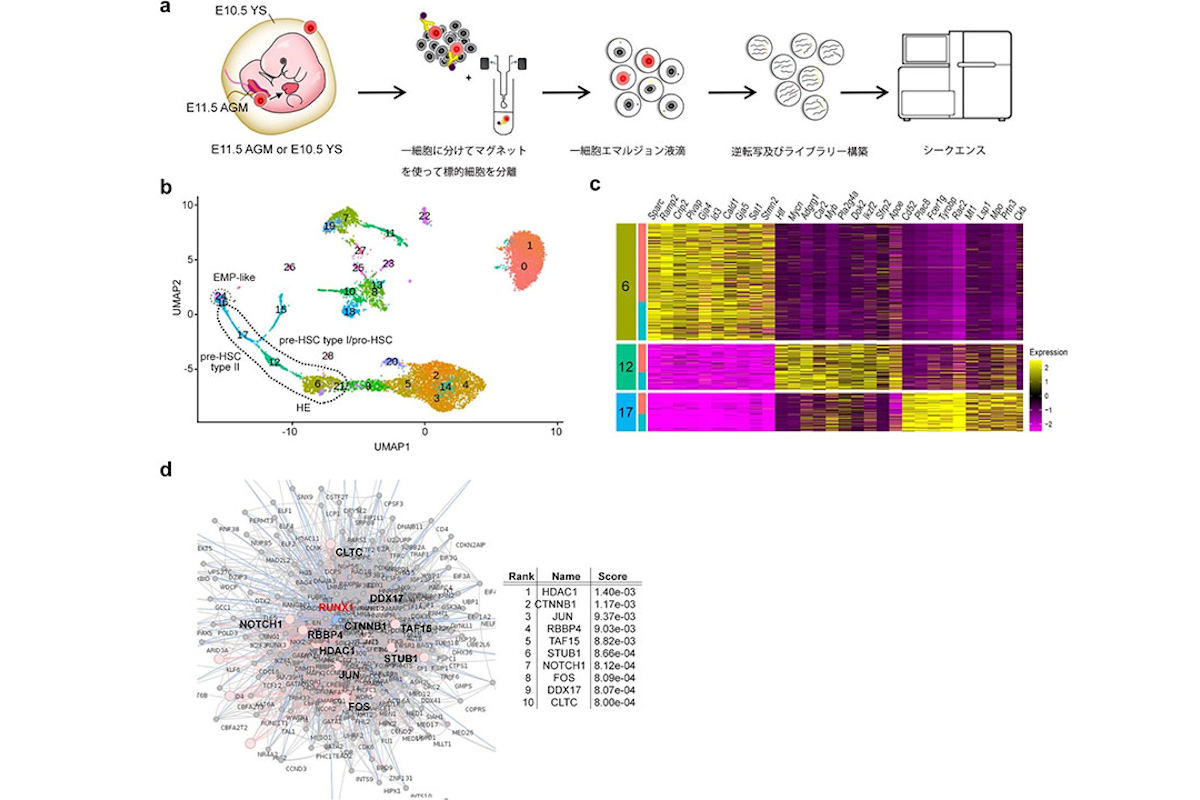
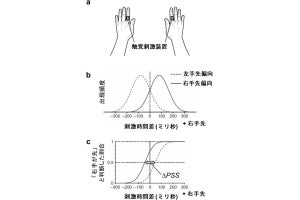
AGMのsc-RNA seq解析。(a)実験概略図。(b)AGM前駆細胞の1細胞解析による細胞群が示されている。(c)(b)の3つの細胞群(6、12、17)で発現上昇したトップ10の遺伝子群のヒートマップ。(d)血管内皮細胞が造血幹細胞を産生する過程(EHT)に必須の転写因子RUNX1のタンパク相互ネットワークに基づく遺伝子エンリッチメント解析 (出所:神戸大Webサイト)
また、特定の発生段階においてエピジェネティックな機構を操作することで、脳や末梢組織における免疫異常を回復させることができることも示されたともしている。共通のメカニズムとして同定されたHDAC1の阻害剤(酪酸ナトリウム、ロミデプシン)をBTBRマウスの胎児期に投与すると、炎症性サイトカインの上昇やミクログリアの活性化が抑制されたという。
-

HDAC1の促進による転写抑制は、血管内皮細胞からEHTに影響を与える。卵黄嚢(Yolk sac)の赤血球・骨髄球系前駆細胞(EMP)はミクログリアを活性化して脳内炎症に影響する。AGMの前造血幹細胞(pre-HSC)は骨髄(BM)にて分化、変化を受けた免疫系は腸内細菌叢に影響を与える (出所:神戸大Webサイト)
さらに、免疫異常が自閉症モデルマウスの特定のプロファイルの腸内細菌の異常を決定するという因果関係も解明され、免疫細胞(Treg)と腸内細菌のバイオマーカーが、免疫異常を有する自閉症のサブタイプを分類する手段となる可能性があることも示されたとする。
なお、研究チームでは今回の成果について、自閉症における全身性免疫異常という長年の謎が明らかにされただけでなく、環境リスク要因の異なる自閉症モデルに共通する病因としてエピジェネティックな障害が果たす役割を示唆するものだとしているほか、将来的に自閉症の精密医療、個別化医療を発展させるためには、発症メカニズムに応じた自閉症のサブタイプ分類が必要であり、自閉症治療の新たな道を切り開く重要な第一歩となるとしている。