京都大学(京大)と日本医療研究開発機構は8月31日、腱の断裂などの大ケガに対する新たな治療法の1つとして、iPS細胞を腱細胞まで分化させた上でそれを患部に移植するという細胞移植の新手法を開発したことを発表した。
-
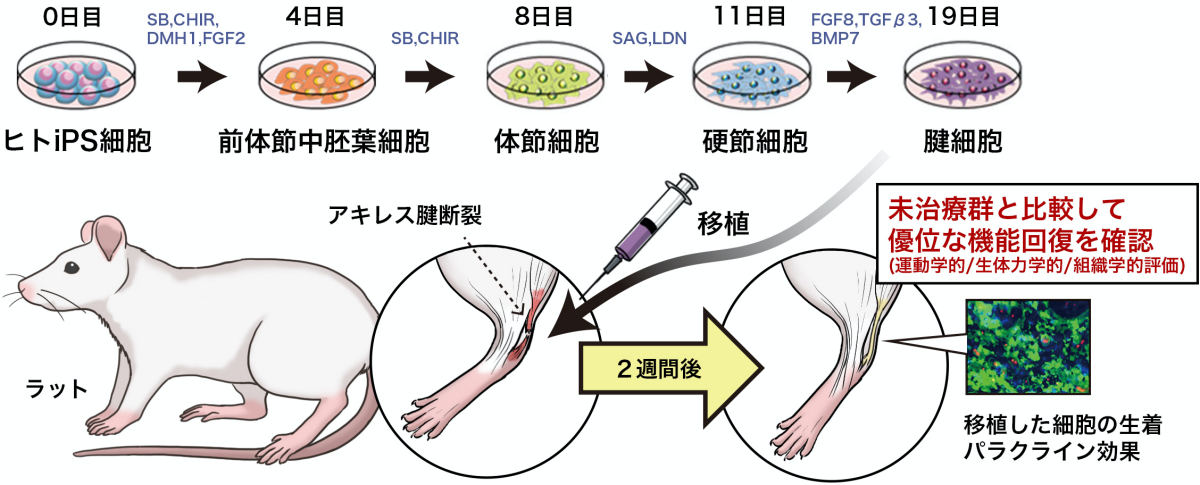
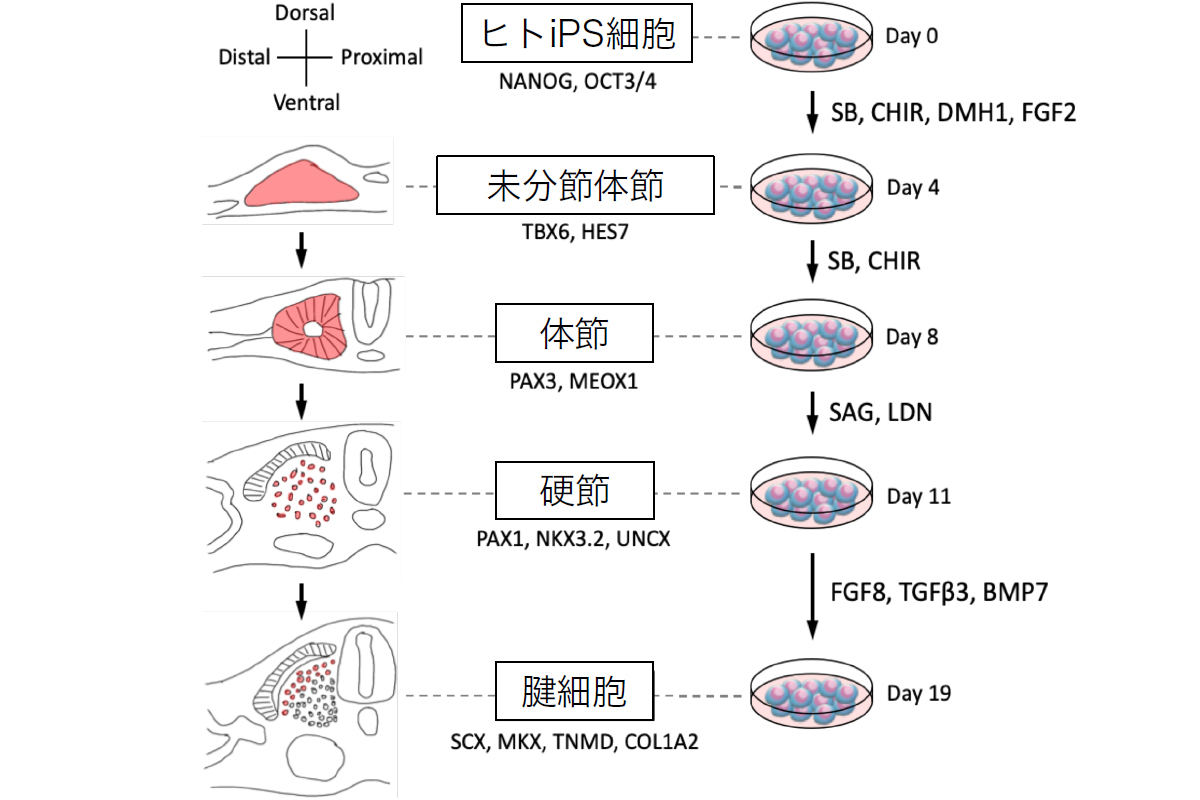
今回の研究の概要図。(上)ヒトiPS細胞から19日間かけて腱細胞へと分化誘導が行われた模式図。(下)アキレス腱断裂モデルラットが用いられ、ヒトiPS由来腱細胞の移植による治療効果の確認実験の模式図 (出所:京大プレスリリースPDF)
同成果は、京大 iPS細胞研究所(CiRA)臨床応用研究部門の中島大輝研究員(現・米ハーバード大学医学部兼米ブリガムアンドウィメンズ病院兼日本学術振興会海外特別研究員)、同・池谷真准教授、同・慶澤景子テクニカルスタッフ、同・趙成珠研究員、CiRA 未来生命科学開拓部門の岩崎未央特定助教、京大医学部 人間健康科学科の黒木裕士教授、同・中畑晶博理学療法士、京大 iPS細胞研究財団/CiRAの加藤智朗特定研究員、東京慈恵会医科大学 附属第三病院 リハビリテーション科の山田尚基講師らの研究チームによるもの。詳細は、英オンライン科学誌「Nature Communications」に掲載された。
ヒトが身体を動かせるのは、骨格と筋肉があるのはいうまでもないが、その2つをつなぐ「腱」があればこそである。腱は、筋肉が伸縮する力を骨に伝える役割を担い、それによってヒトは身体を動かすことができるのである。つまり、腱を負傷することはその部位をうまく動かせなくなり、QOL(人生の質)に大きな影響を及ぼすこととなる。
腱は切れても自然治癒はするものの、血流が乏しいために完治するまでに時間がかかってしまうという特性がある。そのため、アキレス腱断裂などの大きなケガの場合は、その患者自身のほかの部位の腱を用いた再建手術が行われることもあるが、再建手術は健常部位も切り開く必要があるために患者への負担が大きく、それだけ合併症のリスクも高くなる。
しかも、再建したからといって100%回復できるというわけではなく、再建しても再び負傷してしまうこともあるほか、再建のために採取を行うことにより、その取り出した部位の筋力低下も生じるというデメリットもある。それゆえ、再建したアキレス腱を含めて長いリハビリ期間が必要になってしまうとが知られている。
こうした実情を改善しようと、医師や研究者らは、これまでコラーゲンやカーボン、ポリエステルなどを用いた人工腱を開発してきた。しかし、これらの人工腱は力学的強度や生体への親和性といった課題を解決できておらず、実用化のレベルには至っていない。
そこでさらに考案されたのが、腱細胞や間葉系幹細胞、皮膚線維芽細胞などを患部に移植する再生医療の一種である「細胞移植治療」だ。しかし、この細胞移植治療も複数の課題を抱えているという。まず損傷した腱の再生には、腱細胞を補充することが最もシンプルな手法だが、腱細胞は増殖能が低いため、移植に必要なだけの量の腱細胞を用意することが困難だという点だ。さらに、生体外で腱細胞を増やした場合、細胞の機能低下を引き起こす可能性があるという点も課題となっている。
それでは、腱細胞よりも増殖能の高い、間葉系幹細胞や皮膚線維芽細胞などを移植した場合はどうかというと、こちらの場合はさらに難しい課題がある。それらの細胞がすべて狙い通りに腱細胞に分化するとは限らないからだ(まだ生体内で完全制御できる技術が確立されていない)。目的以外の細胞や組織になってしまうことを「異所性組織形成」といい、アキレス腱の代わりに別の細胞ができてしまったら、アキレス腱の機能も回復できない上に、新たな問題まで生じてしまうことになる。
細胞移植治療は可能性を秘めた治療法ではあるが、解決すべき課題があり、それらを克服した新たな手法が待ち望まれているのである。
このような背景を受け、研究チームが取り組んでいるのが、ヒトのiPS細胞から作成した腱細胞を使った治療法だ。これまでのiPS細胞や間葉系幹細胞から腱細胞を作成することは行われているが、ヒトのiPS細胞から腱細胞を誘導し、細胞移植治療へつながる研究が行われたのは今回が初めてだという。
ヒトの腱細胞は、発生をたどると「中胚葉」が出発点となる。研究チームは2018年8月に、体外でヒトiPS細胞から「前体節中胚葉細胞」、「体節細胞」を誘導し、そこから「硬節細胞」や腱・靭帯細胞を分化誘導させるモデルの開発に成功したことを報告している。
ただし、この2018年に発表された分化誘導法では、細胞を培養する過程で動物由来の成分が使用されていた。しかし今回の研究では、将来的にヒトの細胞移植治療への応用を目指すため、動物由来の成分を一切使用しない「ゼノフリー条件」下の分化誘導法への改良が施されたという。
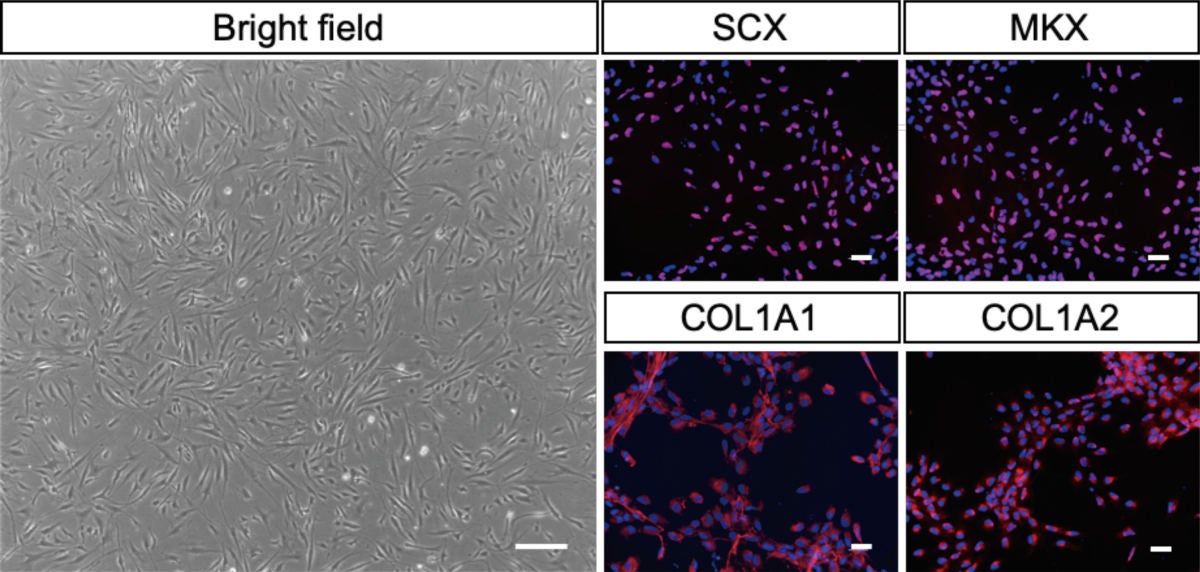
改良型分化誘導法により、19日間かけてヒトiPS細胞から腱細胞が作成され、免疫染色が実施されたところ、腱細胞に特有の転写因子(SCX、MKX、COL1A1、COL1A2)が発現していることが確認できたという。
さらに、シングルセルRNAシーケンシング法を用いた、iPS腱細胞とプライマリー腱細胞(腱細胞から初代培養した腱細胞)との遺伝子発現の比較を行ったところ、プライマリー腱細胞に近づいてはいるものの、100%の一致まではまだ遠く、分化誘導技術のさらなる改良が必要なことも確認されたとする。
-
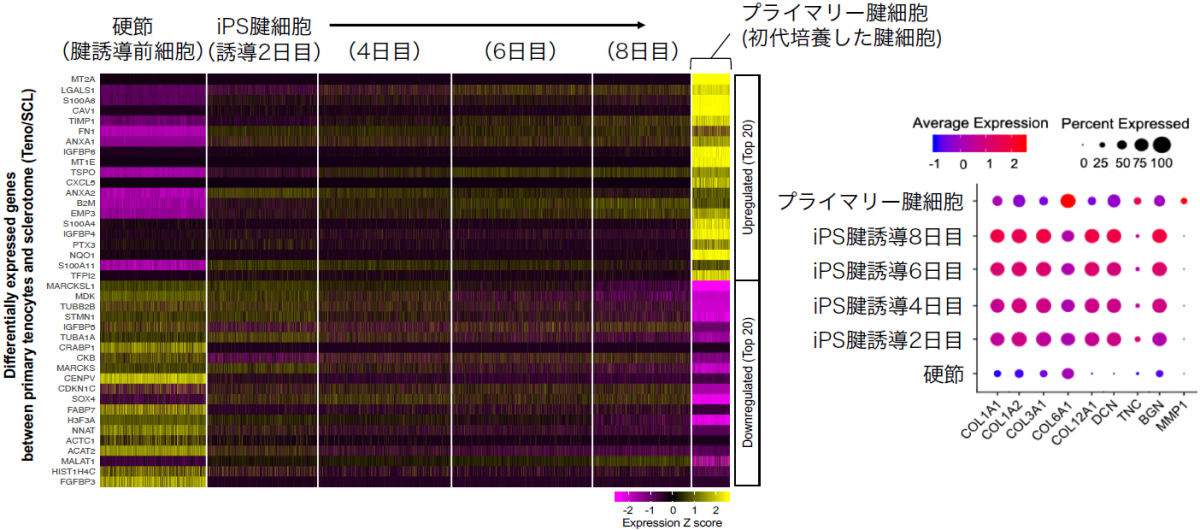
シングルセルRNAシーケンシングによる、iPS由来腱細胞とプライマリー腱細胞(実際の腱細胞から培養された細胞)との遺伝子発現の比較。(左)硬節と、腱細胞に分化誘導されて2・4・6・8日目(iPS細胞からの分化誘導ではトータルで19日目)、そしてプライマリー腱細胞の比較。8日目次点のものは、プライマリー腱細胞に近づいてはいるものの、まだだいぶ異なっている。(右)左の遺伝子発現の比較図をよりわかりやすくまとめたもの。ポイントとなる遺伝子に絞って発現度合いが評価されており、硬節と比べるとiPS由来腱細胞はプライマリー腱細胞に近づいてはいるが、まだ完全に同一までは遠いこともわかる。さらに分化誘導技術を進展させる必要があるようだ (出所:京大会見資料PDF)
まだ改良すべき点はあるものの、iPS細胞を使うことで、移植するために必要な大量の腱細胞を確保するという問題をクリアすることが可能となったことから、その作成されたiPS由来腱細胞の移植が、治療法として有効か否かを調べるため、アキレス腱断裂モデルのラットを用いた動物実験が実施された。モデルラットは、左後ろ足のアキレス腱を、踵骨との結合箇所から5mmほど上方の部位が切断され(腱の一部を取り除くなどはされていない)、そこに注射器を用いて300万個の腱細胞が移植され、4週間の経過観察を行うというものだという。
今回の実験では、ヒトのiPS細胞からゼノフリー条件で作成された腱細胞がそのまま使用されている。つまり、ラットの身体にとっては厳密には問題があるということだが、研究チームはそれを理解した上で、そのままモデルラットに対してヒトiPS由来腱細胞を用いて実験を進めたとしている。
運動学的な評価としての歩行の様子は、一般的にアキレス腱に問題のない健常なラットは、かかとを地面につけずに歩行するが、アキレス腱が断裂したラットは、運動機能の低下のため、負傷後3週間程度まではかかとを地面につけたまま歩行する。ラットのアキレス腱は断裂してもゆっくりとつながり、およそ4週間で断裂前に近い状態にまでは自然治癒するという(ただし、4週間では機能的に100%の回復にはほど遠い状態であることには変わりはない)。
それに対して細胞移植が行われたラットの場合は、1週間はかかとを地面につけて歩行していたが、2週間後にはかかとをつけずに歩行するようになったことが、足跡の解析から確認された。移植された腱細胞が仕事を果たしたことが明らかとなったのである。
-
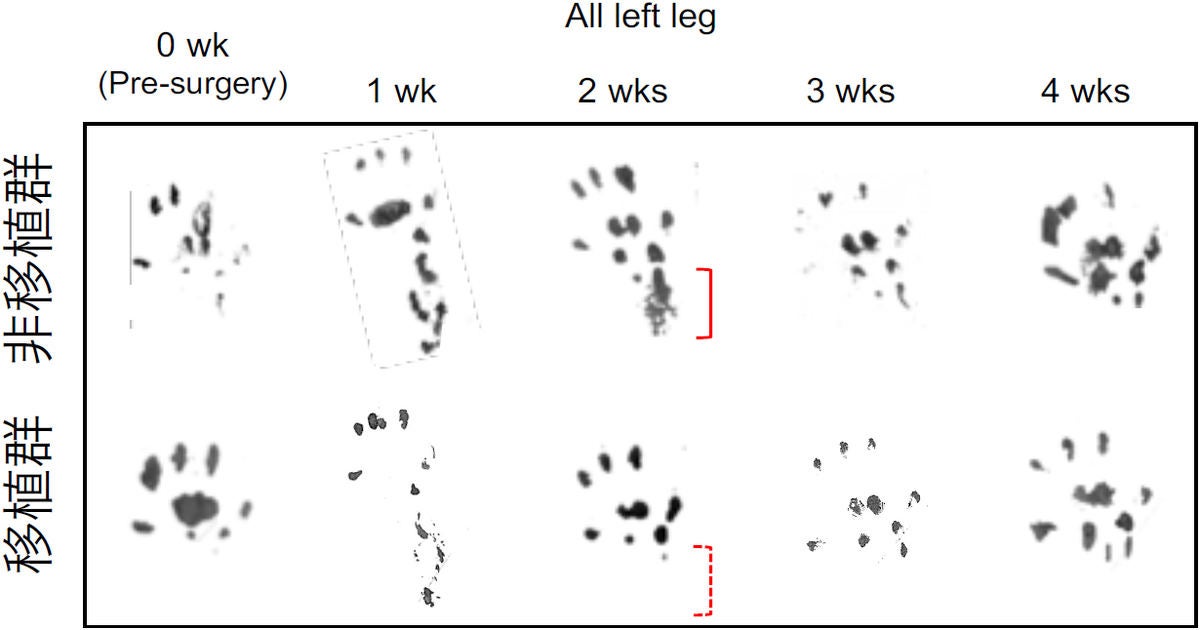
トレッドミルを歩行させて取得された足跡から解析が行われた。上段の非移植群(未治療ラット)は、2週目もかかとをつけているのがわかる。それに対して下段の移植群(細胞移植ラット)は、2週目の時点でかかとをついていない (出所:京大会見資料PDF)
さらに、かかとの骨の位置にマーカーを取り付け、歩行時におけるかかとの地面からの高さも測定したところ、移植後2週間の細胞移植ラットのかかとの高さは、未治療のラットよりも有意に高く、健康ラットのかかとの高さと同程度になっていることがわかったとするほか、ヒザ関節と脚の小指につけたマーカーから、足首の角度においても移植後2週間および4週間の細胞移植ラットは、健常ラットの足首の角度と同程度まで回復したことも判明したという。
-
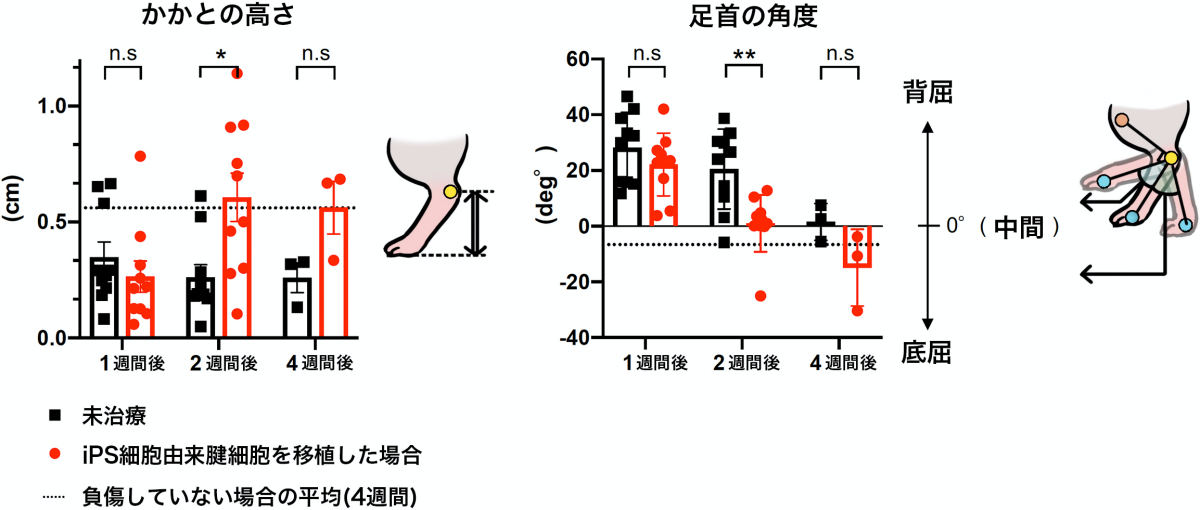
移植後のラットの運動学的評価。細胞移植ラットと未治療ラットを対象にした、切断から1週間後、2週間後、4週間後のトレッドミルでの歩行による比較。どちらのグラフにもある点線は、健常ラットの平均。(左)ラットのかかとの高さの比較。1週間後では未治療の方が高いぐらいだが、2週間後には細胞移植は健常の平均を少し上回るぐらいまで回復しており、未治療は4週間後もかかとが低いままなのがわかる。(右)足首の角度の比較。足首の角度も2週間後の時点で、細胞移植と未治療では差が出ており、細胞移植は健常の平均に迫るレベルとなっている。ただし、4週間後には未治療も細胞移植と同程度まで回復している。移植後1週間と2週間:n=10、移植後4週間:n=3。*:P<0.05、**:P<0.01、n.s:not significant(有意差なし) (出所:京大プレスリリースPDF)
さらに再生されたアキレス腱の生体力学的評価として、移植後2週間と4週間のラットの再生したアキレス腱を採取し、それが破断するまでに要する荷重(最大荷重)の測定を実施したところ、移植後2週間の再生アキレス腱は同期間の未治療アキレス腱と比べ、最大荷重が高いことが判明したが、健常アキレス腱に比べると差があることも明らかとなったとする。
-
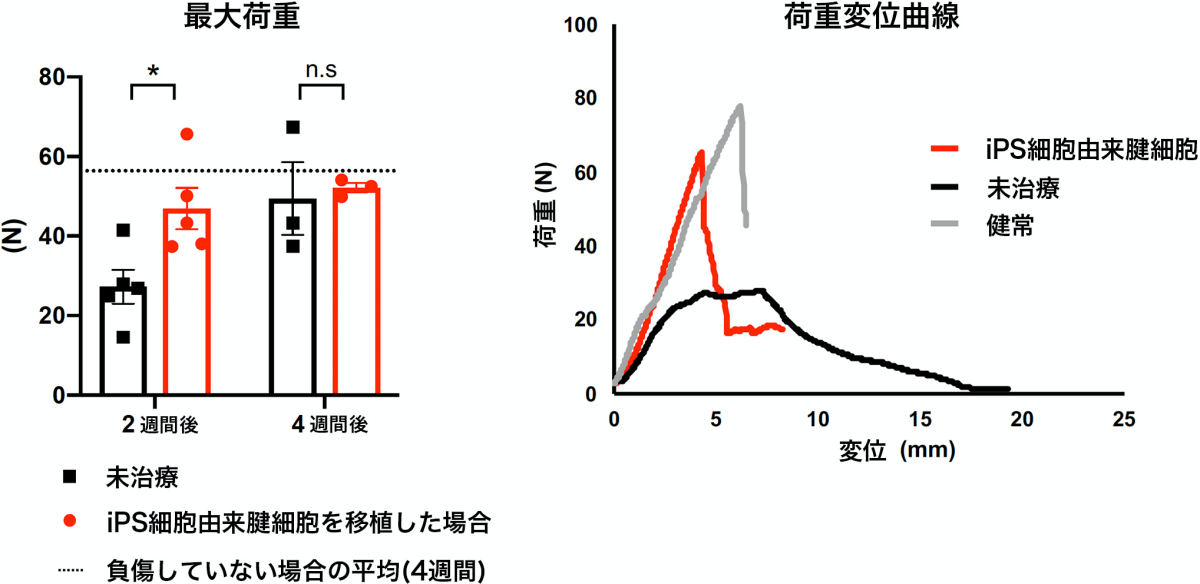
再生アキレス腱の破断に要した最大荷重を測定する生体力学的評価。(左)切断から2週間後と4週間後の細胞移植ラットと未治療ラットの比較。点線は健常ラットの平均。2週間後の時点で細胞移植は、健常の平均の80%ぐらいまで回復している。4週間後は90%ほどだが、100%には至っていない。未治療も4週間後には細胞移植のレベルには追いついており、時間をかければどちらも差はなくなってくるのがわかる。(右)切断から2週間後の健常、細胞移植、未治療のアキレス腱の荷重変異曲線の比較。未治療は健常とはほど遠い曲線を描いているが、細胞移植は健常に近い (出所:京大プレスリリースPDF)
加えて再生した腱の物性を比べるため、荷重変位曲線を作成した結果、未治療アキレス腱はなだらかな曲線を示していたのに対し、再生アキレス腱は健常アキレス腱と似たような挙動を示していることが確認されたとする。ただし似てはいるものの、ここでも再生アキレス腱は、健常アキレス腱には及ばないことが判明したという。
-
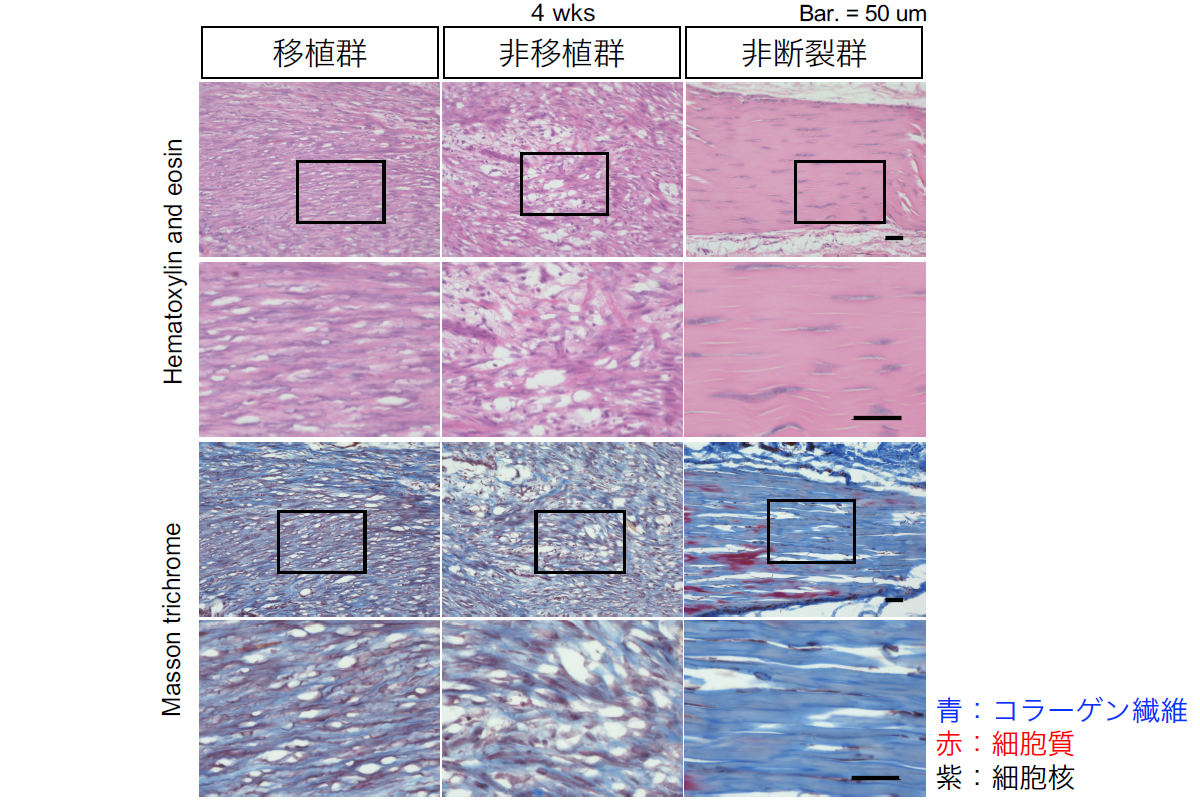
アキレス腱の顕微鏡画像による比較。現時点の細胞移植では、健常なアキレス腱にはまだ及ばないことが見て取れる。(左)移植群(細胞移植ラット)のアキレス腱。健常なアキレス腱とはほど遠く、未治療(非移植群)に近い斑な様子が見て取れる。(中央)非移植群(未治療ラット)のもの。移植群よりもさらに斑な感じとなっている。(右)非断裂群(健常ラット)のもの。滑らかなのがわかる (出所:京大会見資料PDF)
このように再生アキレス腱は最大荷重が高く、荷重変位曲線が健常アキレス腱に近く、健常アキレス腱には及ばないものの、未治療アキレス腱と比べて耐久性と物性が回復していることが確かめられたという。今回は4週間までの実験だったため、さらに時間をかければより健常なアキレス腱に近くなるまで回復する可能性もあるとしている。
このほか、移植された腱細胞の生着や組織の状態を調べることを目的に組織学的評価として、移植するヒトiPS由来腱細胞の移植後24時間、2週間、4週間の蛍光分布を調べたところ、移植された腱細胞は血流に乗って全身に散らばるようなこともなく、移植部位の左後ろ足アキレス腱近辺に留まっていることが判明したという。
-
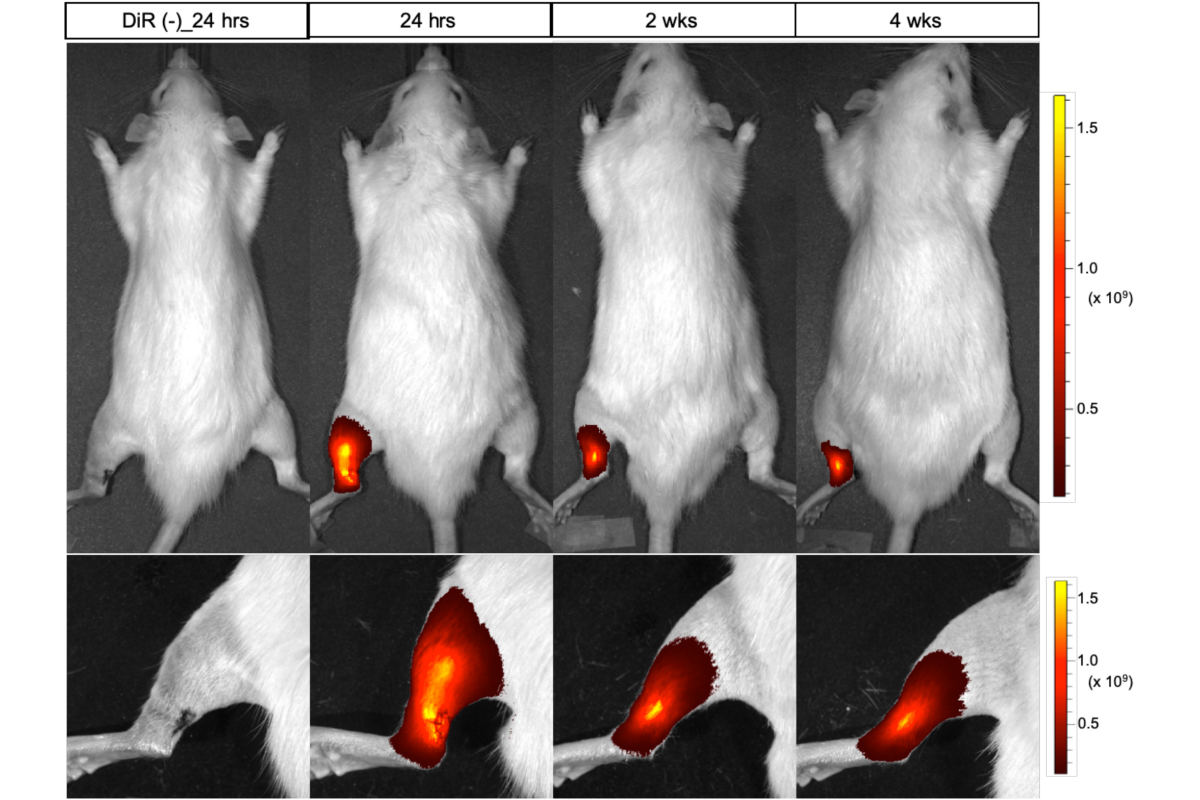
移植されたiPS由来腱細胞の分布。iPS由来腱細胞に蛍光色素が付加され、移植後24時間、2週間後、4週間後の蛍光分布が比較された(一番左は移植前)。移植された腱細胞は移植部位に留まって生着していることが見て取れる (出所:京大プレスリリースPDF)
さらに、I型コラーゲン、III型コラーゲン、ヒト特有の「ビメンチン」の3種類のタンパク質を対象とする免疫染色が移植後2週間の再生アキレス腱に施されたところ、ビメンチン陽性の移植細胞が、コラーゲンを発現していることが確認されたという。これは移植した腱細胞が生着し、ラットのアキレス腱の一部としてある程度機能していることを示唆するという。一方、未治療アキレス腱では、コラーゲンの生成が見られない未再生部分が多く確かめられたとした。
-
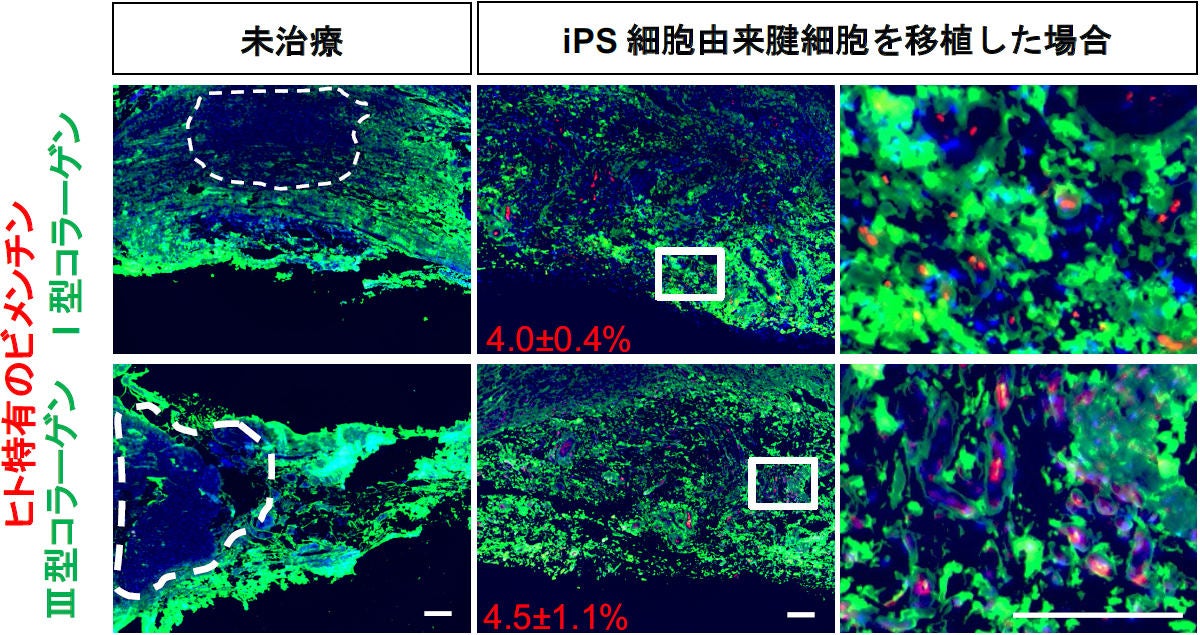
細胞移植されたアキレス腱の組織学的評価(切断後2週間後)。ヒト特有のビメンチンは赤に、I型コラーゲンとIII型コラーゲンは緑に免疫染色されている。(左)未治療ラットのもの。点線内はコラーゲン未再生部分。(中央・右)細胞移植ラットのもの。ビメンチンが確認できる (出所:京大プレスリリースPDF)
これらの結果は、外部で作成されたヒトiPS由来腱細胞が移植されたあとも必要な機能を働かせていること、未治療と比べ明白な治療効果があることが示されたとする。
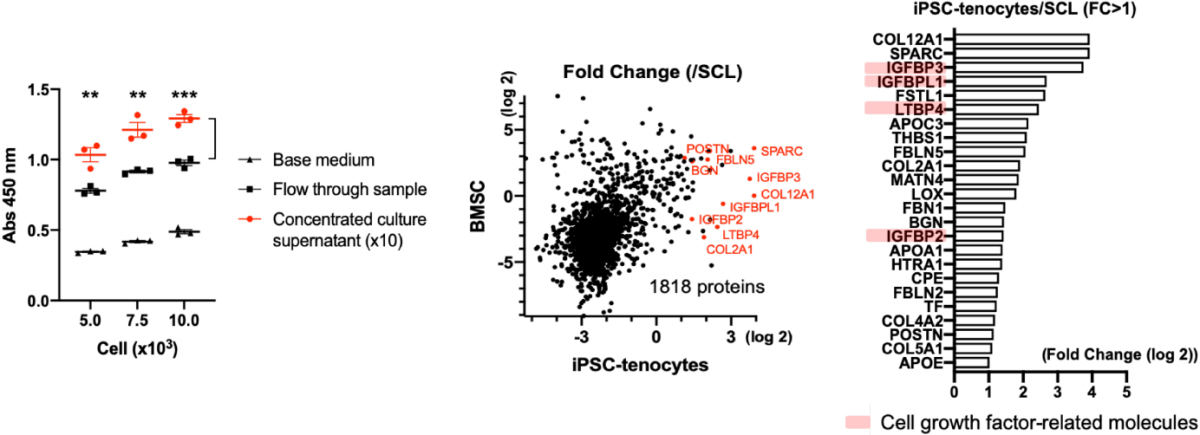
また別の実験として、アキレス腱の機能回復に関与したヒトiPS細胞から分泌されるタンパク質の存在の調査として、ヒトiPS由来腱細胞の培養上清濃縮液でヒトプライマリー腱細胞が培養されたところ、濃縮前の液より増殖がよくなることが明らかとなったという。このことから、ヒトiPS由来腱細胞を培養中の培地上清には腱細胞の増殖に寄与するような何らかの成長因子が含まれていることが示されたとしている。
さらにプロテオーム解析により、その成長因子の候補探索が行われたところ、「IGF1」と「TGFβ3」シグナルの関連タンパク質が、ヒトiPS由来腱細胞から多く分泌されていることが特定された。
そこで、IGF1タンパク質またはTGFβ3タンパク質がアキレス腱断裂モデルラットに投与され、2週間後に評価が実施された結果、生体力学的には効果がそれほど見られなかったものの、運動学的には未治療ラットに比べ、IGF1/TGFβ3投与ラットはそれぞれにおいて優位に機能が回復していることが明らかとなった。つまり、IGF1とTGFβ3が移植先のラットの腱細胞の成長を促す「パラクライン効果」があり、運動学的な機能回復に寄与していることが示唆されたとしている。
一般的に、細胞移植による治療効果のメカニズムは2種類が考えられるという。1つは、移植した細胞が傷ついた細胞と入れ替わり組織の一部となること。もう1つは、移植した細胞によるパラクライン効果によって患部の細胞の自己回復能力が高まることだという。今回のヒトiPS由来腱細胞の細胞移植治療では、両方のメカニズムが関わっていることを示唆する結果が得られたとしている。
今回のさまざまな研究成果について研究チームでは、長期の治療によるリスクが高いアスリートや高齢者にとって、メリットの多い治療法となる可能性があるとしているほか、無限に増殖可能なヒトiPS細胞を用いることで、移植する腱細胞を大量に作製することができるため、これまで腱細胞/皮膚線維芽細胞/間葉系幹細胞を用いた細胞移植治療の課題であった、移植する腱細胞不足の課題を解決できたり、ヒトiPS由来腱細胞は一旦iPS細胞にすることで細胞の若返りが起こるため、老化によって弱った腱にはより有効だと考えられるとしている。
なお研究チームは今後、さらに長期にわたる経過観察や、アキレス腱以外の腱障害への治療適用、そして老年ラットを用いた移植治療効果の検証を進めていきたいとしている。