大阪公立大学(大阪公大)は11月17日、独自に開発した粘膜ワクチン技術と、幅広い血清型をカバーできる「肺炎球菌表層タンパク質」を組み合わせ、新規の肺炎球菌ワクチンを開発し、マウスモデルとカニクイザルを用いた実証実験により、ワクチンを接種した対象動物群では肺炎球菌感染による肺炎を明らかに抑制できていることを確認したと発表した。
-
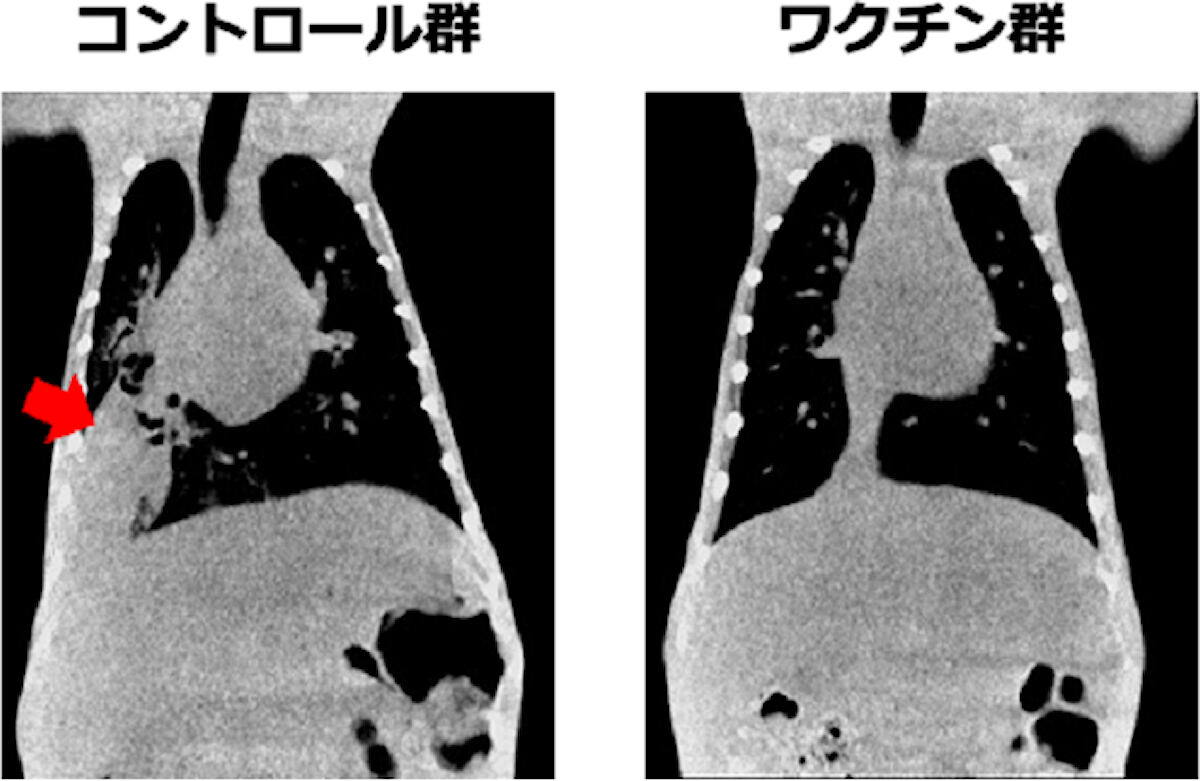
カニクイザルの肺炎球菌感染による肺炎の発症の様子。(左)コントロール(ワクチン非投与)群では、矢印部分に肺炎を発症している。(右)ワクチン投与群では、著明に抑制されている(出所:大阪公大プレスリリースPDF)
同成果は、大阪公大大学院 医学研究科ゲノム免疫学の植松智教授、同・藤本康介准教授、同・横田知衣子大学院生(大阪市立大学大学院 医学研究科)らの研究チームによるもの。詳細は、日本炎症・再生学会が刊行する炎症と再生医療に関する全般を扱う欧文学術誌「Inflammation and Regeneration」に掲載された。
肺炎球菌は乳幼児の鼻咽頭において高頻度に検出され、小児や成人に中耳炎、副鼻腔炎、菌血症を伴わない肺炎といった非侵襲性感染症などを引き起こす。また、髄膜炎や菌血症を伴う肺炎などの侵襲性肺炎球菌感染症を引き起こす場合もあり、2013年には感染症法の5類感染症に追加されている。
肺炎球菌感染症の予防にはワクチンが有効とされているが、そのワクチンが普及したことで、近年はワクチンでは効果がない血清型も増加している。現在、肺炎球菌の血清型は100種類ほど同定されているが、現在のワクチンではカバーできない血清型を原因とする肺炎球菌の感染増加が課題となっている。そのため、すべての血清型に効果を呈する次世代型ワクチンの開発が強く望まれていた。
そうした中で研究チームは、あらゆる粘膜面に「免疫グロブリンA」(IgA)を主体とした抗原特異的な粘膜免疫応答を自在に誘導することができる粘膜ワクチンを、2019年に開発している。しかし、同技術に使用しているワクチン製剤の基剤のうち一部が、副作用のためヒトには使用できない状況であり、臨床応用に向けた基剤の変更が必要だったことから、ヒトで使用可能なもののみを用いた新しい粘膜ワクチンの開発を試みたとする。
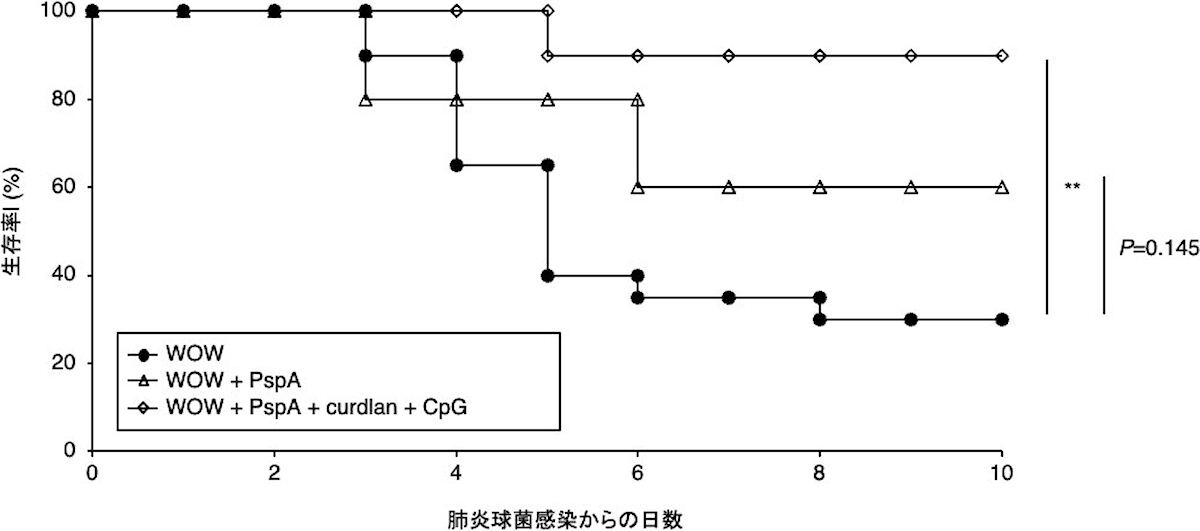
今回の研究では、ヒトで使用可能な「水中油中水型(WOW)エマルジョン」を用いたとのこと。その結果、2019年の粘膜ワクチンと同等の粘膜免疫応答を誘導できる新しい粘膜ワクチンの開発に成功したとする。このワクチン技術と幅広い血清型をカバーすることが可能な抗原「肺炎球菌表層タンパク質(PspA3+2)」を組み合わせて、肺炎球菌感染症に対する効果をマウスモデルで確認できたとしている。
-

水中油中水型エマルジョンの構造。CpGは自然免疫受容体として知られているToll様受容体9番のリガンドのこと。カードランは細菌の菌体成分で、Dectin-1のリガンドを指す(出所:大阪公大プレスリリースPDF)
さらに研究チームは前臨床試験として、肺炎球菌粘膜ワクチンの効果をカニクイザルで確認することにしたという。そして同サルにおいても、マウスと同じように呼吸器粘膜面での抗原特異的なIgAの誘導を示すことが確かめられ、またワクチン群では、肺炎球菌感染による肺炎を明らかに抑制できたとした。
今回の研究成果により、今後臨床応用に向けた開発を進展できるとする。また、肺炎球菌以外の抗原についても今回のワクチン技術は応用可能だといい、あらかじめ注射によって免疫を獲得しておけば、その後抗原の粘膜投与だけで効果的な免疫を誘導できるため、次世代のワクチン技術として今後の感染症医療への貢献が強く期待されるとしている。