名古屋大学(名大)は、自治医科大学神経内科学との共同研究により、本来は生体内に存在する微小なリボ核酸である「マイクロRNA」と、「アデノ随伴ウイルスベクター」を用いた核酸医薬療法を開発し、神経変性疾患の1種である「球脊髄性筋萎縮症」のモデルマウスにおいて治療の有効性を明らかにしたと発表した。
成果は、名大 大学院医学系研究科 神経内科学の祖父江元教授、宮崎雄大学院生らの研究グループによるもの。研究の詳細な内容は、英国時間6月3日付けで英科学誌「Nature Medicine」オンライン版に掲載された。
運動ニューロン病、パーキンソン病、アルツハイマー病などの神経変性疾患は神経難病といわれており、現在のところは本質的に病態を抑える有効な治療法が見出されていない。
研究グループは、今回その1つである球脊髄性筋萎縮症をターゲットとして、マイクロRNAとアデノ随伴ウイルスベクターを用いたまったく新しい核酸医薬療法を開発し、病態を抑止することに成功した。
球脊髄性筋萎縮症は遺伝性の神経変性疾患の1つであり、「アンドロゲン受容体」の異常によって神経変性が引き起こされることが確認されている。球脊髄性筋萎縮症は男性にのみ起こる疾患で、男性ホルモンの「テストステロン」依存性であることがその理由だ。全身の筋力低下や食べ物の飲み込みにくさなどの症状自体も男性のみに見られる。
このように、球脊髄性筋萎縮症は原因遺伝子や病気のメカニズムが明らかになってきているものの、生命予後を改善させるほどの有効な治療法が未だないのが現状だ。
球脊髄性筋萎縮症では、異常を持つアンドロゲン受容体遺伝子から異常な(本来とは異なるアンドロゲン受容体の情報を持つ)「メッセンジャーRNA」が転写され、その結果、異常なアンドロゲン受容体タンパク質が合成されてしまう。
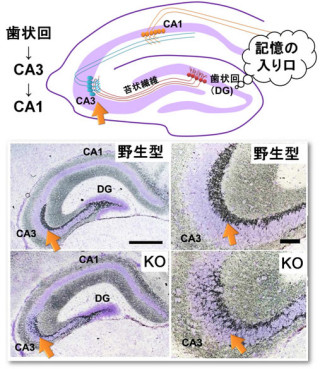
この異常なアンドロゲン受容体は、本来生体にとって重要な働きを果たす正常なアンドロゲン受容体と同じ役割を果たせず、神経組織や筋肉などに障害を及ぼす(画像1)。
研究グループは今回の研究において、タンパク質「CUGBP,Elav-like family member2(CELF2)」がこの異常アンドロゲン受容体のメッセンジャーRNAに結合し、これを安定化させる(異常アンドロゲン受容体のメッセンジャーRNAの半減期を長くする)ことを発見。
さらに、「マイクロRNA-196a」がこのCELF2の発現を抑制することで、間接的に異常アンドロゲン受容体のメッセンジャーRNAの分解を促進することを明らかにした。異常メッセンジャーRNAの分解を促進すると、それから合成される異常アンドロゲン受容体タンパク質の量も減少することも確認されている(画像2)。
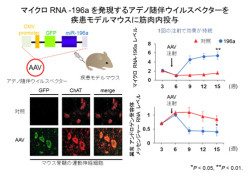
上記の結果をふまえ、マイクロRNA-196aを発現する遺伝子をアデノ随伴ウイルスベクターに組み込み、球脊髄性筋萎縮症のモデルマウスに投与したところ、1回のみの筋肉内注射で全身の組織にウイルスベクターが拡がった。
また、拡がったウイルスベクターからマイクロRNA-196aを発現する遺伝子がモデルマウスの持つ遺伝子に組み込まれ、ここで作られるマイクロRNA-196aがCELF2の発現を抑制し、結果として異常アンドロゲン受容体タンパク質の合成を抑えていることに成功したのである(画像3)。
なお、神経変性疾患の哺乳類モデル(マウスなど)において、マイクロRNAを用いた遺伝子治療法の有効性を示したのは、世界初の成果だ。
疾患の原因となる異常な遺伝子から転写される異常メッセンジャーRNAをマイクロRNAによって制御する方法論は、「脊髄小脳変性症」を初めとするほかの神経変性疾患においても応用が期待される。これらの神経変性疾患に多くの患者や家族が直面している問題を鑑み、早急な臨床応用へ向けた努力を続けたいと研究グループはコメントしている。