その結果、細胞傷害性を誘導することができるヘアピンDNA集合技術、つまり、さまざまながん細胞で過剰発現している細胞内マイクロRNA-21(miR-21)が引き金となって、設計した「化学合成短鎖ヘアピン核酸対」(oHPs)が、ハイブリダイゼーション連鎖反応(HCR)を引き起こして集合体を作ることが発見された。
-

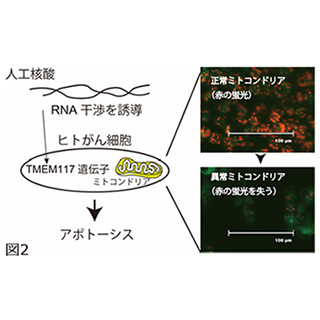
人工核酸oHPsによる細胞内集合体形成。特定の配列のmiRNAが過剰に発現しているがん細胞の中にoHPsが入ると、miRNAを起点にしてハイブリダイゼーション連鎖反応がおこり、長い二本鎖DNAを形成する (出所:東大プレスリリースPDF)
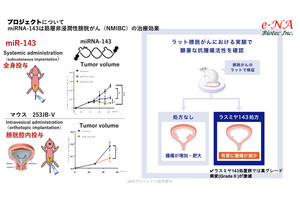
がん細胞の中で生じたoHPs集合体産物は、cGAS-STING経路を経由してI型インターフェロンの発現を誘導し、最終的に細胞死へと至らせたという。ヒト子宮頸がん由来細胞(HeLa)、ヒトトリプルネガティブ乳がん由来細胞(MDA-MB-231)、マウス悪性黒色腫(メラノーマ)由来細胞(B16)など、miR-21が過剰発現して、かつSTINGが十分に発現するがん細胞に対してoHPsは有効に作用することが確認された。さらに、B16担持マウスに対してoHPsを局所注射した結果、腫瘍の成長が強く抑制される様子が観察されたとした。
今回見出された短いDNAoHPsによる、miR-21過剰発現条件下での細胞内二本鎖形成は、標的腫瘍退縮に向けた選択的な免疫増幅・増強回路として利用された最初の例だという。既知の核酸医薬とはまったく異なる機序を示す、新分類の核酸医薬候補で、oHPsは、従来の抗がん剤の効き方と異なるため、それらを補完する役割が期待されるとした。
今後は、oHPsの薬剤としての有効性をさまざまながん種で検討して、特定のがんを標的にした効果的な抗がん性核酸医薬の誕生に向けた研究開発が進展することが期待されるとしている。