理化学研究所(理研)と千葉大学は2月4日、マウスにおける「原始内胚葉幹細胞(PrES細胞)」の樹立に成功したと発表した。
同成果は、理研生命医科学研究センター(IMS)免疫器官形成研究チームの近藤隆上級研究員、同・公文麻美テクニカルスタッフII(研究当時)、同・古関庸子テクニカルスタッフII、同・飯塚裕介専門技術員、同・川元由里衣専門技術員、同・椙下紘貴大学院生リサーチ・アソシエイト(研究当時)、同・古関明彦チームリーダー(千葉大学大学院医学研究院細胞分子医学教授)、理研 IMS 統合ゲノミクス研究チームの遠藤高帆技師、同・渡辺貴志技師、千葉大大学院 医学研究院 細胞分子医学の大日向康秀講師(理研 IMS 免疫器官形成チーム 客員研究員兼任)、同・更屋敦則技術専門職員、かずさDNA研究所の小原收副所長らの共同研究チームによるもの。詳細は、米科学誌「Science」に掲載された。
精子と卵が出会うことで受精卵となって、生命は第1歩を踏み出す。その受精卵が卵割を繰り返したのちに形成される初期胚「胚盤胞」は、全部で数十個の細胞からなる組織であり、主に胚を派生させる「エピブラスト」、胎盤を派生させる「栄養膜」、卵黄嚢を派生させる「原始内胚葉」の3つの細胞系譜を有していることは知られているが、このような単純な構造がどのように生命の始まりとして機能するのかは、よくわかっていないという。
また、胎盤は受精卵から作り出される胚体外組織であり、胎盤が胚と母体とのインタフェースとして機能し始めるのは、マウスの場合は受精後10日目以降で、それ以前は卵黄嚢が胚発生を支持するのに必須であるとされている。このように胚発生は単に胚だけではなく、胎盤や卵黄嚢と密接に連携して進行することが分かっているが、卵黄嚢の発生や発生初期における、胚および胎盤との組織間相互作用についてもほとんど解明されていないという。
こうした胚発生の仕組みを調べるのに、各細胞系譜に由来する幹細胞を試験管内で分化させることが有効とされており、これまでにエピブラストからはES細胞(胚性幹細胞)、栄養膜からはTS細胞(栄養膜幹細胞)が樹立されているものの、残る原始内胚葉の幹細胞(PrES細胞)の樹立は実現しておらず、PrES細胞の樹立が求められていた。
-

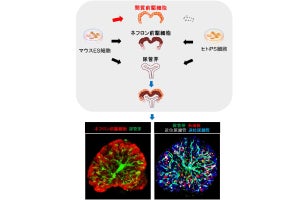
(左)原始内胚葉を欠失させたマウス胚盤胞に、PrES細胞が注入されることで得られたキメラ(受精後18.5日)。(右)胚盤胞と生じる受胎産物(胚と胚体外組織)の模式図。胚盤胞はエピブラスト(赤)、栄養膜(緑)、原始内胚葉(青)の3種、全部で数十個の細胞で構成される(左)。胚はエピブラストから、胎盤は栄養膜から、卵黄嚢(壁側内胚葉、臓側内胚葉、境界領域内胚葉)は原始内胚葉から生じる (出所:プレスリリースPDF)
そこで研究チームは今回、マウス胚盤胞をさまざまな培養条件に置き、PrES細胞を樹立・維持可能な条件の探索を実施。その結果、無血清培地にグリコーゲン合成酵素3(GSK3)阻害剤である「CHIR99021」、線維芽細胞増殖因子の「FGF4」、抗血液凝固薬の「ヘパリン」、血小板由来増殖因子の「PDGF-AA」の4種類を添加することで、PrES細胞の樹立に成功したという。
単一細胞遺伝子解析により、樹立されたPrES細胞が分析されたところ、ES細胞やTS細胞とは異なる遺伝子発現パターンが示され、受精後4.5日目胚の形成直後の原始内胚葉とよく似ていることが確認されたほか、PrES細胞にはES細胞などの多能性幹細胞のマーカーである「OCT4」や「E-カドヘリン」などと、内胚葉のマーカーである「GATA6」や「SOX17」などが共発現しており、既知の幹細胞とは異なる特徴的な遺伝子発現パターンが示されたという。
また、PrES細胞の機能解析として、PrES細胞を胚盤胞に注入したところ、速やかに原始内胚葉に取り込まれることが観察されたとするほか、PrES細胞が注入された胚盤胞を偽妊娠マウスの子宮に移植したところ、PrES細胞は壁側内胚葉、臓側内胚葉、境界領域内胚葉の全細胞の派生に寄与し、胚盤胞の細胞とPrES細胞が混ざったキメラを形成する能力を保持していることも判明したとする。
さらに、4~8細胞期胚を、細胞の増殖や分化を制御するMEKを阻害する「PD0325901」で処理すると、原始内胚葉を欠失した胚盤胞を作製できるが、この胚盤胞は卵黄嚢を形成できないため、発生初期に死んでしまうが、原始内胚葉を欠失させた胚盤胞にPrES細胞を注入すると、PrES細胞がすべての原始内胚葉系列の組織を派生させ、正常な仔マウスが生まれることも確認したという。
この結果は、PrES細胞が原始内胚葉を補完する能力を持つことを意味するものであり、ES細胞、TS細胞に続いて、PrES細胞も樹立され、胚盤胞を構成するすべての細胞の幹細胞がそろったことを意味すると研究チームでは説明しているほか、3つの幹細胞を試験管内で組み合わせることで、人工的に胚様の構造を作製できるかどうかの調査として、ES細胞、TS細胞、PrES細胞を特殊な培養皿を用いて順に組み合わせて培養したところ、作製した組織(ETP複合体)の単一細胞遺伝子発現解析からは、胚の着床前後の過程をある程度再現できることが判明したとしている。
-
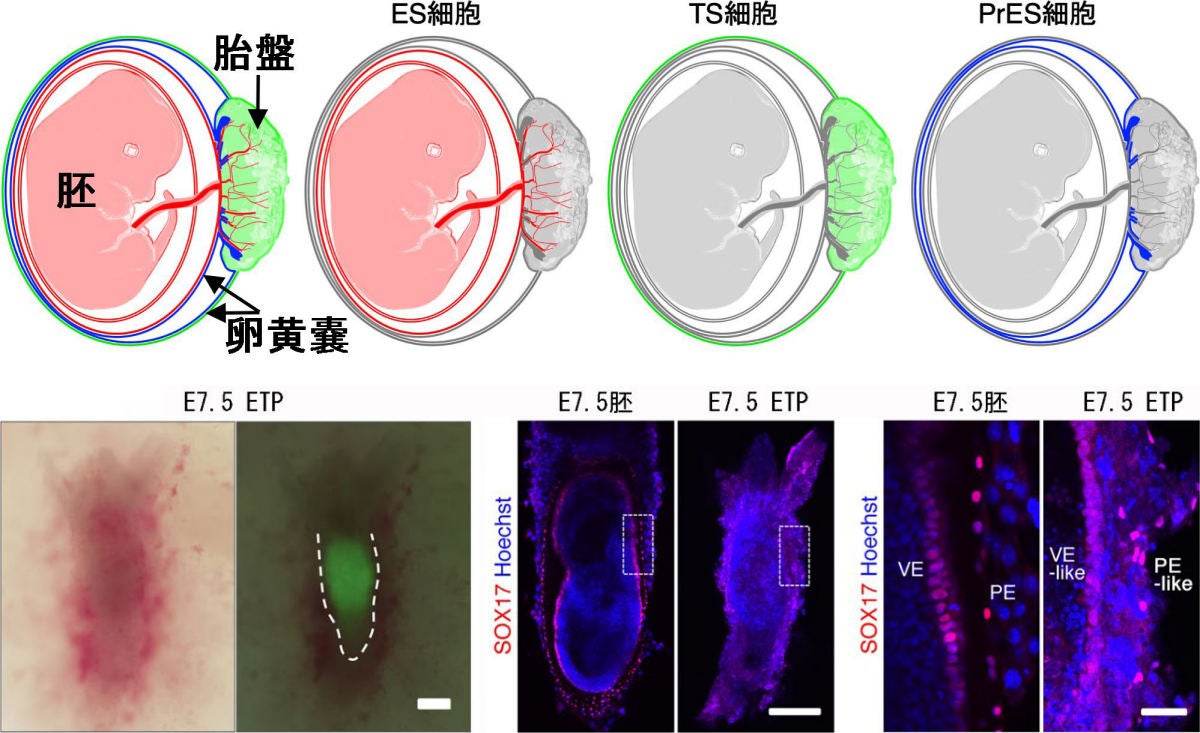
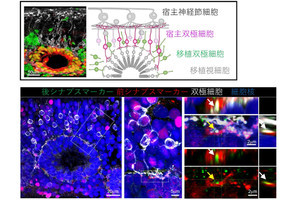
(上)ES細胞、TS細胞、PrES細胞の寄与の模式図。ES細胞は主に胚を、TS細胞は主に胎盤を、PrES細胞は主に卵黄嚢を形成する。これら三つの幹細胞がそろうことで、すべての受胎産物(左)がカバーされる。(下)マウスETP複合体から派生した胚様構造(妊娠7.5日目) (出所:プレスリリースPDF)
なお研究チームでは、今回、卵黄嚢の幹細胞であるPrES細胞が樹立されたことで、特に初期胚内での細胞間相互のシグナル伝達ネットワークの理解、3種類、数十個の細胞の相互作用で生命の萌芽が形成される過程の解明が進むことが期待できるようになるとしているほか、人工胚の作製や人工生命の研究の進展も期待できるとしている。