東京医科歯科大学(TMDU)と九州大学は3月15日、肝臓内の細胞間接着・接触が糖代謝異常を引き起こすメカニズムを発見したと発表した。
同成果は、東京医科歯科大学大学院医歯学総合研究科分子内分泌代謝学分野/九州大学大学院医学研究院病態制御内科学分野 小川佳宏教授、東京医科歯科大学医学部附属病院 土屋恭一郎助教、同大学院生の宮地康高氏らの研究グループによるもので、3月14日付けの米国科学誌「Cell Reports」に掲載された。
肥満になると、肝臓に好中球やリンパ球などの白血球が集積し、肝臓におけるインスリン抵抗性と糖代謝異常を引き起こすことにより2型糖尿病の原因のひとつになることが知られている。肝臓には肝類洞内皮細胞(liver sinusoidal endothelial cells:LSEC)と呼ばれる類洞(血管)と肝細胞を隔てる細胞が存在するが、肥満において白血球が肝臓に浸潤する際、どのような分子機構でLSECと相互作用するかは不明となっていた。また、肝臓に浸潤した白血球は肝細胞と接触するが、両細胞間の物理的な相互作用が糖代謝機能に及ぼす影響は明らかになっていなかった。
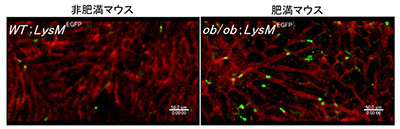
同研究グループは今回、白血球のひとつである顆粒球特異的に蛍光タンパクEGFPを発現する遺伝性肥満マウスの生体イメージングを行い、対照の非肥満マウスと比較して多数の顆粒球が肝類洞に接着していることを発見。また、電子顕微鏡を用いた解析では、多数の白血球が肝細胞の間に浸潤していることがわかった。
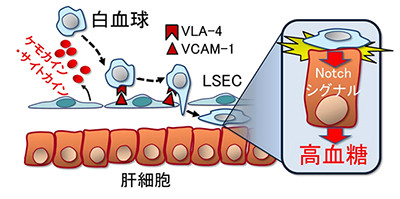
また、肥満マウスのLSECでは、ケモカインや炎症性サイトカイン、接着因子遺伝子の発現が上昇、LSECの細胞表面において接着因子のひとつであるVCAM-1の発現が増加し、VCAM-1と結合するVLA-4を介した白血球との細胞接着が亢進していることを明らかにした。肥満マウスにVLA-4の働きを阻害する抗体を投与したところ、顆粒球とLSECの接着および肝臓への白血球の浸潤が抑制され、高血糖が改善したという。
さらに、肥満マウスの肝臓では浸潤した白血球が肝細胞と接触している様子が電子顕微鏡で観察されたことから、マウス肝臓内の白血球と肝細胞を実際に接触させて培養したところ、肝細胞からの糖の産生が増加した。このとき、細胞同士の接触により活性化されるシグナルであるNotchシグナルを介して、糖の産生を促進する酵素の遺伝子発現が増加することがわかった。
同研究グループは、今回の成果により肝臓内の細胞間の物理的相互作用が新しい糖尿病の治療標的になることが期待されると説明している。