がん治療として一般的な薬物療法(化学療法)。いわゆる抗がん剤を用いた治療法だが、吐き気や食欲不振、脱毛、臓器の障害など、さまざまな副作用が生じることが知られている。そうした副作用を減らし、患者のQOL(クオリティ・オブ・ライフ/生活の質)を向上させる技術の1つとしてDDS(ドラッグ・デリバリ・システム)が期待されており、世界中で研究開発競争が繰り広げられている。その中の1社、韓国CNPharmは、「無苦痛抗がん剤(Pain-free Anticancer Drug)」と呼ぶ新たなDDSを開発。前臨床を完了し、2019年より米国と韓国にて、すい臓がんを対象に、グローバル臨床1/2aを開始する計画であることを明らかにした。
なぜ抗がん剤は副作用を引き起こすのか
そもそも、なぜ抗がん剤の投与によって、さまざまな副作用が引き起こされるのか。簡単に言えば、抗がん剤が有するがん細胞をも破壊する毒性が、血中に溶け、正常な細胞にもダメージを与えてしまうため、と言える。もちろん、近年はがん細胞に特有の分子を見分け、それをターゲットに狙い撃ちする分子標的薬なども開発され、副作用を少なくできるようになってきたが、それでも正常な細胞にも多少は標的とする分子が存在してしまうため、皆無、というわけには行かない。
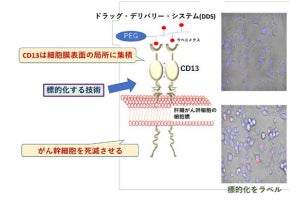
DDSは、さらにこうした取り組みを進化させ、抗がん剤をターゲットの腫瘍組織まで送り届け、そこでしか効果を発揮させない、という仕組みであり、副作用の影響をさらに低減できる技術として期待されている。
また、抗がん剤を投与する場合は、薬理作用が期待され、かつ合理的に安全な投与量を無毒性量(NOAEL)を用いるなどして導き出す必要があるが、「もし、副作用を起こすことがなければ、NOAELを超えた量を投与できるようになる可能性が高まり、それにより、より高い効果を期待することができるようになる。我々の技術は、そうしたことを意識したものとなっている」と、同社でVice Presidentを務めるPark,Kwang Sil氏は自社技術を説明する。
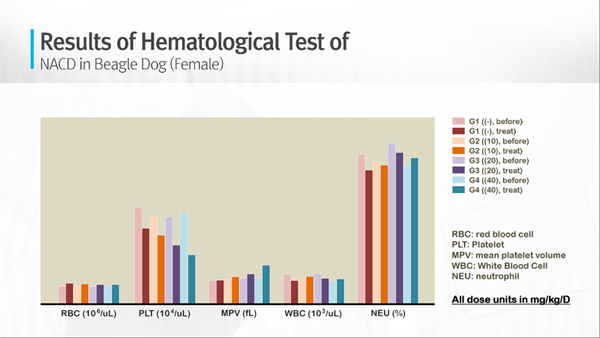
実際に、動物を用いた試験にて、赤血球や血小板、平均血小板容積、白血球、好中球といったさまざまな成分を調べたところ、副作用が起きにくいという結果を得たとする。また、薬剤の半減期が延長できる点も同技術の特徴として挙げられるとのことで、長いものでは10倍程度に伸ばせ、効果を長時間維持できるようになるとする。
DDSの仕組みはどうなっているのか
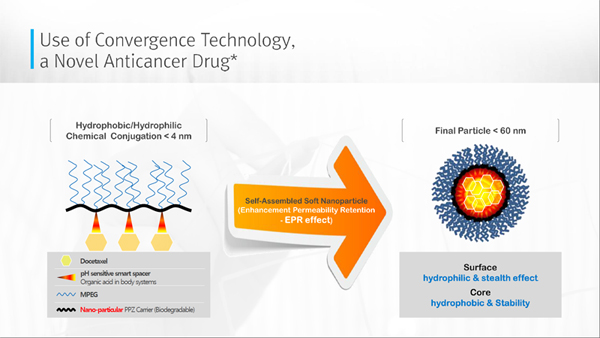
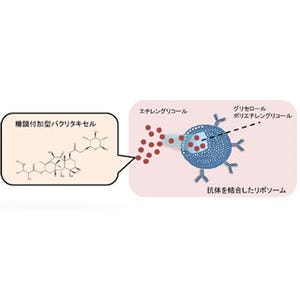
では、どういったDDS技術でこうした成果を実現したのか。そのポイントはカプセル化のノウハウにあると同社では説明する。
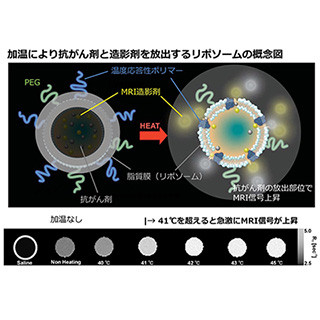
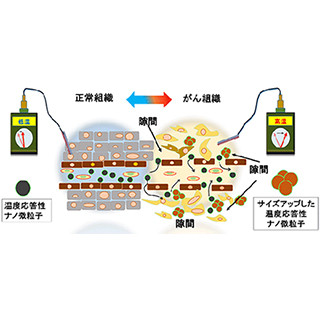
DDSの直径は60nm程度にコントロールされており、「これにより、その中に入る薬剤の粒子経はより小さなものとなる。その結果、より多くの薬剤が腫瘍に届きやすくなる。それは蓄積しやすくなるという意味でもあり、その結果、多くの薬剤がエンドサイトーシスにより、細胞内に輸送される」とするほか、体内でDDSが異物として認識され、分解されないように、表面をステルス化する必要があるが、メチル化されたポリエチレングリコール(MPEG)を高密度に形成することで、これを実現したとする。
すい臓がんでの実用化を目指す
同社では、同技術をまず難治性のすい臓がんでの実用化を目指すとする。なぜ、すい臓がんを選んだのか。同氏は、「米国ならびに韓国の専門家たちと協議したところ、多くの人から、この技術はすい臓がんの治療候補になるという意見が挙がった。体内での半減期の時間が長く、かつ60nmという粒子経から、すい臓がんに対しても高い作用をおよぼすことが期待されたからだ」と説明するほか、「もし、一番治療が困難ながんにおいて、効果が確認されれば、我々の技術はあくまでDDSの媒体となるものであるため、ほかのがん治療にも効果が期待できるようになる」と、自社の技術力に自身をのぞかせる。
また、「すい臓がんの治療であれば、アメリカ食品医薬品局(FDA)からオーファン・ドラッグ(希少疾病用医薬品)として承認を得られる可能性も高い。オバマ前大統領時代に打ち出されたがん撲滅に向けたムーンショット計画のような取り組みもあり、臨床試験の結果次第だが、10年もかからないうちに医師が活用できるようになることも期待できる」といった、商業的な側面も踏まえたうえでの戦略であるとする。折りしも米国の大多数の州で、「Right to try laws(試す権利の法律)」いわゆる第1相試験を終えた治験薬を、患者が医師と製薬企業の合意のもとに試すことを認める権利を行使できる法律が整備されてきており(2018年5月30日には、トランプ大統領が同法に対しての署名を行なっている)、2019年に実施するグローバル臨床1/2aにて、良い結果を得られれば、さらに早い段階で、多くの患者が試す環境が構築されている可能性もある。
なお、同社では、薬剤そのものを開発するつもりはないとしている。「そこは製薬企業の役目だ。抗がん剤は多く市場に出回っているが、それをいかに毒性を抑えつつ、ターゲットとするがん組織に送達するかについては、抗がん剤の開発に比べては優先度は低かった。我々はそこにフォーカスすることで、既存薬の効果を高めることを目指している」と同氏が語る背景には、できるだけ多くの人に治療のベネフィット(恩恵)を届けたい、という思いが同社にはあるとのことで、今後も、1人でも多くの患者のQOLを高めていくことを目指し、研究開発を継続していくとしていた。