九州大学(九大)などは3月8日、がん組織の温度に応答して薬剤分子を集める仕組みを開発したと発表した。
同成果は、九州大学大学院薬学研究院 唐澤悟准教授、荒木健氏、臼井一晃助教、量子科学技術開発機構 青木伊知男博士、村山周平博士らの研究グループによるもので、3月7日付けの米国科学誌「Nano Letters」オンライン版に公開された。
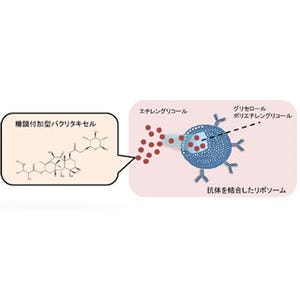
体内の薬剤分布を量的、空間的、時間的に制御する薬剤運搬技術であるドラッグデリバリーシステム(DDS)の研究が、がん治療研究のひとつとして進んでいる。従来のDDSは、血管に生じる「隙間」を利用して、数十~百nmサイズのナノ微粒子中に薬剤を内包させ、がん病巣へ薬剤を集積させるという手法が一般的だった。しかし、この方法では薬剤が正常な組織にも分布するため、副作用を発症するなどの問題があった。
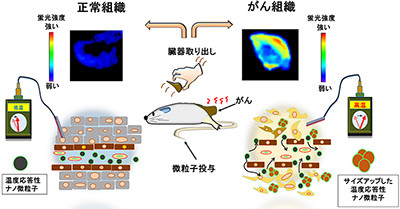
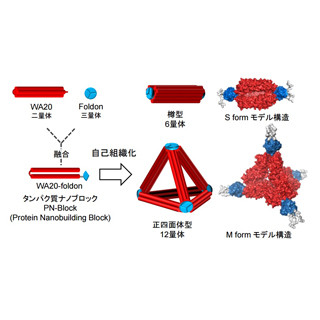
今回、同研究グループは、がん組織が正常な組織よりも温度が高くなる性質をもつことに着目。温度が変わると分子が集合して形やサイズが変化する「温度応答性ナノ微粒子」を研究し、がん組織に分子を集めて留まる方法を開発した。同ナノ微粒子は、ヒトの体温よりも少し高温の温度域で自ら集合して大きなサイズになる。
|
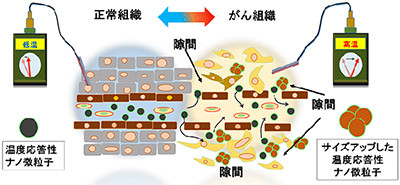
がん組織中には、血管内皮細胞の周辺に数十~数百nmの隙間や、がん細胞自身の周辺にも隙間が生じる。また、がん細胞は活発に活動するため正常組織よりも温度が高く、乳腺がんが2℃程度高温であると報告された例がある。同研究グループは、温度応答性ナノ微粒子(緑色の球)ががん組織の隙間に入り込みサイズアップし(茶色の球)、がん中に留まるように設計を行った (出所:科学技術振興機構Webサイト) |
同ナノ微粒子は、水へ溶かすと透き通った溶液になるが、高温にすると微粒子同士が集まり始め、溶液に濁りが生じる。同ナノ微粒子のサイズ変化を計測した結果、透明溶液中では10nm程度の小さい球状の微粒子だが、濁り始めると100~1000nm程度の大きな微粒子にサイズアップする。粒子は、35℃、37℃、40℃と異なる温度でサイズアップするよう作り分けることができる。
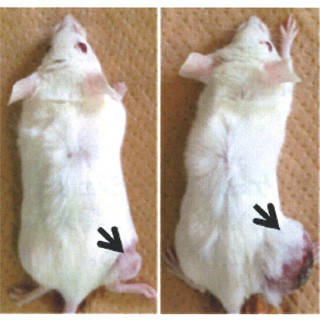
実際に、がんを持つマウスへ蛍光分子を取り付けた同ナノ微粒子を投与したところ、がん細胞の温度に応答してナノ微粒子ががん組織に集積する様子が蛍光イメージングで観察された。また、蛍光強度は上述の微粒子のサイズが大きくなる温度に依存し、35℃、37℃、40℃の順で蛍光が強くなった。
今回の成果について同研究グループは、従来のDDSが抱えていた、がん細胞以外への副作用を解決するだけではなく、低い投与量で負担が少ない、新たながん診断や治療に役立つことが期待されると説明している。