東北大学は7月18日、細胞が外界の物質を取り込む際の直径数100nmの陥入構造を生きた細胞で可視化し、その分子機構に関して新しい知見を手に入れることに成功したと発表した。
同成果は、京都大学生命科学研究科の吉村成弘 准教授、吉田藍子氏(研究当時、北海道大学博士研究員)、東北大学学際科学フロンティア研究所の鈴木勇輝 助教、オリンパスらの研究グループによるもの。詳細は、国際学術誌「PLOS Biology」オンライン版に掲載された。
細胞膜は細胞内部と外界とを隔てる障壁であると同時に、細胞が外界と情報をやりとりするための重要な中継地点だ。特に、細胞が外界の物質を細胞内に取り込む仕組みは、細胞の環境応答、神経伝達などにおいて重要であり、細胞活動に必要不可欠となっている。
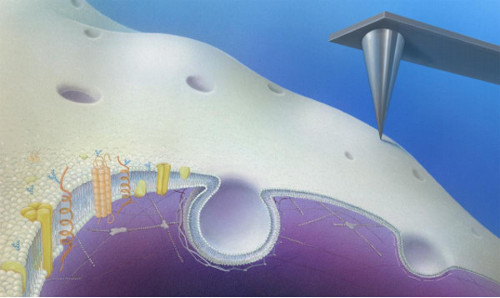
これには、細胞膜に埋め込まれたチャンネルや受容体などが外界の分子を内部に輸送する経路の他に、細胞膜の陥入により外の物質を内部に取り込む仕組み(エンドサイトーシス)が中心的役割を果たしている。これまで、エンドサイトーシスに関与するタンパク質が多く同定されてきたが、実際にどのような形状変化を経て陥入が進行するかに関しては、電子顕微鏡写真を並べて推測するに留まっていた。
研究グループは今回、「走査型プローブ顕微鏡」と呼ばれる特殊な顕微鏡が用いて、この仕組みの解明を試みた。先端径が数nmの鋭利なプローブで試料表面を「なぞる」ことでその形状を可視化する。しかし、細胞膜は「脂」でできた平面膜なのでとても柔らかく、従来の同型顕微鏡では可視化は不可能だった。
この問題を解決するべく「生きた細胞の細胞膜を可視化するための高速走査型プローブ顕微鏡」の開発に取り組み、細胞に与える力を大幅に弱くすることで、細胞膜の形状を数nmの分解能で可視化する事に成功した。
また、高分解能の蛍光顕微鏡と組み合わせることで、タンパク質の局在を同時に可視化する技術を確立し、エンドサイトーシスに伴う膜形状変化のメカニズムを分子レベルで解明することに成功したという。
なお今回の成果を受けて研究グループは、顕微鏡技術の発展とともに進歩してきた生物学の歴史を考えると、生物学的展開の可能性を十分に秘めた成果であり、エンドサイトーシスのみに留まらず、さまざまな生命現象に応用できると可能性があると説明している。