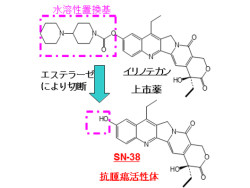
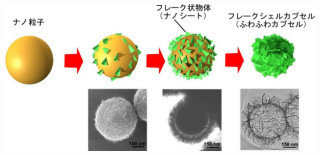
東北大学と京都大学は9月6日、強い抗がん特性を有することで知られる「SN-38」(画像1)の「2量体化合物」(画像2)を新規合成し、難水溶化とした後、同化合物を「再沈法」(対象化合物の溶液を貧溶媒中に急速注入し、溶質を再沈澱させる手法)という独自のナノ化技術を駆使して、約50nmの抗がん性「ナノ純薬(Pure Nano Drugs:PND)」(画像3)を作製することに成功したと発表した。
成果は、東北大学 多元物質科学研究所の笠井均准教授、京大 物質-細胞統合システム拠点(WPI-iCeMS)の村上達也助教らの研究グループによるもの。研究の詳細な内容は、国際学術誌「Angewandte Chemie」電子版、印刷版共に掲載される予定だ。
薬剤用に合成される化合物に対しては、水に溶解するような置換基を導入することで、水溶性薬剤として使用することを目指すのが一般的だ。ところが、最近の合成技術の高度化もあり、一見複雑な置換基を有する化合物が増えてきており、約半数が難水溶性を示すという現状がある。
この場合、高い分散安定性を有しつつ、「Enhanced Permeation and Retention(EPR)効果」のような効率的な薬理効果を発現させるためには、ナノ製剤化が不可欠だ。ちなみに、EPR効果は、20~100nmのナノ製剤に発揮しやすいとされるが、その中での最適サイズは明らかになっていない。
このような状況下、研究グループは、難水溶性で抗がん性を有する化合物として知られたSN-38に着目。実は、SN-38に水溶性置換基を付けたイリノテカンはすでに上市されているが、人体に投与後、「カルボキシエステラーゼ」により、薬理活性を有するSN-38に転換して抗がん作用を示すという、そのままの状態では不活性、もしくは明らかに活性の低い「プロドラッグ」だ(画像1)。
そこで研究グループは、SN-38について東北大で20年間以上追及されてきた「有機ナノ結晶の作製技術」である再沈法を用いて、SN-38のみで構成される「キャリアフリー」で、かつ疎水性表面を有するPNDを創製すれば、EPR効果を発現しつつ、高い細胞浸透性を有する副作用のない「ドラッグデリバリシステム(DDS)」となり得ると着想。ただし、これまでにこのような発想が抗がん剤として試用されたことはなかった。なお、キャリアフリーとは、薬化合物はキャリアとしてのポリマーなどに包接されるのが一般的だが、キャリアフリーではポリマーなどを使用せず、ナノ薬剤だけでDDSを行う設計である。
これは、一般に細胞膜を構成するリン脂質においては、親水性の物質に比べて、疎水性の物質の方が細胞内への透過性がよいとされていることに基づくものである。しかし、上記のアイディアをSN-38に適用し、再沈法によりナノ粒子化を試みた結果、SN-38のナノファイバーしか得られないことが明らかとなった(画像4)。
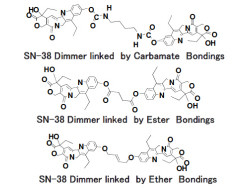
再沈法の特徴としては、貧溶媒である水に対する溶解度がより低い化合物を対象とした時、ナノ粒子化が速くなり、微小化しやすくなることがすでに判明している。そこで、画像2のようなSN-38の2量体化合物を新規合成し、水に対する溶解度を下げることにより、再沈法にてナノ粒子を作製することが着想された。
結果、SN-38「カルバメート結合」や「エステル結合」で連結した2量体化合物を合成することに成功し、それらの化合物のナノ粒子化を試みた結果、走査型電子顕微鏡観察により、画像3のような約50nmのナノ粒子が得られることがわかったのである。加えて、2量体ナノ粒子の水分散液は、安定な分散性を示すことや冷凍保存後、超音波照射で、分散液に戻ることも明らかになった。
作製されたSN-382量体ナノ粒子には、がん細胞内への浸透性が向上するという特徴が見られることがわかったため、イリノテカンと比較する目的で、約10倍希薄な低濃度の水分散液をがん細胞「HepG2細胞」の培地に投入したところ、がん細胞をイリノテカン以上に死滅させることができることが判明した。
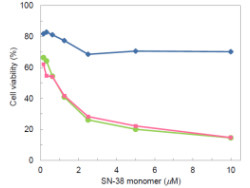
その細胞試験が行われた結果が画像5のグラフだ。画像5の縦軸に薬剤投与の48時間後のがん細胞の生存率を、横軸にSN-38の単量体の濃度を示した。その結果、再沈法により作製したSN-382量体ナノ粒子(ピンクの■、黄緑の●のライン)が、現在上市されているイリノテカンよりも、高い抗腫瘍効果を示すことが判明したのである。
DDS技術に関する先行報告例は多数あるが、ポリマーに包接する研究が一般的であり、キャリアフリーのナノ薬剤粒子に関する既報研究論文の数はごく少数だ。さらに、抗がん性ナノ薬剤に関する研究は皆無といえる状況だという。また今回の研究のように、がん細胞内部までDDSすることを念頭に入れている技術もこれまでにはなかった。
今回の研究で開発されるナノ純薬の優位性としては、キャリアフリーであるゆえにポリマーによる副作用がない上、「再沈法と2量体化によるナノ純薬の作製」という独自に開発された技法は、低コストで、大量生産が可能な手法であることが挙げられる。
さらに、EPR効果やステルス効果が発現しやすいサイズであり、画像5のグラフで見られるように上市薬であるイリノテカンの1/10以下の投与量としても優れた薬効を発揮できる可能性を有する点も魅力的だ。
研究グループは今後、副作用のないDDSに向けて、企業への技術移転を図ると共に、マウスなどの小動物を用いたin viboの実験系に進む予定としている。また将来的には、少量の使用で、効果的なPNDによるドラッグデリバリの実用化を目指すとした。