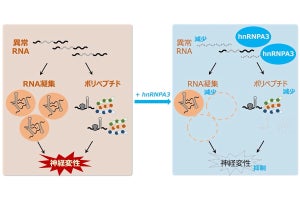
北海道大学(北大)、浜松医科大学、産業技術総合研究所(産総研)の3者は3月31日、脳内で分泌されるペプチド「p3-Alcβ」が神経細胞中のミトコンドリアを活性化することにより、アルツハイマー病(AD)の原因因子「アミロイドβ」(Aβ)が引き起こす神経毒性を抑制することを見出したと発表した。
同成果は、北大大学院 薬学研究院 認知症先進予防・解析学分野の鈴木利治特任教授、同・大学院 生命科学院の齋藤遥大学院生(研究当時)、浜松医科大の尾内康臣教授、産総研 生物プロセス研究部門の羽田沙緒里主任研究員、浜松ホトニクス 中央研究所の塚田秀夫主幹、ペプチド研究所の熊谷久美子サイエンスアドバイザーらの共同研究チームによるもの。詳細は、実験医学の分野全般を扱うオープンアクセスジャーナル「EMBO Molecular Medicine」に掲載された。
高齢化の影響を受けて注目が集まるADについては、アミロイド前駆体タンパク質(APP)から切り出されたAβが細胞外に分泌されることで多量体(オリゴマー)が形成され、それが神経細胞のシナプスを傷害し、神経毒性を現すことがAD発症の引き金になることがわかってきた。
しかし、形成される多様なAβオリゴマーが、神経伝達物質受容体などのさまざまな標的タンパク質を介して神経毒性を発現することや、AD発症・悪化のメカニズムには個人差があるといった複雑性が、有効な治療法の開発を困難にしている。中でも、孤発性ADの多様な発症機構の解明と、その多様性に対応できる予防・治療法の開発が進んでいないという。
研究チームが見出したAlcadeinβ(Alcβ)は、神経細胞に特異的に発現する膜タンパク質だ。APPを切断する酵素により同じ退社様式切断され、p3-Alcβという37~40アミノ酸のペプチドを産生する。p3-AlcβはAβとは異なり非凝集性で、脳神経細胞から脳脊髄液中に分泌され、AD患者の脳脊髄液中では同ペプチドが減少することが確認されている。そこで今回の研究では、p3-Alcβの脳内における機能を、マウス胎仔脳由来の初代培養神経細胞とADマウスモデルを用いた実験により検証したとする。
p3-Alcβの神経細胞に対する効果を調べるため、Aβによる傷害を受けやすい大脳皮質および海馬由来のマウス初代培養神経細胞を使って、加齢やADで低下するミトコンドリアの活性評価実験が行われた。その結果、37アミノ酸のp3-Alcβ37の添加によって、神経細胞の代謝活性の増加と、ミトコンドリアが産生するエネルギー源である「アデノシン3リン酸」産生量の増加が認められたとする。神経細胞は分裂での増殖をしないため、これらの細胞生存シグナルの増加は、神経細胞のミトコンドリアの活性化を反映しているという。