マサチューセッツ工科大学(MIT)の研究チームは、リチウム空気電池の添加剤であるヨウ化リチウム(LiI)の有効性をめぐる論争に決着をつける研究成果を発表した。「LiIはリチウム空気電池材料には適していない」というのが同チームの結論だが、研究過程で得られた知見は、新たなリチウム空気電池材料を見つけるための指針を与えるものになったとしている。研究論文は「Energy & Environmental Science」に掲載された。
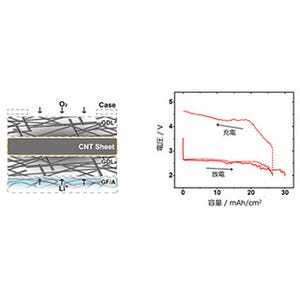
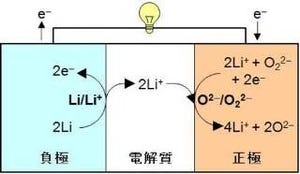
リチウム空気電池は、負極側に金属リチウム、正極側に空気極を用いる二次電池である。正極活物質である酸素は電池内に収める必要がなく、大気中にあるものを利用できる。このため重量当たりのエネルギー密度をリチウムイオン電池の約3倍と高い値にできると考えられ、次世代の高容量二次電池として活発な研究開発が続けられている。しかし、充放電を繰り返すと性能劣化が進むといった問題が解決しておらず、実用化には至っていない。
リチウム空気電池の理論上の性能が実デバイスで出ていない理由として、主に次の3つの問題があるとされている。(1)充電に高電圧が必要、(2)投入エネルギーに対する効率が低い、(3)空気極の安定性に問題があり、サイクル寿命が短い。
これまでの研究では、LiIを電解液に添加することによって電池のサイクル寿命が改善される効果があったと報告されていた。無機材料であるLiIは材料安定性が高く、有機系電解液の不安定性に起因する問題を解消できるため、数千回の充放電サイクルの実現を促すことができると主張する研究もある。
しかしその一方で、LiIの存在によって不可逆的な反応が進み、サイクル寿命が短くなったとするなど、矛盾する研究結果もあった。このため、LiIの有効性に関しては論争が続ていた。
研究チームは今回、リチウム空気電池の放電プロセスにおけるLiIの役割に注目し、LiIが電池にどのような影響を及ぼしているかを詳細に調べた。
紫外線および可視光による分光法などを用いて反応プロセスの分析を行った結果、LiIと水が存在する条件では、副反応物として過酸化リチウム(Li2O2)ではなく、水酸化リチウム(LiOH)が生成していることがわかった。
LiIには水の反応性を強める効果があり、水がプロトンを放出しやすくなるため、電池内でLiOHの生成が促進される。この反応から、LiIが充電プロセスを阻害する働きをしていると考えられる。したがって、LiOHの生成を抑える方法を見つけることができれば、LiIのような化合物をより有効に働かせられる可能性があるという。