理化学研究所(理研)は、大腸がんの発症にかかわると考えられているAPC(adenomatous polyposis coli)タンパク質の機能上重要となる部分の構造とその結合因子であるSam68との複合体の立体構造を決定することに成功し、大腸がんの新たな治療戦略に関わる重要な知見を得たことを発表した。同成果は、理研生命分子システム基盤研究領域の横山茂之領域長(東京大学大学院理学系研究科構造生物学社会連携講座教授)、Ella Czarina Morishita特別研究員らと、東京大学分子細胞生物学研究所、および東京大学大学院理学系研究科の秋山徹教授らとの共同研究によるもので、米国の科学雑誌「Structure」オンライン版に掲載されたほか、その表紙を飾った。
大腸がんは、他のがんに比べて患者数が増加傾向にあり、平成20年厚労省患者調査の概況によると日本では23万5千件の羅患が報告されており、世界的にもがんによる主要死因の1つになっている。
これまでに大腸がんの発症にかかわる重要な遺伝子の1つに「APC遺伝子」が同定され、大多数の大腸がん患者でこの遺伝子に変異が見いだされていることから、がん抑制遺伝子として機能していると考えられてきた。APCタンパク質は、2843アミノ酸残基からなる大きなタンパク質で、がん化や形態形成に重要な役割を果たすWntシグナル伝達経路に関するβカテニンに結合して、その分解を誘導することが知られている。大腸がんで見いだされる変異APCタンパク質はβカテニンの分解を誘導できないため、細胞内にβカテニンが蓄積され、TCF/LEFと呼ばれる転写因子と相互作用して、Wnt標的遺伝子の転写を促進し、それらの標的遺伝子が無制御な細胞増殖を刺激し、大腸がんを引き起こすことまでは分かっている(正常なAPCタンパク質は細胞質内でβカテニンに結合し、その分解を促進する結果、Wnt標的遺伝子の転写が制御され、細胞の過増殖が防止される)が、それ以上の分子レベルでの解明が十分ではないこともあり、効果的な治療法がまだ見つかっていないのが現状である。
APCタンパク質は他のタンパク質との結合に関わるドメインを有しており、多くのタンパク質はAPCタンパク質にあるアルマジロリピート(Arm)ドメインに結合するが、近年、東京大学の秋山徹教授の研究室が、APCタンパク質がβカテニンの分解誘導以外にも、Sam68というタンパク質とArmドメインを介して結合し、TCFの活性を制御してWntシグナルを阻害することを見いだした。
APCタンパク質とSam68の複合体はTCFのスプライシングを制御し、TCFのスプライスバリアントが過剰にできないようにしている。TCFのスプライスバリアントはWnt標的遺伝子を活性化し、過剰に存在するとがん化を誘導。変異したAPCタンパク質はSam68と結合はできるものの、その複合体はTCFのスプライシングを制御できなくなってしまうため、TCFのスプライスバリアントが増えることでWnt標的遺伝子が強く活性化され、細胞ががん化するというもので、研究グループは、こうして変異したAPCタンパク質がどのようにがんの発症を導くのか、その分子メカニズムの解明につながるAPCタンパク質とSam68の複合体の立体構造の解明を今回行った。
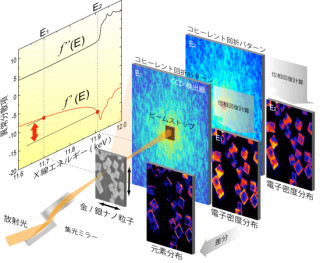
一般的に、APCタンパク質を含むヒト由来の大きなタンパク質を、高い品質で効率良く調製することは難しいが、理研生命分子システム基盤研究領域では、独自開発した無細胞タンパク質合成系をはじめ、数々の技術を基に高難度タンパク質に対応した試料調製システムの開発を進めており、今回はこれらのシステムをヒトAPCとSam68タンパク質の発現に応用することで、100通り以上のアミノ酸領域についての試行を行った。その結果、APCとSam68タンパク質のそれぞれについて、効率よく試料が得られる領域を見いだしたほか、この方法を用いてX線結晶構造解析に適した高品質なタンパク質を大量に精製し、SPring-8およびSwiss Light SourceでX線回折データを取得し、APCのArmドメインの構造を2.1Åの分解能で、Sam68のチロシンリッチドメインとの複合体の構造を2.4Åの分解能でそれぞれ決定することに成功した。
さらに立体構造を詳細に分析した結果、APCタンパク質の516番目のリジン残基(Lys516)が特にSam68との複合体を作るのに重要であることが判明したほか、等温滴定カロリメトリ(isothermal titration calorimetry:ITC)を用いた研究により、実際にこの箇所に変異を入れると、APCタンパク質とSam68との間の結合能が落ちることを確認した。
加えて、Sam68のチロシン残基(Tyr387)がリン酸化されるとAPCタンパク質との結合能が失われることも見いだされた。大腸がん患者のAPCタンパク質では、Lys516の部分がアスパラギン残基(Asn)に変異している事例があることから、この箇所が変異した複合体はWnt標的遺伝子を強く活性化し、細胞のがん化を導くと考えられ、変異APCタンパク質と細胞のがん化との関連性を立体構造の観点からも明らかにできたという。
今回の成果は、変異したAPCタンパク質によるがん発症の分子メカニズムの解明に対する知見を与えるもので、大腸がんに対する新しい治療戦略にもつながるものと期待される。なお、研究グループでは現在、がん進行におけるAPCの役割についてさらに深く理解するために、Sam68以外の結合タンパク質とAPCとの複合体の構造解析を目指して研究を進めており、こうして決定された立体構造や今後の構造解析による知見が、正常なシグナル伝達には影響せずにがん細胞にだけ選択的に作用する薬剤の創製につながるものとの期待を示している。