国立がん研究センター東病院、中外製薬、NTTデータは6月11日、電子カルテに記載された臨床データのEDC(Electronic Data Capture:電子的な臨床データ収集)への連携に関する共同研究を実施したことを発表した。今回の研究ではNTTデータが開発した「PhambieLINQ」を活用し、疾患領域を限定せずに有害事象や併用薬など治験で必要となる主要な臨床データを連携できるようになったという。
各社の役割
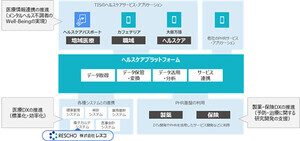
NTTデータはどの医療機関や製薬企業でも電子カルテとEDCのデータ連携を可能とする、治験DX(デジタルトランスフォーメーション)サービス「PhambieLINQR」の開発と提供を進めている。現在同サービスで連携可能な臨床データは、患者背景、臨床検査値、バイタルサインの3種類。
しかし、電子カルテにはその他にも有害事象や併用薬などの情報も記録されていることから、これらの情報がEDCへ電子的に連携可能となれば、治験業務のさらなる効率化が期待できる。
国立がん研究センター東病院は医療DXの加速に向けて、デジタル技術を活用したデータの収集、データ利活用に向けた構造化などの整備、さらには治験業務改革を進めている。中外製薬は「CHUGAI DIGITAL VISION 2030」の基本戦略の一つにバリューチェーンの効率化を掲げ、治験プロセスのさらなる加速を目指す。
中外製薬とPhambieLINQRを利用する国立がん研究センター東病院はNTTデータと共に、有害事象や併用薬を含めて、疾患に関わらず試験共通で必要となる主な臨床データをEDCへ連携する共同研究を実施した。
共同研究の内容
今回の検証では、電子カルテに記録された有害事象や併用薬を含む臨床データについて、症例データ報告やデータ収集の効率化など治験に利活用する際の技術的、および運用上の課題解決を目指す。
具体的には、NTTデータのPhambieLINQを活用して、国立がん研究センター東病院の電子カルテから有害事象と併用薬を含む臨床データを中外製薬のEDCまで電子的に連携できることを確認する。
連携対象となる臨床データは、有害事象、併用薬、患者背景、バイタルサイン、臨床検査値。データ連携による効果を、製薬企業から医療機関へのクエリ(問い合わせ)数、医療機関におけるデータ転記およびSDV(Source Data Verification:倫理的および科学的に治験の適切な実施とデータの信頼性を検証する作業)作業の時間によって評価した。
検証結果
共同での検証の結果、電子カルテからEDCへの電子的な連携は一定程度可能であり、オペレーションおよびデータ品質を含む信頼性の観点から、実際の治験においても利用可能性があることを確認できた。
医療機関の転記作業時間においては、1例あたり1時間程度の削減効果を確認。また、製薬企業のSDV作業時間について、1例あたり1.5時間程度の削減効果を確認した。さらには、医療機関のEDC入力にかかる心理的負荷の軽減への貢献についても確認できたとのことだ。
実証の背景
新薬開発は、研究や治験での臨床データの収集と解析、有効性や安全性の評価といったプロセスを経て開発され、平均で9~17年程度かかるとされる。多くの労力と時間が費やされる臨床データの収集においては、業務効率化と品質確保の両面が課題となる。
近年では医療機関の電子カルテから製薬企業のEDCに臨床データを電子的に連携させる取り組みも進められるが、電子カルテとEDCの互換性や製品間の差異のため、業界全体での普及はなかなか進まない。特に、患者の安全性評価で重要となる有害事象や併用薬情報に関するデータ連携の取り組みは例が少ない。