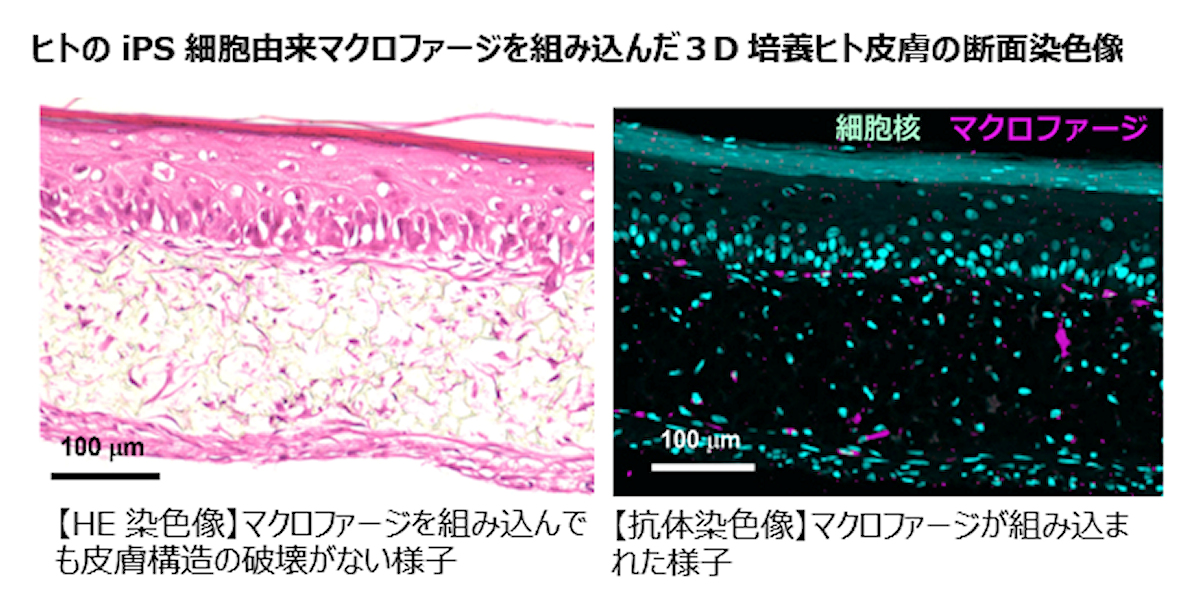
キリンホールディングス(キリン)は9月11日、ヒトのiPS細胞から炎症応答を制御する免疫細胞「マクロファージ」に安定的に分化させる方法を確立してヒトiPS細胞由来のマクロファージを組み込んだ「3D培養ヒト皮膚モデル」を作製し、炎症性刺激を与えた時に3D培養ヒト皮膚モデル内のマクロファージが応答することも確認したと発表した。
同成果は、キリン中央研究所、ファンケル、順天堂大学大学院 医学研究科・環境医学研究所との共同研究講座「抗老化皮膚医学研究講座」によるもの(同講座はファンケルと順天堂大が2018年6月から開始し、キリン中央研究所は2021年6月に参画した)。詳細は、9月4~7日にポルトガルで開催された第53回欧州研究皮膚科学会で口頭発表された。
病原体や毒物などの侵入を防ぐなど、皮膚はさまざまな外部刺激から人体を守る防御器官であるが、皮膚も日常のさまざまな外的・内的ストレスを受けることでダメージを受け続けると慢性的な炎症状態となり、立体構造が壊れ、外部刺激から防御する皮膚のバリア機能が低下するなどの現象が起きてしまう。その結果、乾燥肌やかゆみなどのさまざまな皮膚トラブルが発生し、特に、老化やアレルギーなど、昨今増えている皮膚トラブルには炎症状態が深く関わっているとする。
炎症により皮膚の立体構造が壊れ、皮膚本来の機能が失われるメカニズムを解明することは、炎症状態を改善し、皮膚トラブルに対処する方法を見出すことにつながる。そのため、立体構造を持つ3D培養ヒト皮膚モデルを使い、炎症状態を再現することが皮膚科学研究業界において強く求められていたという。しかし、炎症応答を制御するマクロファージを3Dヒト皮膚モデルに組み込むことは技術的に難しく、これまでのところは、炎症状態の評価は実際のヒトの皮膚と比較して再現できる組織構造や機能が限定的である、平面的な2Dヒト皮膚モデルなどで行われていた。
そうした中、長年にわたる免疫機能の研究実績を活用し、「抗老化皮膚医学研究講座」の中で、ヒトの皮膚の炎症応答を評価・制御できる手法の開発を進めてきたのがキリンだ。今回の共同研究では、3D培養ヒト皮膚モデルの構造を壊すことなくマクロファージを組み込む方法の開発に挑むことにしたという。
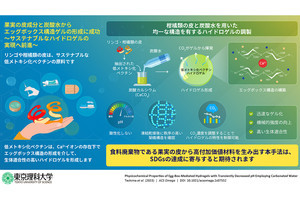
まず、ヒトのiPS細胞を使ったマクロファージの安定的な分化誘導方法が確立された。ヒトiPS細胞を大量に増殖させて多数のストックを作製することで、同一のロットから分化誘導した均一な性質を持つマクロファージが作製された。
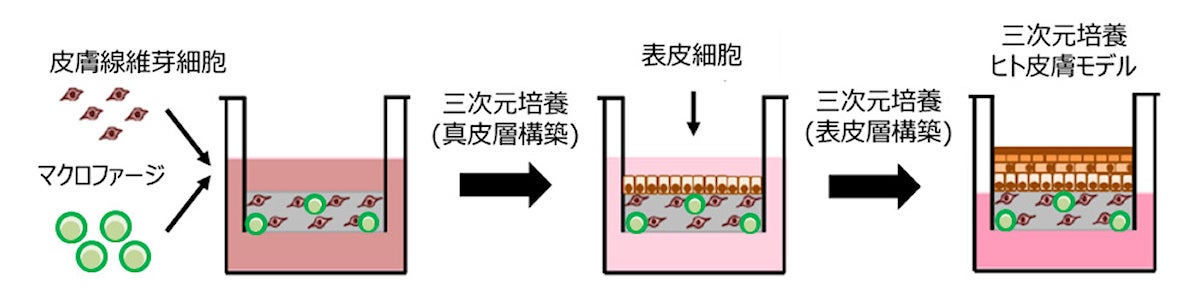
次に、分化させたマクロファージをヒト皮膚線維芽細胞と混合して3D培養を行い、真皮層を構築。真皮層上にヒト表皮ケラチノサイトを播種して、さらに3D培養を行い、マクロファージを組み込んだ真皮層、表皮層から構成される3D培養ヒト皮膚モデルが実現された。
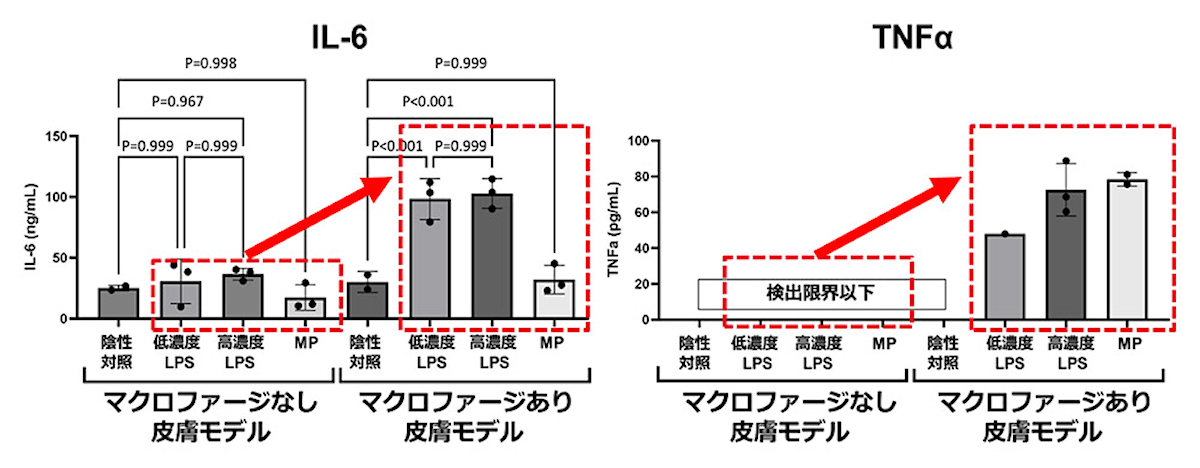
マクロファージを組み込んだ皮膚モデルが炎症性刺激に応答するか検証するため、2種類の刺激剤(Lipopolysaccharide(LPS)およびMethylparaben(MP))が添加され、炎症応答の指標である「炎症性サイトカイン」類(「インターロイキン-6」や「TNFα」など)の放出量を測定。
すると、マクロファージが組み込まれていない3D培養ヒト皮膚モデルと比較して、マクロファージが組み込まれた皮膚モデルでは、LPSまたはMPの添加24時間後の培養上清中に炎症性サイトカイン類の放出がIL-6は約3倍、TNFαは顕著に上昇することが認められたとした。このことから、マクロファージを組み込んだ皮膚モデルが炎症応答を評価できることが確認された。
キリンは今後も免疫機能と皮膚症状の関係性に着目し、3D培養ヒト皮膚モデル作製をはじめとする、さまざまな皮膚研究を進め、皮膚症状のメカニズムの知見を創出することで「肌の健康」の課題解決と共に、ヘルスサイエンス事業の拡大を目指すとしている。