東京大学は2月7日、筑波大学、九州工業大学との共同研究により、ウイルス感染と戦うための「自然免疫」を制御する新たな生体分子を発見してその分子機能を解明、発見した生体分子はタンパク質へ翻訳されない特殊なRNA分子の「長鎖ノンコーディング(nc)RNA」であることが判明したと発表した。
成果は、東大 アイソトープ総合センターの秋光信佳准教授、東大大学院 薬学系研究科大学院生の今村亮俊氏らの共同研究チームによるもの。研究の詳細な内容は、米国東部標準時間2月6日付けで「Molecular Cell」にオンライン掲載された。
20世紀後半から21世紀初頭にかけて行われたヒトゲノムプロジェクトの成果の1つが、それまではジャンク(機能のない無駄なDNA配列)と考えられていたゲノムDNAの配列からも多様な機能未知の転写産物RNAが生み出されていることを明らかにした点だ。
これら機能未知のRNAは、メッセンジャーRNA(mRNA)とは異なってタンパク質のアミノ酸1次配列を指令しないことからncRNAと呼ばれるようになった。発見からおよそ10年が経過するが、この間、世界中で熾烈な研究競争が繰り広げられている。しかしながら、ncRNAの機能の大部分は未だ不明である。
一方、ウイルスなどによって引き起こされる感染症は常に大きな社会問題となっている。インフルエンザウイルスの脅威は例年のことだし、最近でもノロウイルス感染が問題となったことも記憶に新しい。そのため、ヒトの生体防御システムの解明は科学的にも社会的にも大きな意義があるというわけだ。
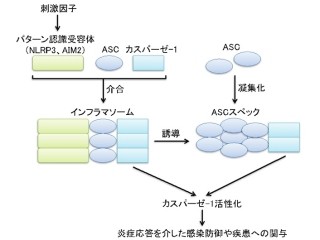
ヒトの免疫は「自然免疫」と「獲得免疫」の2種類から構成されている。自然免疫は免疫の初期段階を担い、獲得免疫は免疫の後期段階を担う。自然免疫はウイルス感染に抵抗するため、「サイトカイン」(細胞間でやり取りされる多様な生理活性を持つタンパク質の1種)と総称されるインターフェロンなどを産生することでウイルスに抵抗している。
よって、自然免疫はヒトの生体防御システムの中でもウイルス感染の最前線といえる。そのため、これまで幅広い研究がなされてきたが、その仕組みの全貌解明には至っていない。その原因の1つが、自然免疫の制御を司る生体分子として、タンパク質以外にどのようなものが存在するかが解明できていない点が挙げられるという。免疫研究のブレークスルーのため、従来のタンパク質以外の生体分子に着目した研究が必要であった。
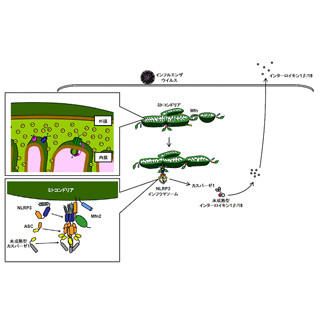
そこで研究チームは今回、最新の「分子生物学的手法」、「分子イメージング技術」、「バイオインフォマティックス」を縦横に駆使して、ncRNAの1種「NEAT1」が自然免疫に必須なサイトカインの発現を制御する分子スイッチとなっていることを発見し、詳細な分子機構を明らかにした。
具体的には、まずウイルスに感染するとそれが刺激となって、NEAT1が誘導されることを解明。次に、誘導されたNEAT1が転写を抑制する働きを持つタンパク質「SFPQ」を吸着して、その働きを阻害することが示された。転写を抑制するSFPQの働きが阻害された結果、サイトカインを指令するmRNAの転写反応が促進され、それに引き続いてサイトカインの大量生産が引き起こされ、結果的に自然免疫活性が高まることが見出されたのである。
今回の成果は、ヒトゲノムの謎に光を当てる発見であると同時に、免疫応答の仕組みの解明に多大な貢献をもたらすものであるという。さらに、今回明らかになったサイトカインの発現を制御する仕組みは、抗インフルエンザ薬などの新たな抗ウイルス薬の開発を加速する成果でもあり、社会的意義と医薬品産業への波及効果が高いとした。
研究チームは今後、自然免疫に関わるncRNAを網羅的に探索し、免疫を調節する仕組みの解明を目指す計画だ。そして、ウイルス感染防御のみならず、花粉症などアレルギーやリウマチなどの自己免疫疾患の起きる分子機構を解明し、治療法開発や治療薬開発に貢献するとしている。