千葉大学と高輝度光科学研究センター(JASRI)の両者は3月22日、これまで考慮されてこなかった電解液中のイオンが白金(プラチナ)電極表面の粗面化や溶出に影響を及ぼすことを明らかにしたと共同で発表した。
同成果は、千葉大大学院融合理工学府の久米田友明大学院生(現・物質・材料研究機構所属)、同・大学大学院工学研究院の中村将志教授、同・星永宏教授、JASRIの坂田修身常務理事らの共同研究チームによるもの。詳細は、米国化学会が刊行する機関学術誌「Journalofthe American Chemical Society」に掲載された。
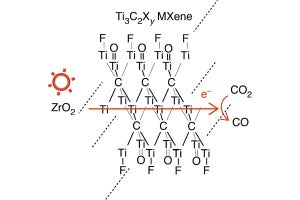
白金は耐腐食性があり、電気化学反応に高い活性を示すことから、腐食性の強い電解質を用いた電気化学デバイスの電極材料に用いられている。燃料電池においても電極として利用されているが、燃料電池の起動・停止を繰り返していくと、白金の溶出や凝集が起こり、発電性能が徐々に低下していくことが課題となっている。
現在のところ、溶出する理由は次のように考えられている。燃料電池の起動・停止により、電極触媒である白金の電極電位が変動する結果、(1)白金の電極電位が正電位になると水(アルカリ中では水酸化物イオン)と反応し、白金表面に水酸基や酸素原子が吸着。(2)白金原子と吸着酸素の原子位置が変わる「原子位置交換」現象が発生。(3)その結果、原子位置を交換した白金が、電極電位を負電位側に還元し容易に溶出する、というものである。
これまでの燃料電池触媒の研究では、酸化されにくい電極触媒を用いたり、酸素源である水が反応しにくいように疎水性物質を触媒表面に吸着させたりする取り組みにより、耐久性の向上が目指されていた。しかし今後は、さらなる活性化や耐久性の向上に向けて、異なるアプローチが求められているとする。そこで研究チームは今回、白金表面から少し離れた場所にあるイオンに着目することにしたという。
水溶液中においてイオンは水和されているが、水との親和性はイオンの種類によって大きく異なる。アルカリ金属イオンの場合、イオン半径の小さなリチウムイオンは、水との親和性が強く親水性となるが、カリウムイオンやセシウムイオンは親水性が弱くなる。水との親和性の弱いアルキル基を持つアルキルアンモニウムイオンは強い疎水性となる。このような親水性や疎水性に着目し、さまざまなイオンを電解質に用いて、大型放射光施設SPring-8や放射光実験施設フォトンファクトリーでの表面X線回折法により白金表面の構造が決定された。
-

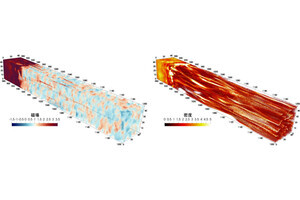
水酸化カリウム(KOH:寒色の波線)溶液中では、白金原子の溶出や原子位置交換による粗面化のため、不可逆的に回折強度が減少する。水酸化テトラメチルアンモニウム(TMAOH:暖色の波線)溶液中では回折強度は変化せず、表面が平滑であることが示されている(出所:千葉大プレスリリースPDF)
これまでの研究から親水性イオンは白金表面の水酸基と強く相互作用するため、表面構造を安定化しやすいと考えられていたという。しかし、疎水性であるテトラメチルアンモニウムイオンを用いても、高電位側において白金の表面が平滑であり原子位置交換が起こりにくいことがわかり、研究チームは予想と反する結果だったとした。
一方、水との親和性が中程度のカリウムイオンでは、原子位置交換がより低電位から起こり、白金の電極電位が変動することによって粗面化したため、原子位置交換の起こりやすさは、陽イオンの親水性と密接に関係していることが判明。アルキルアンモニウムイオンは、平滑な白金電極の燃料電池反応を活性化する効果もあることから、活性と耐久性の両立が可能となるとした。
さらに、振動分光により吸着酸素と吸着水酸基の観測を行ったところ、原子位置交換の起こりやすさには、吸着水酸基と吸着酸素が関与していることが明らかにされた。カリウムイオンのような、中程度の親水性陽イオンは、吸着水酸基と相互作用する。同時に吸着酸素も存在するが、どちらも負の電荷を帯びているため互いに反発する。この負電荷同士の反発力を低減するため、白金原子が表面から持ち上げられることが原子位置交換を促進するという。白金表面の酸化過程は複数の酸化状態を取るために複雑な構造となるが、今回、最先端の分析手法などを用いたことで、詳細な構造や酸化メカニズムの解明につながったとした。
今回の研究により明らかにされた疎水性イオンによる粗面化の抑制は、高い触媒活性の維持につながることが考えられるという。今回の成果は、活性と耐久性を両立した電極触媒の開発につながるとしている。