京都大学(京大)は2月15日、遺伝性ニューロパチーの病態を細胞レベルで再現し、そのメカニズムの一端を明らかにすることに成功したと発表した。
同成果は、徳島大学大学院医科学教育部の大学院生 村上永尚氏、京都大学iPS細胞研究所 井上治久教授らの研究グループによるもので、2月15日付けの英国科学誌「Molecular Brain」に掲載された。
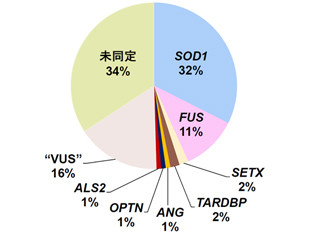
近位筋優位遺伝性運動感覚ニューロパチー(HMSN-P)は、1997年に日本において世界で初めて報告された遺伝性ニューロパチーのひとつで、家族性に運動神経と感覚神経が障害される病気。この原因として、これまでにTFG遺伝子の異常が同定されており、HMSN-P患者では、脊髄運動神経細胞にTFGタンパク質が蓄積し、運動神経細胞の変性・脱落をきたすことがわかっているが、その詳細なメカニズムについては明らかになっていない。
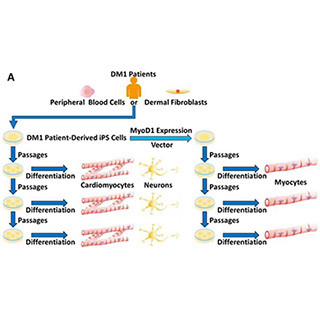
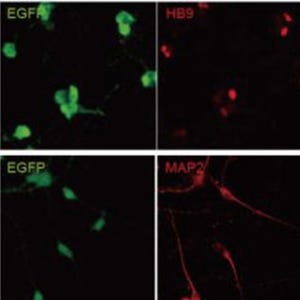
そこで同研究グループは、2人のHMSN-P患者および3人の健常者からiPS細胞を作製し、神経細胞へと分化させた。この結果、神経細胞への分化のしやすさに差はなかったものの、患者のiPS細胞由来神経細胞では、TFGタンパク質が蓄積し、また不要なタンパク質を分解する仕組みのひとつであるユビキチン・プロテアソーム系(UPS)の機能が低下。UPSの働きを低下させる試薬を加えたところ、HMSN-P患者由来iPS細胞から作製した神経細胞では細胞死を引き起こしやすいことがわかった。
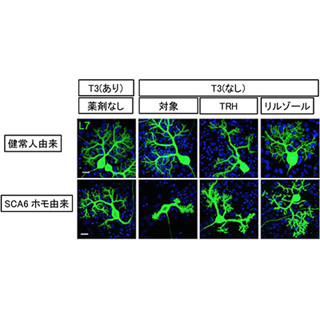
さらに同研究グループは、CRISPR-Cas9システムと呼ばれるゲノム編集技術を用いて、患者由来iPS細胞のTFG遺伝子変異の修復を行った。この結果、TFGタンパク質の凝集が消失したほか、UPSの働きが改善し、UPSの働きを抑える試薬による細胞死の引き起こしやすさも改善したという。
今回の成果について、同研究グループは、HMSN-Pをはじめとした運動神経が障害される病気の研究や治療薬の探索に貢献するものと説明している。