理化学研究所(理研)と東京工業大学(東工大)の両者は5月24日、がん細胞に多く存在する反応性の高い化合物「アクロレイン」を利用し、「シアル酸転移酵素」(タンパク質の表面に存在する糖の1つであるシアル酸の合成に関与する酵素)の阻害剤をマウス体内のがん細胞内で合成し、がん細胞表面上の糖鎖構造を変えて、副作用なくがんを治療することに成功したと共同で発表した。
同成果は、理研 開拓研究本部 田中生体機能合成化学研究室の田中克典主任研究員(東工大 物質理工学院 応用化学系 教授兼任)、同・チャン ツンチェ研究員(東工大 物質理工学院 応用化学系 特任助教兼任(研究当時))、同・アンバラ プラディプタ客員研究員(東工大 物質理工学院 応用化学系 助教兼任)、同・笠原隆継研修生(研究当時、東工大 物質理工学院 応用化学系 大学院生(研究当時))、同・吉岡広大基礎科学特別研究員らの研究チームによるもの。詳細は、英国王立化学会の機関学術誌「Chemical Science」に掲載された。
がん細胞表面上の糖鎖にある過剰なシアル酸は、生体内の免疫細胞によるがん細胞の排除を妨害する厄介な存在だ。これはがんの浸潤や転移につながるため、糖鎖上のシアル酸を減らし、糖鎖構造を変えることのできるシアル酸転移酵素阻害剤が新たながん治療戦略になる可能性があるとされている。しかし、シアル酸を有する糖鎖は正常な細胞にも存在し、多様な生体機能の調整に関わることから、正常な細胞のシアル酸を減らしてしまう既存のシアル酸転移酵素阻害剤は、重篤な副作用を生じてしまうことが課題だった。特に、腎臓の機能障害は大きな問題となっているという。
そうした中で研究チームの田中主任研究員らはこれまでの研究で、がん細胞にアクロレインが過剰に生成されることを発見していた。また、同化合物と反応する保護基を開発し、がん細胞内のみで薬剤を合成する戦略も報告済みだ。そこで今回の研究では、シアル酸転移酵素阻害剤をがん細胞内でのみ合成し、がん細胞上の糖鎖構造のみを合成化学的に変換することができれば、副作用のない治療法になると考察し、その実現を目指したという。
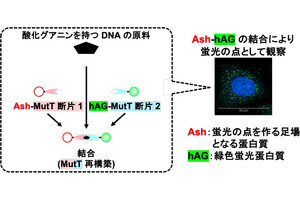
研究チームはまず、以前開発した、細胞内でアクロレインと効率的に反応する保護基(反応性の高い官能基に導入し、その反応性を下げる官能基)をシアル酸転移酵素阻害剤(ドラッグ)に導入し、「プロドラッグ」に変換したとのこと。プロドラッグとは、生体内の薬剤標的部位での化学反応によって、薬効を示す分子に変換されるようにデザインされた薬剤のことであり、今回の場合は、がん細胞に取り込まれると、がん細胞が産生するアクロレインと環化付加反応を起こし、保護基の部分のみが切断されドラッグへと変換される。このプロドラッグはがん細胞(標的部位)で選択的に活性を示すため、副作用の軽減が期待できることが大きな特徴だ。
そして、今回のプロドラッグの作用機序を確認すべく、マウスのがん治療を通じて検証が行われた。その結果、マウス体内ではプロドラッグによる腫瘍成長の抑制効果が見られ、がん細胞内では確かにドラッグが合成されていることが確かめられたという。
その一方で、腎臓の障害による体重増減の副作用は確認されず、正常な腎臓組織上ではドラッグが合成されていないことが示唆されたとのこと。実際に、がん治療後のマウス体内の腎臓組織ではドラッグによってシアル酸が減少しているが、プロドラッグではシアル酸が減少していないことが明らかにされた。このことから、正常な腎臓組織ではドラッグの合成が起きていないことが強く支持され、副作用の回避につながっていることが示されたとする。
-

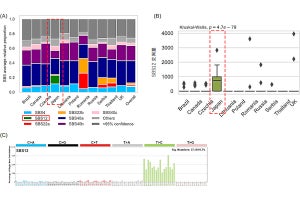
(A)動物実験の概要(上、実験期間16日)。マウスにおける未処理群、ドラッグ投与群、プロドラッグ投与群の腫瘍体積変化(左下)と体重変化(右下)。ドラッグやプロドラッグは腫瘍の成長を抑える。ドラッグは体重増減の副作用があるが、プロドラッグにはその副作用がない。(B)標準的な色素を用いたヘマトキシリン・エオジン染色による細胞の検出(上段)とシアル酸含有糖鎖の検出(下段)。シアル酸含有糖鎖は緑色の蛍光として検出される。ドラッグは腎臓組織のシアル酸を減少させるが(下段中)、プロドラッグは腎臓組織のシアル酸を減少させない(下段右)(出所:理研Webサイト)
今回の研究ではこのように、シアル酸転移酵素阻害剤をプロドラッグ化することで、がん細胞内のみでドラッグを合成し、がん細胞の糖鎖構造のみを合成化学的に変換するという、副作用のないがんの治療戦略を実証することが達成された。研究チームは、がん細胞内で薬剤を合成するという今回の研究戦略は、他の作用機序を有する抗がん剤の開発においても、副作用を減らす戦略としての活用が期待されるとしている。