京都大学(京大)は7月17日、物質透過性を持つ糖鎖高分子ベシクルを新たに開発し、がん組織周囲でプロドラッグを抗がん剤へと変換できる酵素封入型ナノデバイスとして機能することを見いだしたと発表した。
同成果は、京都大学大学院工学研究科 西村智貴特定研究員、秋吉一成教授らの研究グループによるもので、7月17日付けの独科学誌「Advanced Materials」オンライン版に掲載された。
リン脂質からなるリポソームや両親媒性ポリマーからなるベシクルは、酵素反応場としての応用が進められているが、極めて物質透過能が低いことが知られている。そのため、酵素基質を外部から供給できず、長期的に酵素反応を進行させることができないことが課題であった。
今回、同研究グループは、オリゴ糖とポリプロピレングリコールからなる両親媒性ポリマーを設計。同ポリマーが水溶液中で自発的に集合し、糖鎖高分子ベシクルを形成することを明らかにした。
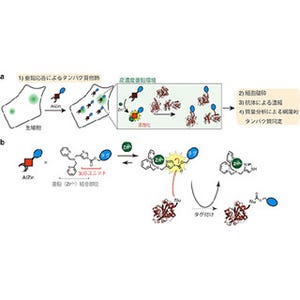
同糖鎖高分子ベシクルは、分子量の大きなタンパク質・酵素などを溶媒で満たされた内部空間(内水相)に保つことができ、低分子量の化合物は2分子膜を透過する「物質透過性」を持つ。実際に、モデル酵素であるβ-ガラクトシダーゼをベシクルに内包させ、加水分解されると蛍光を示す基質を外部から添加すると、基質が2分子膜を透過し、内水相にあるβ-ガラクトシダーゼによって加水分解を受け、蛍光を示すことがわかっている。
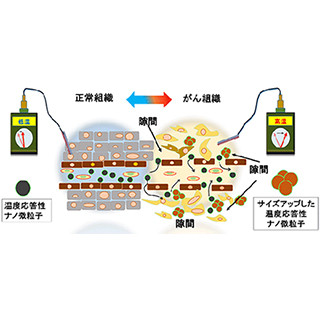
さらに、同糖鎖高分子ベシクルは、血中投与により生体内のがん組織周囲に集まり、プロドラッグを抗がん剤へと変換し、優れた抗腫瘍効果を示すことがマウスで実証されている。体重減少や臓器毒性などの副作用は検出されていない。
このことから同研究グループは、同糖鎖高分子ベシクルについて、薬物をがん組織周囲で合成、放出し得る酵素搭載型新規治療用ナノファクトリーとして機能するものと説明している。ナノファクトリーによる治療の概念は、2007年に他の研究グループから提案されていたが、実際にナノファクトリーとして機能する材料の報告はこれまでなかったという。