理化学研究所(理研)は4月18日、記憶や学習などの脳機能に必要なカルシウムチャネルであるイノシトール三リン酸受容体(IP3受容体)の動作原理を解明したと発表した。
同成果は、理研脳科学総合研究センター発生神経生物研究チーム 濱田耕造研究員、御子柴克彦チームリーダーらの研究グループによるもので、4月17日付の米国科学誌「Proceedings of the National Academy of Sciences of the United States of America(PNAS)」オンライン版に掲載された。
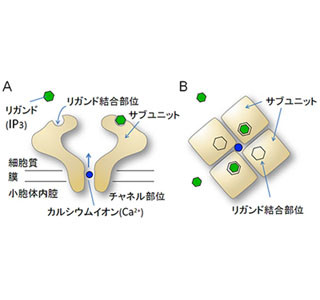
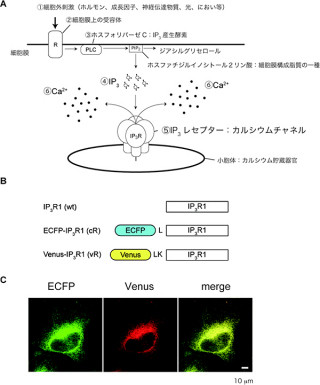
IP3受容体は小胞体の膜上に局在するタンパク質。個体の発生や神経のシナプス可塑性を担っており、4つ組み合わさることで中心部にカルシウムイオン(Ca2+)をひとつだけ通す小さなイオン透過口を形成し、カルシウムチャネルとして働く。しかし、IP3受容体のIP3結合部位はチャネル部位から大きく離れているため、リガンドのIP3が物理的にどのようにチャネルを開けるのか不明であった。
今回、同研究グループは、遺伝子工学を用いてIP3結合部位からチャネル部位につながるタンパク質ドメインを昆虫細胞で大量に発現・精製し、2200個を超えるアミノ酸残基からなるIP3受容体細胞質ドメインの巨大タンパク質結晶の作製に成功。同結晶の立体構造をX線結晶構造解析によって決定した。
また、IP3存在下・非存在下と欠失変異体の結晶構造を決定し、IP3が結合して生じる構造変化の経路を見出した。さらに、遺伝子操作でこの経路に変異を入れ機能解析を行い、IP3結合部位からチャネル部位までの経路を決定した。この結果、その経路中でユニークな小葉型構造がチャネルを開く伝達部位となることがわかった。
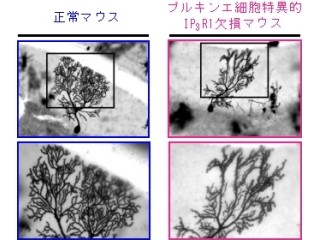
IP3受容体タンパク質に異常があると脳の形態やシナプス可塑性に異変が起き、IP3受容体の遺伝子に変異が起きると神経疾患を発症するほか、認知症にも関わることが知られているため、今回の明らかになった動作原理は今後、神経疾患や認知症の治療・予防に役立つ新しい創薬ターゲットとして役立つことが期待される。