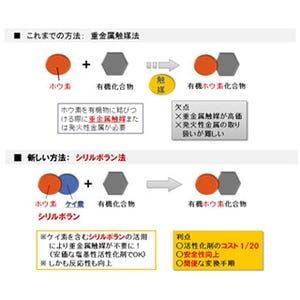
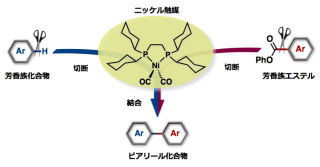
名古屋大学(名大)は7月22日、環境への負荷が小さい上に、これまで不可能だった芳香族分子とアルケン分子の組み合わせを使うことが可能な改良型「溝呂木-ヘック型カップリング反応」を、安価で空気中で安定して使えるニッケル触媒を用いて実現したと発表し、商品化も実現して8月末には発売を開始することを発表した。
成果は、名大 トランスフォーマティブ生命分子研究所の・山口潤一郎准教授、モン・リンクイ氏(中国武漢大学・留学生)、名大学部生の鎌田祐子氏、同・博士課程学生の武藤慶氏、同・伊丹健一郎教授らの研究チームによるもの。研究の詳細な内容は、7月20日付けで独化学専門誌「Angewando Chermie International Edition」のオンライン版に掲載された。
溝呂木-ヘック型カップリング反応とは、故・溝呂木勉教授(東京工業大学)と、2010年に鈴木章教授(北海道大学)と根岸英一教授(米パデュー大学)と共にノーベル化学賞を受賞したリチャード・ヘック教授(米デラウェア大学)が、同時期にそれぞれ独自に開発した、化学合成の中心的な触媒反応である。パラジウム触媒を用いて芳香族分子とアルケン分子を連結させることが可能な、現在では医薬品や有機エレクトロニクス分子を合成する強力な技術だ(画像1)。
従来、同反応には触媒にパラジウム触媒、芳香族分子に芳香族ハロゲン化物、アルケン分子に「オレフィン」が使われている。芳香族とアルケン分子をつなげるためには目印が必要であり、芳香族分子にはハロゲンが、アルケン分子には水素が用いられている仕組みだ。近年、芳香族分子とアルケン分子の目印を変えた新しいカップリング反応も開発されているが、それらは環境に悪影響が懸念される金属化合物やハロゲン化物などを排出する点や、高価なパラジウムやロジウムを触媒として用いる必要があるなどの問題点があった。
研究チームによって今回開発された反応は、独自開発のニッケル系の「Ni-dcype(ニッケル-1,2-ビスジシクロヘキシルホスフィノエタン)触媒」を用いることで、芳香族分子として「ヘテロ芳香族化合物」を、アルケン分子として「エノール誘導体」もしくは「不飽和エステル」をカップリング基質とすることを可能としている点が特徴だ(画像2)。特に、エノール誘導体や不飽和エステルが反応する点は、これまでにない大きな進展だという。
このNi-dcype触媒を使うと、リン酸三カリウムの存在下でヘテロ芳香族化合物とエノール誘導体もしくは不飽和エステルが反応し、対応するカップリング生成物が良好な化学収率で得られる仕組みだ。カップリングによって生成される共生成物は「カルボン酸誘導体」や「フェノール誘導体」であり、これらは環境への負荷が極めて小さい物質である点が優れている。なお、この反応の進行にはNi-dcype触媒が必須で、ほかの触媒を使っても反応はまったく進行しないという。
今回のカップリング反応を使えば、生物活性分子、医農薬、複雑有機天然物、有機色素、有機エレクトロニクス材料など、さまざまな芳香族-アルケン連結分子の効率的な化学合成が可能となる(画像はそれが期待される分子の例)。実際に今回のカップリングを駆使することで、生物活性天然物「シホナゾホールB」(画像3)の迅速合成ルートが確立された。従来の手法では7工程かかった中間体の合成を4工程で達成することに成功したのである。今回はレアメタルではなく、独自に開発されたニッケル触媒「Ni-dcype」を用いるという点で従来のカップリングに比べて実用的だ。
今回のカップリング反応の特徴としては、3つほどが挙げられる。1つ目は、環境に悪影響が懸念される金属化合物やハロゲン化物などを共生成物として排出しないということ(環境への負荷が小さい)。2つ目は、これまで不可能だった芳香族分子とアルケン分子の組み合わせを使うことが可能なこと。3つ目は、高価なパラジウムやロジウムではなく、安価なニッケルを触媒としてで安定的に用いることができる点だ。よって、従来のクロスカップリングに比べて実用的だとしている。
現在、世界中でポスト・クロスカップリングの開発研究が進められており、独自の触媒を開発して駆使することで、今までは不可能だった合成化学が可能となりつつある。有機分子を自由自在かつ迅速に合成することができれば、動植物のシステムバイオロジー、医薬品、有機材料など、今後の発展が注目される分野のパラダイムシフトを起こす起爆剤になると考えられ、新規触媒開発への挑戦はますます注目されてことになるだろうとした。