理化学研究所(理研)は、名古屋大学、東京都健康長寿医療センター、福祉村病院長寿医学研究所との共同研究により、全身の筋肉マヒを引き起こす運動神経変性疾患の1つ「筋萎縮性側索硬化症(ALS)」の運動神経細胞の中に、小児期に発症する運動神経変性疾患「脊髄性筋萎縮症(SMA)」と類似した異常を発見し、2つの疾患に共通する神経細胞変性のメカニズムの一端を解明したと発表した。
成果は、理研 脳科学総合研究センター 運動ニューロン変性研究チームの山中宏二チームリーダー、同・築地仁美研究員らの共同研究グループによるもの。研究の詳細な内容は、欧州の医学専門誌「EMBO Molecular Medicine」2月号に掲載されるのに先立ち、日本時間1月25日付けでオンライン版に掲載された。
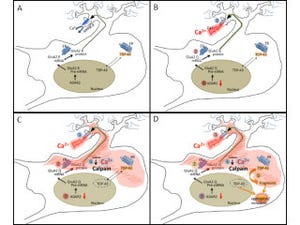
ALSは、全身の筋肉を支配する運動神経細胞に障害が起き、呼吸筋を含む全身の筋肉がマヒする運動神経変性疾患だ。50代から60代での発症例が多く、進行が早い原因不明の難病である。
有効な治療法は現時点では見つかっておらず、日本では約8500人のALS患者が闘病しているという推定だ(出典:難病情報センター)。患者の苦痛に加え、長期にわたって負担が大きい介護を必要とするため、その原因の解明と治療法の開発が社会的に強く求められている。
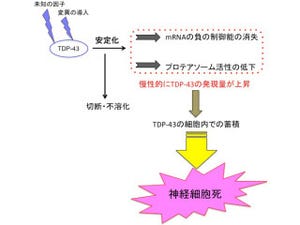
ALSの約90%は非遺伝性だ。そして、ほぼすべての非遺伝性ALSの病巣にRNA結合タンパク質「TDP-43」が運動神経細胞の細胞質内に異常に凝集し蓄積していることがわかっている。
さらに、過去の研究から遺伝性ALSの一部にTDP-43や「FUS遺伝子」の変異が見つかっていることから、TDP-43やFUSタンパク質の異常がALSの発症に直結する原因であると考えられるようになってきた。
TDP-43とFUSタンパク質の働きは、スプライシングやメッセンジャーRNA安定性の制御など、さまざまなRNA代謝の制御に関わることが知られている。RNA代謝の制御は、DNAからタンパク質が合成される転写や翻訳などのプロセスに重要な役割を持ち、生物が正常に生命維持活動を行うために欠かせない機構の1つだ。しかし、この2つのタンパク質の異常がどのようなメカニズムで運動神経細胞の変性を引き起こすのかは依然として不明のままである。
一方、SMAはALS同様に脊髄の運動神経細胞の病変によって全身の筋肉マヒが起こる運動神経変性疾患で、小児期から発症する遺伝性の進行性神経難病だ。過去の研究から、タンパク質「SMN」の減少によりSMAを発症することが知られていた。
SMNタンパク質は、スプライシング反応を担うタンパク質「snRNPs」とRNAの構造体の形成に必須なので、snRNPsの減少がSMA発症の要因と考えられる。ALSもSMAと同様なRNA代謝の異常が予想されるが、ALSではどのようなRNA代謝異常があるのか、またALSでどのメカニズムの破たんが運動神経細胞を死滅させるのかは不明だった。
そこで共同研究グループは、TDP-43やFUSタンパク質の異常とRNA代謝の関連性を突き止め、運動神経変性メカニズムの解明に挑んだ次第だ。
まず、正常な状態でのTDP-43、FUSとSMNの動態を確認するため、ヒトとマウスの正常な培養細胞内でこれらの局在が詳細に調べられた。すると、TDP-43、FUS、SMNは一緒に核内に存在し、構造体「Gem」に共に局在していることが見出された(画像1)。
さらに生化学実験によってTDP-43タンパク質のカルボキシル末領域がGemへ局在するのに必要であることが判明し、その領域はSMNとの結合に必要であることも明らかになった(画像2~4)さらに、この3つのタンパク質は互いに結合して複合体を形成していることもわかった(画像5)。

|

|
|
画像4(左):TDP-43タンパク質のカルボキシル末領域がSMNとの結合に必要だ。画像5:SMA疾患変異体(W92S、G95R、E134K)では3タンパク質からなる複合体形成が減ることがわかり、SMN、TDP-43、FUSタンパク質が複合体を形成する際の重要部位の同定に成功した |
|
次に、ALS患者と非ALS患者の脊髄組織を用いてTDP-43タンパク質とGemを免疫染色したところ、非ALS患者の脊髄にある正常な運動神経細胞では核内にGemが観察され、TDP-43タンパク質はGemに局在することが判明。しかし、ALS患者の変性した運動神経細胞では、TDP-43は細胞質に異常に凝集し、Gemが形成されていなかったのである(画像6)。

|
|
画像6。1つの細胞当たりのGem数。ALS患者の脊髄運動神経細胞Gemが減少している。非ALS患者の脊髄運動神経細胞ではGemが1つの細胞あたりに2個程度存在するが、ALS患者ではGemの数が極端に減っている |
また、ALS患者の脊髄の運動神経細胞では、snRNPsの量が異常に上昇し核内に凝集していることもわかった(画像7~9)。
snRNPsのRNA構成成分である「snRNAs」の染色法による解析によっても核内にsnRNAsの異常蓄積が認められ(画像10・11)、かつ脊髄組織中のRNA量を定量するとALS患者組織でsnRNAs発現量の上昇が確認された(画像12)。

|
|
画像12。各種(U1~U6atac)のsnRNAs量をRT-PCR法で測定し、その平均値をプロットするとALS患者におけるsnRNAs量が、統計学的に有意に増加していることがわかる。*:p<0.05、**:p<0.01(Student'st検定、p値=偶然にそのようなことが生じる確率) |
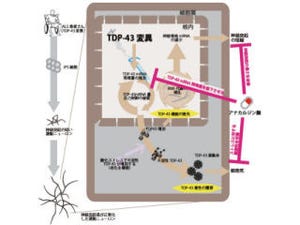
通常、核内でDNAから転写されたsnRNAsは細胞質へ運ばれ、SMNによりsnRNPsが構築され、再び核内のGemへと輸送される。Gemでさらに修飾が起こり、多くのタンパク質が相互作用することでスプライシング反応を起こす「スプライソソーム」まで成熟する。
ALSの変性した運動神経細胞では、snRNPsが核内に異常に増えて凝集し、スプライシング反応の破たんを招いていることが示唆された。snRNPsの減少がもう1つの運動神経変性疾患SMAを起こすことを考え合わせると、運動神経細胞はsnRNPs異常に脆弱であると考えられた(画像13)。
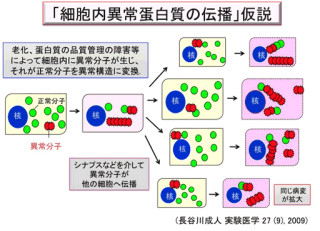
画像13は、概念図。ALSとSMAは共にRNA代謝に関わるタンパク質の異常により運動神経細胞の変性が起こり、その影響で細胞が死滅する疾患である。SMA患者では、その細胞死はスプライソソーム異常により起こることがわかっていた。
今回の研究によりALSでもスプライソソーム異常があることがわかり、運動神経細胞はほかの細胞よりもスプライソソーム異常に脆弱で、スプライソソーム異常がALSとSMAに共通した発症メカニズムではないかと考えられる。
今回の研究により、根本治療法がなく難病とされるALSとSMAに共通した病態メカニズムが初めて突き止められた。今後は、このスプライシング反応の破たんがどのように運動神経細胞死を引き起こしているかを詳細に検証することで、ALSやSMAを含む運動神経変性疾患全体の発症メカニズムの全貌の解明や治療法開発への応用が期待できると、研究グループはコメントしている。