名古屋大学(名大)は、東京大学の協力を得て、片頭痛の治療薬である「ナラトリプタン」がアルツハイマー病などの神経変性疾患に対する新規治療薬であることを見出したと発表した。
成果は、名大大学院 医学系研究科 神経内科学の祖父江元教授、同・勝野雅央特任准教授、同・南山誠研究員(現・国立長寿医療センター研究所室長)らの研究グループによるもの。研究の詳細な内容は、英国時間9月30日付けで英国科学誌「Nature Medicine」オンライン版に掲載された。
神経変性疾患(アルツハイマー病、パーキンソン病、運動ニューロン病など)は特定の神経が徐々に弱っていく進行性の病気で、中高年で発症し徐々に認知や運動などの機能が失われる難病だ。現在のところ病気のメカニズムは十分に解明されておらず、病気の進行を抑える有効な治療法は見出されていない。
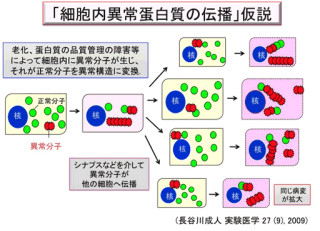
神経変性疾患に共通する病理学的所見として、神経細胞の中や周囲に異常なタンパク質が蓄積することが知られているが、それがどのように神経細胞を変性させる(弱らせる)かについてはよくわかっていない状況である。
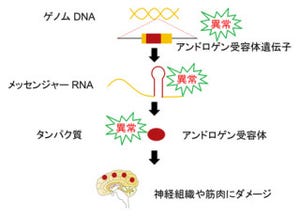
今回、研究グループが対象とした「球脊髄性筋萎縮症(SBMA)」は全身の筋力低下や食べ物の飲み込みにくさを主な症状とする進行性の神経変性疾患だ。「ポリグルタミン」という異常な構造を持った「アンドロゲン受容体タンパク質」が男性ホルモンと結合することによって運動神経中に蓄積し、転写に異常を来すことによって変性を起こすことが知られている。
しかし、変異アンドロゲン受容体タンパク質による転写異常がどのようなメカニズムで神経変性につながるのかは不明だった(画像1)。そこで研究グループは今回、SBMAモデルマウスの脊髄から抽出したメッセンジャーRNA(mRNA)を用いて「マイクロアレイ」解析を実施。
運動障害の発症前からコントロール(野生型)と比較し、SBMAマウスで有意に転写が変化している13の分子を同定し、その内の多機能神経ペプチドである「カルシトニン遺伝子関連ペプチド(CGRP1)」が最も著しく発現変化(量が増加)していることが確認されたのである(画像2)。さらにCGRP1は、SBMAマウスのみならずSBMA患者の運動神経でも発現量が増加しているのが確かめられた。
次に、CGRP1の増加が神経細胞にとって有害であるか否かを調べるため、神経系培養細胞でCGRP1を過剰発現させてみたところ、細胞死が誘導され、CGRP1のノックダウンや薬物学的阻害を行うと変異アンドロゲン受容体の毒性が抑制されることが判明。
その分子機序として、CGRP1が「c-Jun N末端キナーゼ」のリン酸化を介して「JNKシグナル」を活性化すること、および変異アンドロゲン受容体の細胞毒性がJNK阻害剤によって抑制されることも確かめられた。
さらに、SBMAモデルマスとCGRP1ノックアウトマウスを交配して症状の変化を行ったところ、CGRP1の発現抑制によりSBMAマウスの運動神経におけるc-Junのリン酸化が抑制されると共に、運動機能や寿命に有意な改善が認められた。
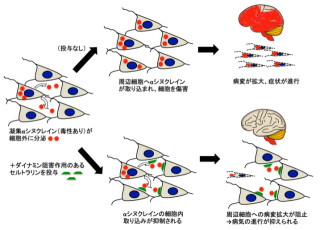
CGRP1をターゲットとした治療法を開発するため、低分子化合物によるCGRP1の発現を抑制する低分子化合物をスクリーニングしたところ、片頭痛の治療薬として使用されているナラトリプタンなどの「セロトニン受容体アゴニスト」がCGRP1の発現量を低下させることが判明。そこで、変異アンドロゲン受容体を過剰発現させた神経系培養細胞にナラトリプタンを投与すると細胞障害が軽減することが示されたのである。
次にナラトリプタンをSBMAモデルマウスに経口投与したところ、運動神経におけるCGRP1の発現量が減少し、JNKシグナルが抑制(正常に制御)され、運動機能や寿命が有意に改善されたのが確認された(画像3)。
以上の検討結果から、ナラトリプタンによるCGRP1-JNK経路の抑制はポリグルタミンに関連した運動神経変性を抑制する治療法となりうると考えられるとしている。
またポリグルタミンはSBMAのみならず、「ハンチントン病」や一部の「脊髄小脳変性症」にも共通する原因であり、今回と同様の手法でポリグルタミンによる転写障害の詳細を解明することにより、病態に深く関連する分子をターゲットとした根本治療法を開発することができると考えられるという。
SBMAについては現在男性ホルモンを押さえる薬剤の臨床試験が行われており、その結果が判明した後にナラトリプタンの臨床試験を行うことを検討する予定であるが、綿密に計画を進める必要があると、研究グループは述べている。