京都大学は6月22日、モデル動物であるニワトリ胚の遺伝子操作を用いて、個体発生過程における交感神経と副腎の形成機構を解明したと発表した。
成果は、京大理学研究科の高橋淑子教授、奈良先端科学技術大学院大学 バイオサイエンス研究科の斎藤大介助教らの共同研究グループによるもの。研究の詳細な内容は、6月22日付けで米学術誌「Science」に掲載された。
多くのストレスにさらされる現代社会において、「恒常性(ホメオスタシス)」の乱れによる「現代病」が急増している。恒常性は自律神経系によって調節される。そして自律神経系の中でも、交感神経と副腎は特に重要な組織だ。
しかし、これらの臓器の機能(の異常)がどのようにして「自律神経失調症」や「ストレスに強い(弱い)体」に結びつくのかはほとんどわかっていない。その理由として、交感神経系の成り立ちの仕組みがまったく解明されていないことが考えられるという。
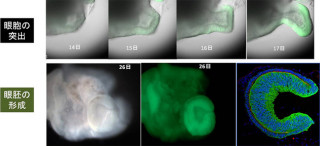
その交感神経系と副腎は、初期発生過程において同じ前駆細胞から作られる。その前駆細胞は「神経堤細胞」と呼ばれるのもので、幹細胞のような未分化状態として出現した後、胚内を長距離にわたり移動する内に徐々に分化する。
交感神経系が作られる場合、神経堤細胞はまず体の中心にある「背側大動脈」(以下、大動脈)に向かって移動する。そして大動脈付近で、さらに副腎になるものが分岐する。高橋教授らは、以下のような解析を通して、大動脈が交感神経系形成のカギを握ることを突き止めた。
まず、トリ胚の利点を活かして、大動脈を胚内の本来とは異なる場所に移植したところ、その場所に向かって神経堤細胞が移動することが確認された。このことは、大動脈が神経堤細胞を誘引することを示す。
さらに詳しく調べたところ、大動脈から分泌される「BMPタンパク質」がその周辺でさまざまな因子の産生を促すこと、そしてこれらの因子こそが細胞誘引を直接的に引き起こすことが判明。これらの細胞誘引因子には、免疫細胞の移動をコントロールするものも含まれるなど、免疫系と神経系の共通性もうかがえた。
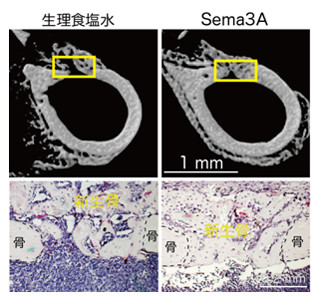
大動脈にたどり着いた神経堤細胞は、やがて交感神経と副腎の2種類へと分岐するが、この分岐にも大動脈から分泌されるBMPタンパク質が働くことが判明。BMPシグナルが働くと、副腎細胞が分化するのだ。このことは、BMPシグナルを人工的にブロック(阻害)すると、交感神経はできるが副腎は作られないという実験結果から示された。
これらの発見は、主にトリ胚の胚操作を用いて得られたものだ。特筆すべきは、同一の胚内で、血管(大動脈)と神経(神経堤細胞)の両方を同時にかつ別々に遺伝子操作するという、世界初の技術が開発されたことである。
神経と血管は、胚発生の過程から成体まで、さまざまな箇所で密接に関わっていることは「経験的」に知られているが、両者の関係性を遺伝子やタンパク質の機能面から明らかにした研究はほとんどなく、今回の発見は大きな成果といえよう。
副腎を除去されるとヒトは死に至る。また、交感神経はその正確な機能はおろか、どこでどのようにして作られるのか、ほとんどわかっていなかった。今回の研究から、交感神経系が作られるためには、液性因子BMPが極めて中心的な役割を持つことが証明された形だ。
なお、iPS細胞から交感神経や副腎を作ったという報告はまだない。今後の細胞工学や細胞治療、そして自律神経失調症の治療に向けて、BMPは注目されるべきタンパク質となるであろう。また、自律神経に関わる血管の作用も今回の研究で明らかになったことから、循環器系の治療と自律神経失調症との関わりも期待されると、高橋教授らはコメントしている。