RNA干渉法を用いた核酸医薬に関する研究開発を進めてきた九州大学(九大)、東京医科大学、ボナックの3者は日本独自の核酸医薬に関する新しい基盤技術を確立するに至り、それを機に眼科領域に特化した、新しい分子標的核酸医薬の開発と臨床応用を本格的に進めるために、2012年3月19日に、産学連携ベンチャー「アクアセラピューティクス」を福岡市に設立したことを共同で発表した。
「RNA干渉」は、特殊なRNA(2本鎖短鎖RNA、siRNA)を介した、メッセンジャーRNA(タンパク質合成で重要な役割を果たす遺伝子:mRNA)の発現を抑制する現象で、広く生命体に備わる生体反応機構として、2006年度のノーベル生理学医学賞の受賞テーマとなった。
RNA干渉医薬は、この生体機構を利用し人工的に2本鎖RNAを導入することで、任意の遺伝子の発現を抑制し、病気の原因となるタンパク質の産生を妨げることで、さまざまな疾患を治療しようとする手法だ。
RNA干渉医薬を含む核酸医薬は、従来の低分子医薬品や抗体医薬などとはまったく異なる作用機序を有することから、これまで治療が困難とされてきた、がん、遺伝性疾患、そのほかインフルエンザやウイルス感染症などへの適用が期待されている。
また、核酸医薬は抗体医薬とは異なり、標的分子の同定から臨床試験開始までに要する期間が格段に短いことがメリットの1つだ。さらには、医薬品(特に原薬)の製造に要する設備は、抗体医薬に比較して単純で小規模であり、設備投資額も含め、安価に製造することが可能な点もメリットとなっている。
つまり、核酸医薬は、低分子医薬品の容易な製造性を持ちつつ、抗体医薬の有効性と安全性を凌駕する可能性を秘めた、次世代の創薬技術として期待されているというわけだ。
しかし、製品として販売されている核酸医薬は世界で1つのみで、多くは臨床開発の難しさに阻まれている。その主な原因は、主要な技術特許が特定の企業により独占されていることで、特に日本国内での医薬品開発は遅々としており、なかなか進んでいない状況だ。
また核酸分子自体の生体内での安定性や、自然免疫応答の亢進による副作用への懸念、さらには、適切な薬物送達技術がハードルとなり、欧米でも医薬品開発は思うように進んでいない。
こうした状況の中、ボナックは、日本独自の核酸医薬に関する新規基盤技術として、上記課題を克服することが可能な1本鎖長鎖RNAである「ボナック核酸」(画像1)を開発し、2012年3月に特許査定を取得した(米国・欧州では各国移行審査請求済み)。
ボナック核酸は、同社が独自に開発した、次世代型の核酸干渉作用を有する基盤技術だ。従来のsiRNAとは異なる、ユニークな分子内構造(2次構造)を有する1本鎖長鎖核酸を構造的な特徴とし、従来のsiRNAが抱える課題であった生体内での安定性が改善されている。
なぜRNAが不安定化というと、体内にはRNAを切断するさまざまな種類の酵素があり、通常、体内に入ったRNAは迅速に分解されてしまうからだ。従って、多くの医薬品候補として用いられているsiRNAは、生体内での安定性を向上すべく、加水分解の起点となる部分を化学修飾することで保護している。しかし、それによる薬理作用の低下、人工的異物としての安全性への問題、さらに製造コストの増大など、新たな課題を生じてしまっているというわけだ。
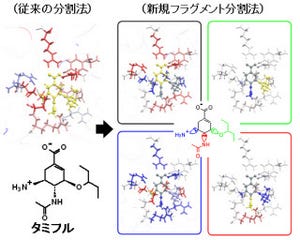
ボナック核酸は、RNA核酸の3'末端部分が分子内結合により折り返されている、ユニークな分子内構造を有する(画像2~4)。今後より詳細な検討を進めて行く必要はあるというが、ボナック核酸はこうした特徴的な分子内構造により、核酸分解酵素が作用しづらく、生物学的安定性(核酸酵素耐性)の向上に関与しているものと考えられているのである。

|

|
|
画像2。ボナック核酸は分子内に折りたたみ構造(分子内水素結合)を有し、核酸の物理化学的安定性や核酸酵素耐性などが向上している。この形状は「nkRNA」と呼ばれる |
画像3。nkRNAの折り返し(リンカー)部分を「プロリン誘導体」などのアミノ酸誘導体で置換したボナック核酸の1つの「PnkRNA」 |
また、ボナック核酸はすでに日本国内にて特許査定が認証されているため、特定の欧米企業が専有する既存の核酸干渉に関する基盤技術(特許)に依存することなく、独自の核酸医薬を開発することが可能という点も大きな特徴だ。
そして、ボナック核酸は従来から使用されている「TBDMSアミダイト」(主要な核酸の合成原料)では効率よく製造することができず、安価に高純度で大量に合成するには高性能なアミダイトが必須となる。
しかし、新たに開発された「EMMアミダイト」は、核酸合成における縮合効率及び製造価格が格段に改善されており、長鎖核酸オリゴマー(比較的分子量が低い重合体)でも安価に高品質で製造することが可能だ。
このように、ボナックは医薬品としての品質・コストに耐え得る原料製造技術、さらには安定同位体核酸を用いた薬物動態法を有する技術の開発にも成功しているのである。
そして、九大大学院医学研究院眼科学分野の石橋達朗教授らは、核酸医薬を用いた画期的な「糖尿病網膜症」治療薬の開発につながる新たな疾患因子として、「ペリオスチンパク質」を独自に同定し、これを新たな標的分子として見出した(画像5)。なお糖尿病網膜症とは糖尿病3大合併症の1つであり、日本では後天性視覚障害原因の約19%を占め、年間約3000人が失明しており、今後も患者数が増加するといわれている。
ペリオスチンは、細胞増殖に関与する細胞外マトリクスタンパク質であることが知られている。九大眼科学分野における研究により、ぺリオスチンタンパク質が「増殖糖尿病網膜症(PDR)」(糖尿病網膜症の進行したもの)患者の「硝子体」(眼球の水晶体後方の器官で、ガラス体とも呼ばれる)と「線維血管増殖組織」で対照に比べ有意に上昇していることが初めて見い出され、PDRの進展に関与していることが明らかとなった(画像6・7)。従って、ぺリオスチンは糖尿病網膜症治療の新しい分子標的となる可能性があるというわけだ。
また、PDRでは網膜上に線維血管増殖組織を生じ、その収縮に伴う「牽引性網膜剥離」が失明の原因となる仕組みだ。現在のところ、線維血管増殖組織生成の機序は十分には明らかになっていない。治療は網膜光凝固術と硝子体手術が行われるが、視機能を十分に保持できない場合も珍しくはないのである。
しかも、現時点で糖尿病網膜症を適応症とし承認されている治療薬はなく、本疾患におけるアンメットメディカルニーズは高く、新薬(新規治療法)の開発が求められているという状況だ。
さらに、東京医科大分子病理学講座の黒田雅彦主任教授らは、従来の2本鎖核酸分子に致命的な副作用として問題となっている「自然免疫応答」を、ボナック核酸は回避可能であることを見出し(画像8)、新規な「加齢性黄斑変性症」の治療薬に関する技術を開発したという経緯を持つ。
副作用の問題とは、siRNAを用いた遺伝子の発現抑制には、「Toll様受容体」(動物の細胞表面にある受容体タンパク質で、種々の病原体を感知して自然免疫を作動させる機能を有する)の活性化によるものだ。特にToll様受容体3(TLR3)は、ウイルスの2重鎖RNAを認識することにより活性化され、ウイルスへの防御機能として、インターフェロンなどのサイトカインなどを生成する。
siRNAはこのTLR3を活性化して、サイトカインを誘導する仕組みだ。そしてこの誘導はsiRNAの塩基配列には関係なく、2本鎖という構造に依存することが明らかとなっている。実際、これが理由で米国においてsiRNAによる第III相臨床試験が中断したとの評価があるほどだ。
ボナック核酸は折り返し構造を有するが、そもそも1本鎖であることから、こうした2本鎖RNAによるTLR3活性を回避し、「非特異的炎症誘導」が低減された副作用の少ない新しい治療薬となることが期待されるのである。
そうした経緯を持つ3者が技術を結集し、核酸医薬の開発及び臨床応用に進むべく、この度、アクアセラピューティクスを設立するに至ったというわけだ。
同社には、上記3者が、取締役及び科学諮問委員(SAB)として会社運営に参画し、それぞれに開発してきた特許技術を株式会社アクアセラピューティクスへ技術移転することで、これまで有効な治療薬がなかったさまざまな眼疾患に対し、日本初の核酸医薬品開発を目指す。
まずは、糖尿病網膜症に対する新しい分子標的であるペリオスチン遺伝子をターゲットとする核酸医薬の開発が目標だ。そして2013年10月を目途に前臨床試験、2015年初旬での臨床試験開始を計画している。