京都大学と高輝度光科学研究センター(JASRI)は4月16日、セラミックス材料が大量の水素を取り込む能力があることを発見したと発表した。
成果は、京大大学院工学研究科物質エネルギー化学専攻博士後期課程の坂口辰徳氏、同辻本吉廣博士研究員(現所属:物質・材料研究機構)、同小林洋治助教、同陰山洋教授、京大物質-細胞統合システム拠点の高野幹夫特定教授、JASRIの金廷恩副主幹研究員らの研究グループによるもの。そのほか、倉敷芸術大学、東京工業大学、物質・材料研究機構、レンヌ第一大学も共同研究に参加している。研究の詳細な内容は、4月15日付けで英科学誌「Nature Materials」に掲載された。
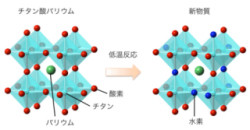
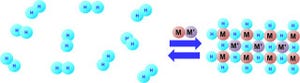
画像左のチタン酸バリウム(BaTiO3)は、1940年代に初めて合成されて以来、あらゆる電子機器に使われている誘電体材料だ。陰山教授らは今回の研究に先立ち、2007年に水素化物を利用した「低温合成法」によって、長年不安定であると考えられてきた鉄の局所構造を実現し、Nature誌に報告している。
なお低温合成法とは、一般的に酸化物(セラミックス)は1000℃以上の高温で合成されるが、適切な反応剤(今回の研究では水素化カルシウム)を選ぶことによって500℃以下の低温でも反応を進行させることが可能で、そのような反応のことをいう。
今回の研究では、チタン酸バリウムに対して同様の低温反応を施したところ、結晶中の酸素の一部を水素で置き換えることに成功した(画像・右)。構造は、理化学研究所が所有し、JASRIが運営する大型放射光施設「SPring-8」の粉末結晶構造解析ビームライン「BL02B2」の高輝度X線を用いて決定した形だ。
今までに、チタン酸バリウムに水素の導入を試みた研究例はあったが、その量はごく微か(酸素に対して0.1%以下)だった。しかし本手法を用いた場合、水素量は最大で20%(BaTiO2.4H0.6)にも達したのである。この新しく合成された物質は、水にも温度にも安定なので、クリーンなエネルギー資源である水素を変換/輸送/貯蔵するのに適した水素材料としての高い将来性があるというわけだ。
この新物質の学術的な意義は、その水素貯蓄量の多さだけではない。取り込まれた水素の電荷状態にもあるのだ。一般に酸化物に存在する水素は、正の電荷を持つ「プロトン(H+)」として存在する。身近な例では、サビの成分である水酸化鉄(Fe(OH)2)などだ。
これに対し、負の電荷を持つ「ヒドリド(H-)」は強力な還元剤であるため、チタンのような遷移金属とは共存できないと考えるのが固体化学の常識だった。ところが、今回得られた物質における水素は負の電荷を持っており、従来の常識を覆す結果となったのである。
今回の研究によって、酸化物の中でH-が遷移金属と共存できることが確認されたことにより、今後はヒドリドの流れを制御して利用することができる「酸化物ヒドリドニクス」という新たな学問体系として発展していくことが期待されると、研究グループはコメント。
今回合成した物質中の水素は、400℃程度の低温にて結晶内を動き回る能力を持つことを明らかにした。この結果は、水素イオン(H-)伝導性を示唆している。酸素イオン伝導体は、現在燃料電池の電解質として実用化されているが、水素は酸素と比べて軽くて動きやすいため、より低温での高速動作が原理的には可能だ。同時に、チタンが持つ電子に由来する電子伝導性もあるため、例えば、水素を燃料とする燃料電池に必要な電極のほか、水素センサとしての応用が期待されるとしている。