理化学研究所(理研)は1月30日、神経系に発現する膜タンパク質「SLITRKファミリー」の1つである「SLITRK3」が、神経細胞の「抑制性シナプス形成」に重要な役割を持つことを発見したと発表した。理研脳科学総合研究センター行動発達障害研究チームの有賀純チームリーダーや、カナダ・ブリッティシュコロンビア大学の高橋秀人研究員、アンマリー・クレイグ教授らの研究グループによるもので、成果は科学雑誌「Nature Neuroscience」に掲載されるに先立ちオンライン版に日本時間1月30日に掲載された。
神経細胞は情報を伝達することに特化した特別な細胞で、動物の感覚や行動などを制御していることは説明するまでもない。神経細胞同士が情報を伝え合う時には、神経細胞間に形成されるシナプスという構造が重要な役割を果たすことをご存じの方も多いだろう。シナプスとは、神経細胞間あるいは筋繊維、または神経細胞と他種細胞間に形成される、シグナル伝達などの神経活動に関わる接合部位とその構造のことだ。
構造的なタイプとしては、「化学シナプス(小胞シナプス)」と「電気シナプス(無小胞シナプス)」、および両者が混在する混合シナプスがある。そして、シグナルを伝える側の細胞を「シナプス前部」、伝えられる側の細胞を「シナプス後部」と呼ぶ。神経細胞の増殖の際に、特定の位置にある神経細胞が特定の細胞に軸索を伸ばし、シナプスを形成して神経回路を形成する仕組みである。
情報の伝達に神経伝達物質が使われるタイプのシナプスは、機能的に「興奮性シナプス」と「抑制性シナプス」に分類することが可能だ。興奮性シナプスでは情報を受け取った細胞が電気的に興奮しやすくなり、抑制性シナプスでは興奮しにくくなる。近年の研究から興奮性シナプスと抑制性シナプスのバランスが正常な脳機能活動に重要で、いくつかの神経疾患ではこのバランスが乱れていると考えられている具合だ。
また、最近の研究によってシナプスの形成に関わる分子についての理解も進み、興奮性シナプスの形成メカニズムについては多くのことが判明してきた。しかし、一方の抑制性シナプスの形成については、これに関わる分子が少数しか見つかっていないため、あまり理解が進んでいない状況である。
SLITRKファミリーは、2003年に理研脳科学総合研究センター発生発達研究グループが発見し、命名した神経系に発現する細胞膜貫通型タンパク質ファミリーだ。「SLITRK1」から「SLITRK6」まで6種類の細胞膜貫通型タンパク質からなるが、脳神経系や内耳などで産生されること、一部のものは高次脳機能の調節、神経回路の形成に重要な役割を持つことが判明している。
また、SLITRKファミリー1回膜貫通型タンパク質で、アミノ末端側にはロイシンリッチリピートというタンパク質-タンパク質間の結合によく用いられるドメインが2個存在し、カルボキシ末端側には神経栄養因子受容体と部分的に類似のアミノ酸配列が存在するのが特徴だ。
2009年と2011年に、米国とカナダのグループがこのタンパク質ファミリーとヒトとの精神神経疾患に関与する可能性を報告したことから、現在は疾患原因遺伝子の候補として注目を集めている状況だ。そこで研究グループは、SLITRKファミリーとシナプスの関わりに着目し、その機能や分子機構の解明に挑んだ次第である。
研究グループは、SLITRKファミリーとシナプス形成の関係性を調べるため、6種類のSLITRKファミリータンパク質をそれぞれ発現させた非神経細胞と、ラットの海馬の神経細胞を混ぜ合わせて培養を行った。すると、SLITRKファミリータンパク質を発現させた細胞に対して、海馬の神経細胞がシナプスに似た構造を作ることが明らかになったのである。
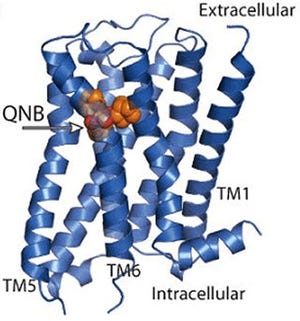
興奮性シナプスと抑制性シナプスそれぞれの局在がわかる特有な分子マーカーで調べると、SLITRK3タンパク質以外を発現させた非神経細胞は、興奮性と抑制性シナプス両方を同程度に誘導するのに対して、SLITRK3タンパク質を発現させた非神経細胞は、抑制性シナプスだけを強く誘導することが確認された(画像1)。
発現は、アフリカミドリザルの腎線維芽細胞を形質転換させた培養細胞の「非神経系培養細胞(COS細胞)」に、SLITRKファミリータンパク質の遺伝子を導入して実施。この細胞とラットの脳から取り出した海馬の神経細胞を混ぜ合わせて培養し、興奮性シナプス前部、抑制性シナプス前部に特有な分子マーカーに対する抗体を使った蛍光免疫染色を行った。すると、SLITRK3以外を発現させた非神経細胞には、興奮性と抑制性シナプス両方を同程度に誘導するのに対して、SLITRK3タンパク質を発現させた非神経細胞は、抑制性シナプスだけを強く誘導することがわかったのである。
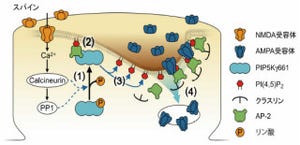
また、培養した海馬の神経細胞では、SLITRK3タンパク質は抑制性シナプスのシナプス後部(神経伝達物質を受け取る側)に存在する足場タンパク質「ゲフィリン」と共在し、興奮性シナプスの後部に存在する足場タンパク質「PSD95」とは共在しないということも判明。なお足場タンパク質とは、伝達物質が分子複合体を形成するための足場となることから、そのように呼ばれている。
さらに海馬の培養細胞の中で、SLITRK3タンパク質の遺伝子発現を減少させると、ゲフィリン陽性の抑制性シナプスの数が減少するのに対して、PSD95陽性の興奮性シナプスの数には明確な影響がなかったことがわかった。つまり、SLITRK3タンパク質は抑制性シナプスを誘導し、シナプス後部にゲフィリンと共在していることがわかったというわけだ。
なお、SLITRK3は脳全体で発現するが、特に海馬の「錐体細胞」層などで強いことが知られている。また錐体細胞とは、海馬に存在する主要な興奮性の神経細胞のことだ。その細胞体は明瞭な層状構造を形成するのが特徴。数多くの海馬の抑制性神経細胞が錐体細胞のさまざまな部位に抑制性シナプスを形成し、その活動を制御していることが知られている。
次に、シナプス形成にはシナプスの前部と後部の間でいくつかの分子が結合され、分子複合体を形成することが必要なことから、これまでにシナプスの形成に関与することが知られているいくつかの分子について、SLITRK3と結合するかどうかが検討された。
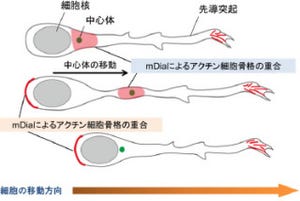
その結果、膜タンパク質の1つ「受容体型チロシンホスファターゼ(PTPRD)」がSLITRK3と結合することを確認。PTPRDはシナプス前部(神経伝達物質を放出する側)に分布しており、培養した海馬の神経細胞でPTPRDの遺伝子発現を減少させると、SLITRK3を発現させた非神経細胞と混合培養しても、抑制性シナプスが形成されにくくなった。つまり、SLITRK3はPTPRDと結合して、抑制性シナプス前部の構造を誘導すると考えられるというわけだ(画像2)。

|
|
画像2。SLITRK3とPTPRDの結合が抑制性シナプスの形成を促進する。SLITRK3はシナプス後部に、PTPRDはシナプス前部に局在している。両者の結合が抑制性シナプスを構成する分子複合体の形成を促進するものと考えられる |
なお、PTPRDは膜貫通型のタンパク質であり、通常2個の「ホスファターゼ関連ドメイン」を持つ。細胞外はさまざまな分子間相互作用に関わる「免疫グロブリン様ドメイン」、「フィブロネクチン3様ドメイン」が存在している。このグループのホスファターゼは、細胞外の情報を細胞内の伝達経路に伝える役割を担っていることが多い。PTPRD欠損マウスは空間学習機能に異常があり、海馬のシナプスの性質が変化していることが知られている。
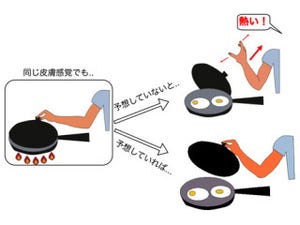
続いて、実際に脳の中でSLITRK3が抑制性シナプス形成に関与するのか調べるため、SLITRK3欠損マウスを作製し、そのシナプスの異常の調査が行われた。すると、海馬の錐体細胞の細胞体周囲で抑制性シナプス特有の分子マーカーの発現が減少していることが確認されたのである(画像3)。

|
|
画像3。SLITRK3欠損マウスの海馬における抑制性シナプスの様子。SLITRK3欠損マウスの海馬の錐体細胞層(*印)で、抑制性シナプスに特有な分子マーカーに対する抗体を用いたところ、正常マウスに比べて蛍光色が少なくなっている。つまり、抑制性シナプスが顕著に減少していることを示している |
そこでSLITRK3欠損マウスの海馬の切片でシナプスの活動を調べると、抑制性シナプスの活動に由来する電気信号が減少するのに対し、興奮性シナプスの活動に由来する信号には変化が認められなかった。つまり、SLITRK3欠損マウスの海馬の錐体細胞では、抑制性シナプスが減少することがわかったのである。
SLITRK3欠損マウスは、時々てんかんの発作に似た異常行動(突然無動状態になる、頭部を規則的にゆする、前肢を硬直させるなど)を示す。また、脳波を調べると振幅の大きい異常波が頻繁に観察された。これらの異常は、おそらく抑制性シナプスの機能が失われたために起きる神経細胞の過活動が原因であると推測されている。
今後、抑制性シナプスの脳機能における役割を詳細に解明するため、研究グループではSLITRK3欠損マウスの神経回路の異常や行動の異常を検証するという。特にSLITRK3を含めたSLITRKファミリーが持つ中枢神経系の興奮性・抑制性シナプスのバランスを制御する仕組みの解明は、基礎研究の観点から重要なテーマである。
さらにSLITRK3を含む抑制性シナプスの形成・維持に関わる分子機構を解明できれば、てんかんや多動症など神経細胞の過活動と関連した神経疾患の病態の理解や改善に役立つと期待できると研究グループではコメントしている。