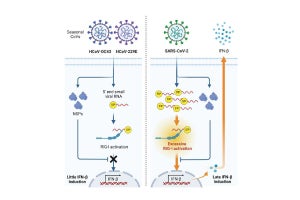
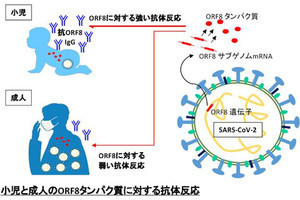
そこで今回の研究では、SARS-CoV-2が感染すると重症化を引き起こす可能性のある肺組織に由来する細胞株から精製されたRNAを基に、R-CAMPsの調整が行われたほか、R-CAMPsと蛍光分子で標識されたSARS-CoV-2のタンパク質を混合させ、タンパク質とRNAとの結合により強い蛍光シグナルが示されている微粒子を回収。その後、1つずつ回収された微粒子からDNAの増幅が行われ、DNAからRNAを転写合成することで選別されたRNAの再合成が行われ、その再合成されたRNAが、RdRpによるRNAの合成反応を抑制できるかどうかの検討がなされたという。
-

R-CAMPsの調整過程。さまざまな配列を有する鋳型DNAを基にして、(1)1つの微粒子に数十万コピーのDNAとRNAが固定化されている、(2)同じ微粒子には同じ配列のDNAとRNAが固定化されている、(3)異なる微粒子には異なる配列のDNAとRNAが固定化されている、といった特徴を有する微粒子群を一度に数百万種類得ることができる (出所:甲南大プレスリリースPDF)
その結果、RdRpによるRNAの合成反応を抑制できるRNAを複数種類獲得することに成功したとするほか、抑制効果が示されたRNAの配列解析から、グアニン塩基が豊富な配列を有していることが確認されたともしている。このような配列は、特徴的な立体構造の「グアニン四重らせん構造」を形成する可能性があるという。
-

RdRpに結合するRNAの選別過程。肺がん細胞に由来するRNA断片を固定化したR-CAMPsを調整し、蛍光色素「ATTO647」で標識したRdRpと混合。RdRpと結合するRNAを固定化している微粒子は、ATTO647の蛍光シグナルを示す。セルソーターを用いて、R-CAMPsの蛍光シグナルを解析しつつ、選別領域として設定した強い蛍光シグナルを示す微粒子を1粒子ずつマルチウェルプレート(96ウェルプレート)に回収 (出所:甲南大プレスリリースPDF)
同構造は、4つのグアニン塩基が平面上で円を描くように配置された「G-カルテット」と呼ばれる塩基対様式を基本としており、それが積み重なって形成されたものであることから、もっとも強い抑制効果が示されたRNAを用いて検討が行われたところ、グアニン四重らせん構造を形成することでRdRpの働きを抑えていることが判明したとする。
またこのRNAは、細胞外マトリクスを構成する一種である「ラミニンタンパク質」を構成する「β1サブユニット」をコードする遺伝子「LAMB1」から転写された産物のイントロン領域に存在していることも確認されたという。イントロンは、タンパク質をコードするmRNAの一次転写産物が合成された後に切り出される領域であり、これまではノンコーディングで不要な領域であると考えられてきたが、近年になって、同領域にも何かしらの生物学的な意味合いがあるのではないかと注目が集まりつつあるとされている。今回の研究成果では、同領域がSARS-CoV-2の複製を抑制できる可能性を有していることが示されたことになる。
なお、もともとヒトの中に存在するRNAであることから安全性が高く、このRNAを基に抗ウイルス効果を示す核酸医薬品の研究開発への展開が期待されると研究チームでは説明している。