東京医科歯科大学(TMDU)は2月17日、東海大学との共同研究により、ほ乳類の個体発生に重要な働きをする「ゲノムインプリント記憶」が、生殖細胞でリプログラミング(消去・再成立)される際の消去過程に「能動的脱メチル化機構」が機能することを、マウス個体を用いた実験で突き止めたと発表した。
成果は、TMDU 難治疾患研究所・エピジェネティクス分野の石野史敏 教授、同・李知英 特任講師、東海大の金児-石野知子 教授らの共同研究チームによるもの。研究の詳細な内容は、1月13日付けで英オンライン総合学術誌「Scientific Reports」に掲載された。
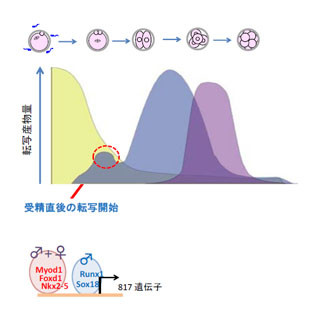
ほ乳類の発生過程では、ゲノムワイドな「DNA脱メチル化」が、(1)受精から着床までの初期発生の時期、(2)「始原生殖細胞(primordial germ cell:PGC)」が将来の生殖巣(精巣や卵巣)である生殖隆起まで移動し定住する時期で起きる。特に、PGCでは脱メチル化に伴うインプリント消去後、精子・卵子形成過程でインプリントが再刷り込み(再成立)されるので、インプリントは完全に消去(脱メチル化)される必要がある(画像1)。
画像1は、ゲノムインプリントのリプログラミングを表した概念図だ。ゲノムワイドの脱メチル化は、受精直後の受精卵(a)と生殖細胞系列のPGCの中で起きる(b)。精子、卵子に刷り込まれたゲノムインプリント(c、d)は体細胞系列で一生維持され、細い黒線がそれを表す。PGCは、初めは体細胞と同じゲノムインプリントを持っているが(太い黒線)、将来の生殖巣(卵巣や精巣)である生殖隆起に定住する前後で消去される仕組みだ(b)。
なおDNAメチル化とは、DNA塩基「シトシン(C)」が「メチル基(CH3)」で修飾されることをいい、一般的にはこれが起きると遺伝子が抑制される形だ。よって、DNA脱メチル化は、その反対の現象である。ゲノムインプリントの場合、精子、卵子にメチル化状態が刷り込まれ、インプリント遺伝子の発現・抑制の両方に機能し、消去の際に脱メチル化される。
そのゲノムインプリントとは、ほ乳類発生に重要な「エピジェネティック」情報の1つのことで、父親・母親由来ゲノムからのみ発現する「インプリント遺伝子」の発現制御を行う。ゲノム刷り込みともいわれるこの情報は、ほ乳類のライフサイクルで生殖細胞において消去・再成立され次世代に伝わる形だ。
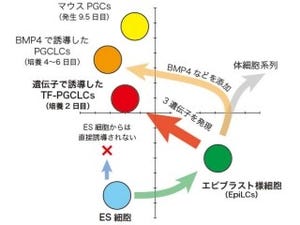
脱メチル化過程でメチル化シトシン(5mC)は異なる2つの機構で未修飾のシトシン(C)に変換される。「受動的脱メチル化(passive demethylation)」は5mCが細胞分裂に伴って希釈されていく機構、「能動的脱メチル化(active demethylation)」は細胞分裂に依存せずCまで変換する機構だ。しかし、前述した(1)、(2)の時期にどちらの機構が関与するのか、見解は二転三転していたという(画像2)。
初期発生における卵子に由来する「雌性前核」は、細胞分裂と共に徐々に希釈される受動的脱メチル化を受ける(画像2a)。それに対して精子に由来する「雌性前核」、つまりPGCにおけるゲノムインプリントの消去は能動的脱メチル化の代表例と考えられていた(画像1・2b)。
しかし2009年以降、ゲノム中に5mCの酸化誘導体である「ヒドロキシメチル化シトシン(5hmC)」などの存在が確認され、この酸化反応を触媒する「Tet(ten eleven translocation)酵素」群もほ乳類で同定されたことから、それまでの考えは大きく修正されることになったという。
5hmCは「能動的脱メチル化機構」の中間体でもあるが、雄性前核の場合、Cから5hmCへの急速な変換後は受動的に希釈されること(画像2c)、PGCでのゲノムインプリント消去も、PGCの細胞分裂速度の速さから考えて受動的脱メチル化を支持する意見が優勢になったのである(画像2c)。
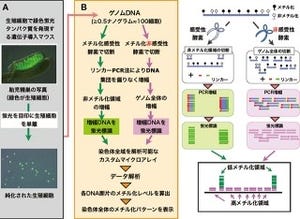
2002年に研究チームは胎仔期のPGCにおいてインプリント記憶の消去が起きる過程を世界で初めて検出することに成功した。インプリント消去途中のDNAメチル化パターンがモザイク状を示すことが能動的脱メチル化の関与を示唆する証拠であると考えられ(画像3)、受動的脱メチル化反応に対する阻害剤としてDNA複製阻害剤の「アフィディコリン」、能動的脱メチル化の阻害剤としてDNA塩基除去修復に働く「Poly(ADP-ribose)polymerase(PARP)阻害剤」の「3-AB」の2つの薬剤のPGCにおける脱メチル化における効果が生体において測定された。
画像3は、PGCにおけるゲノムインプリントの消去に関するグラフとモザイク状メチル化パターン。胎仔から分離したPGCの「H19-DMR」の場合、PGCにおける脱メチル化は胎仔期9.5日目から11.5日目までにほぼ完了する。途中のメチル化パターンには、メチル化(黒丸)部分と非メチル化(白丸)部分が1本のDNA(左から右への一行)に混在したモザイク状模様が見られる。細胞分裂による希釈では説明できず、能動的脱メチル化の関与が示唆されるとした。
その結果、どちらの薬剤も脱メチル化を阻害することから、両方の機構がこれに関係していることが判明した(画像4)。特に、DNA複製を止めた状態でも脱メチル化反応が進むことは(画像4)、生体内でのPGCのインプリント消去に能動的脱メチル化機構が積極的に関与することを物語っているという(画像2d)。
画像4は、脱メチル化反応に対する阻害剤の効果を表したグラフ。胎仔期9.5日目から半日置きにDNA複製阻害剤または塩基除去修復阻害剤を母体に投与し11.25日目に胎仔から分離したPGCのH19-DMRのメチル化度が調べられた。コントロール(右)と比べて塩基除去修復阻害剤(中央)の高い阻害効果は能動的脱メチル化の証拠だとする。DNA複製阻害剤(左)も一部に阻害効果が見られたが、脱メチル化はかなり進行していることも能動的脱メチル化の関与を示唆するという。
卵子形成では、インプリント消去の開始から短時間で、「減数分裂第一分裂」に入り、そこで個体の性成熟まで細胞分裂が停止する。完全に両親由来のインプリンティング記憶の消去(特に父親由来のインプリント記憶消去)がなされないと、次世代の子供の発生に重大な問題を生じると考えられるという(画像5)。その意味で、PGCにおける能動的脱メチル化は、ヒトを含めたほ乳類の個体発生において重要な役割を果たしているといえるとした。
画像5は、能動的脱メチル化の生物学的意義を表した概念図。メスのPGCではゲノムインプリントの消去開始から減数分裂が開始されるまでの細胞分裂の回数は限られる。受動的脱メチル化だけでは幾つかの卵細胞にメチル化DNAが残り(細胞分裂3回ならば2/8、4回ならば2/16)、特に、父親型インプリントが残る場合は発生異常の原因となると考えられるという。よって、能動的脱メチル化はゲノムインプリントの完全な消去に必須の機構と考えられるとしている。
今回の研究はゲノムインプリントの消去に能動的DNA脱メチル化が関与することを、生体内から分離したPGCを用いて明らかにすることに成功した形だ。今回の成果は、PGCにおける真の脱メチル化機構を明らかにしただけでなく、能動的DNA脱メチル化の卵子形成における重要性を示したことで、ほ乳類の生物学に重要な新局面を拓いたものといえるとしている。