九州大学(九大)と日本トリムは、「分子状水素」及び「還元性ミネラルナノ粒子」を含む「電解還元水」が悪性のがん細胞であるヒト線維肉腫「HT-1080」細胞内の「過酸化水素」を消去し、同細胞の浸潤を抑制することを発見したと発表した。
成果は、九大大学院 農学研究院の白畑實隆教授らと、日本トリムの研究者らの共同研究グループによるもの。研究の詳細な内容は、「rends in Food Science & Technology」2011年11月号でオンライン掲載された。
がんは日本において男性2人に1人、女性の3人に1人が罹患し、3人に1人ががんで亡くなっている状況だ。がんはステージIからIVまで分類され、それがさらにa及びbに分けられている。がんが転移・浸潤を始めるステージIIIbからIVに進行すると治療が非常に難しくなるのはいうまでもない。
がんには主だった悪性の性質として、以下の6つがある。(1)勝手に増殖する、(2)増殖を停止させることができない、(3)アポトーシス(自殺死)を起こさない、(4)血管新生を行い栄養を独り占めにする、(5)無限の寿命を持つ、(6)転移・浸潤を行い、全身に広がっていく、だ。
この中でも、最も厄介な性質ががん細胞が1カ所に留まらずに全身に広がる転移・浸潤で、どのがんもその結果として、患者を死亡させてしまう原因となっている。
悪性のがんは抗がん剤や放射線に対する耐性すら持ち、増殖速度を速めていく。こうしたがんに対する3大標準療法は(1)外科的療法、(2)放射線療法、(3)化学療法(抗がん剤療法)の3つだが、いずれもがんによる死因の大半を占める進行がんには有効ではない。有効な治療法を見出せないまま、がん患者の数は増加の一途をたどっているのが日本の現状だ。
がんの発生機構として、まず体内の正常細胞の遺伝子に変異が生じた変異細胞が発生し、さらに異常細胞が活性酸素(ROS)を浴び続けることによりがん細胞に変化すると考えられている。
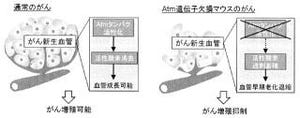
がん細胞がさらに活性酸素を浴び続けると、転移・浸潤、薬剤耐性(抗がん剤が効かなくなる)、発がん遺伝子活性化・がん抑制遺伝子不活性化、染色体の不安定化などのさらに悪性の性質を持つ細胞に変化していく(画像1)。
がんの悪性の性質を支えているのが活性酸素種であると考えられているが、現在の3大療法はいずれも活性酸素を発生させて生体の免疫力や自己治癒力を低下させ、新たながんの発生やより悪性化したがんの発生を助長する可能性がある矛盾した療法といえる。
ただし、がん細胞内の活性酸素のレベルを適切に制御することで、がん細胞の悪性の性質を良性化できる可能性があるという。ビタミンC、ビタミンE、ポリフェノールやカテキンなどの抗酸化剤は活性水素(原子状水素)を放出することで活性酸素を消去することが可能だ。
しかし、活性水素を放出した抗酸化剤は、次に活性酸素を発生させる酸化剤として働くという両刃の剣的な性質を持っているため、従来の抗酸化物質によりがんを抑制するのは容易ではない。抗酸化力のみを示し、酸化力を示さない安定な新しい抗酸化剤が求められている。
電解還元水はアルカリイオン水とも呼ばれ、日本では広く普及している健康に良いとされる機能水の1つだ。電解還元水は、胃腸症状の改善に有効な医療用の水として厚生労働省に薬事法で認可を受けている。そして、電解還元水中の活性物質なのが、水の電解で生成する分子状水素と還元性ミネラルナノ粒子だ。
分子状水素と還元性ミネラルナノ粒子のいずれにも活性酸素種消去作用が確認されている。分子状水素は活性酸素を直接あるいは間接的に消去して安全な水に変えてくれるのだ。
還元性ミネラルナノ粒子は「SOD酵素様活性」や「カタラーゼ様活性」、「ヒドロキシルラジカル消去活性」など多面的な活性酸素種消去活性を持つ新しい抗酸化剤として注目されている。
分子状水素と還元性ミネラルナノ粒子を持つ電解還元水は細胞内活性酸素消去活性を示し、マウス及び線虫の寿命延長作用、抗腫瘍効果、抗糖尿病効果、抗動脈硬化症効果、抗神経変性症効果、抗アレルギー効果、放射線防護効果、肝臓保護効果、胃粘膜障害保護効果、網膜保護効果、抗がん剤の副作用軽減効果、抗二日酔い効果など多彩な生理効果を示すことが多数の論文により示唆されており、血液透析の水に電解還元水を使用する電解水透析法では副作用が軽減されるなど医療への応用も進んでいる状況だ。
電解還元水ががん細胞の増殖抑制、血管新生抑制、白血病細胞の正常細胞への分化誘導、化学発がん抑制などの抗腫瘍効果を持つことがすでに報告されている。そして今回、白畑教授と日本トリムによって、電解還元水ががん細胞の最も悪性の性質の1つである浸潤活性を抑制することを明らかにしたというわけだ。
悪性腫瘍の1つであるヒト線維肉腫HT-1080細胞は、高頻度で転移・浸潤を起こす細胞である。近年の研究で、がん細胞内に蓄積する過酸化水素(活性酸素種の1つ)が、「MMP-2」などの「金属プロテアーゼ(タンパク分解酵素)」の生産及び分泌を促進し、コラーゲンなどのがん細胞を取り巻く繊維状タンパク質を分解することにより、がんの浸潤が促進されることが明らかとなってきた。
がん細胞の浸潤能はコラーゲンゲルの上にがん細胞をまき、がん細胞がコラーゲンゲルを破壊して潜り込む能力を調べる「インビトロ浸潤アッセイ試験」で調べることが可能だ。
そして最近の研究では、過酸化水素ががん細胞の浸潤に直接関係していることが報告されている。NaOH水を電解することにより作製した、組成が単純な電解還元水はHT-1080細胞内の過酸化水素を消去すると共に、浸潤能力を抑制することが明らかとなった。
特に、電解還元水は過酸化水素処理により浸潤能力が高まった細胞により抑制効果が示された(画像2)。作用機構を詳細に調べたところ、電解還元水はMMP-2の遺伝子発現を抑制し、MMP-2タンパク質の酵素活性も抑制することが明らかとなったのである。
MMP-2の活性化を促進する「MT1-MMP遺伝子」の発現も電解還元水により抑制されたが、MMP-2の活性を阻害する「TIMP遺伝子」の発現は抑制されなかった。MMP-2遺伝子発現抑制経路を調べるために「マイトジェン活性化プロテインキナーゼ(MAPK)」の特異的阻害剤を用いて検討した結果、電解還元水は「p38MAPK経路」を介してMMP-2遺伝子発現を抑制していることが示唆されたのである(画像3)。

|

|
|
画像2。電解還元水による過酸化水素刺激ヒト線維肉腫細胞HT-1080細胞の浸潤抑制。24時間処理時の浸潤細胞数が測定された。■:コントロール培地、□:電解還元水培地 |
画像3。電解還元水によるがん細胞の浸潤抑制機構 |
今回の研究に関する論文は、Trends in Food Science & Technologyにて2011年11月に掲載されてから2012年3月までの90日間で最もよく読まれた論文の第1位を占めたことから、今後、電解還元水に関する研究が世界的に活発になるものと期待されるという。
今後の展開として、あらゆるがんに対しても抑制効果を示すのかどうかを調べるために、さまざまな臓器別がん細胞に対する効果を調べる必要があると、研究グループは述べている。
また、腫瘍を排除する腫瘍免疫の活性化作用についても詳細に検討する必要があるという。こうした基礎研究を基に、より有効な高機能電解還元水を開発すると共に、動物実験、ヒト臨床試験を行い、低コストでがんの予防及び治療に役立つ医療補助水としての電解還元水の利用方法を確立する必要があるとした。
さらに、電解還元水の日常的飲用により、がん細胞内の活性酸素レベルを低下させ、がん細胞の増殖抑制、血管新生抑制、転移・浸潤抑制を図り、がん細胞の悪性の性質を良化できる可能性があるとする。
電解還元水に関する研究は生体が持つ自己治癒力及び自己免疫力を高め、がんと闘うというよりむしろがんの悪性の性質を緩和し、がんとの共存を可能にする新たながん治療法の確立に貢献することが期待されると、研究グループはコメントしている。