東京医科歯科大学(TMDU)は3月12日、皮膚アレルギー炎症局所の1細胞RNAシーケンス解析を行い、皮膚にやって来た「炎症性単球」がアレルギーを抑制する「マクロファージ」へと変化していく仕組みを解明したと発表した。
同成果は、TMDU 高等研究院 炎症・感染・免疫研究室の三宅健介特任助教、同・伊藤潤哉大学院生、同・髙橋和総大学院生、同・烏山一特別栄誉教授、TMDU 教養部の中林潤教授らの共同研究チームによるもの。詳細は、英オンライン科学誌「Nature Communications」に掲載された。
日本におけるアトピー性皮膚炎をはじめとするアレルギー疾患の罹患者数は年を追うごとに増えており、たとえばアトピー性皮膚炎の場合は、2020年の集計で約125万3000人とされている。アレルギー疾患の罹患者数は非常に多く、患者のQOL低下や医療費負担の増加が社会的に問題となっているものの、アレルギーの病態にはいまだに数多くの不明な点が残されており、その病態の解明が強く望まれている。
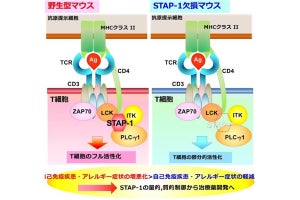
そうした中で、研究チームはこれまで、慢性皮膚アレルギー炎症のモデルマウスを開発し、アレルギーが生じる理由として、抗体「IgE」と、血中を流れる白血球の仲間の内ではわずか0.5%ほどしかいない希少な免疫細胞である「好塩基球」が重要であることを解明した。さらに、同アレルギーモデルマウスにおいて、炎症性単球が皮膚へとやって来て、炎症収束型のマクロファージへと変化することで、アレルギー炎症を抑制することも明らかにしている。
単球は白血球の一種で、炎症性単球はその仲間のうちでは主要グループの1つ(もともとは炎症を引き起こすと考えられていたことから、このような名称がつけられた)。しかし、炎症性単球がどのような経路で誘導されることで、炎症を収束させるタイプのマクロファージとなるのか、さらに、どのようにしてアレルギーを抑制しているのか、その仕組みはまだ解明されていなかったとする。
そこで今回の研究では、アレルギーモデルマウスにおいて炎症抑制型マクロファージの性質を調べるため、アレルギーが起こっている現場に存在する1つ1つの細胞の遺伝子発現を網羅的に調査できる手法である1細胞RNAシーケンス解析を用いて、アレルギーが起こった皮膚細胞を解析することにしたという。
解析の結果、血中を循環する炎症性単球が皮膚に入って来た後、まず中間型のマクロファージへと変化し、そして最終的に炎症抑制型のマクロファージへと2段階で変化していくことが突き止められた。さらなる解析から、好塩基球の産生するタンパク質「インターロイキン4」(IL-4)が炎症性単球に作用することで、炎症抑制型マクロファージへの変化を引き起こしていることも判明。さらに、詳細に炎症抑制型マクロファージの性質を調査したところ、死細胞や炎症分子を貪食(どんしょく)する能力が非常に高いことも確認されたとした。
反対に、炎症性単球が皮膚に入り込めないように作り出された「CCR2欠損マウス」を用いた実験から、炎症現場において炎症抑制型マクロファージの数が極端に減少し、除去されずに残った死んだ細胞が炎症性分子「インターロイキン-1α」を分泌することで炎症が悪化し、アレルギー症状が長引いてしまうことも発見された。
今回の研究により、炎症を悪化させる細胞である炎症性単球が、アレルギーを抑制する炎症抑制型マクロファージに変化していく過程が明らかにされた。さらに、アレルギーを抑制するマクロファージが炎症性単球から誘導される仕組みをより詳しく解析することで、アトピー性皮膚炎をはじめとするアレルギー炎症を効率的に抑制できる有望な治療標的の開発につながることが期待されるとしている。