愛媛大学、東京大学、神戸大学などの研究グループは、糖鎖異常型とよばれる筋ジストロフィーモデルマウスの治療に成功したことを発表した。
同成果は、愛媛大学大学院医学系研究科の金川基 教授、東京大学大学院医学系研究科の戸田達史 教授、神戸大学大学院医学研究科の徳岡秀紀 医師、蘭ラドバウド大学 ドンデルス脳認知行動研究所 神経学分野のDirk J. Lefeber教授らの研究グループによるもの。詳細は、2022年4⽉14日付で「Nature Communications」に掲載された。
筋ジストロフィーは筋力が進行性に低下していく遺伝性疾患の総称で、有効な治療法が未だに確率されていない難病として知られている。長年の研究によって現在までに、50種類以上の原因遺伝子が特定されており、その中にタンパク質や脂質に結合した形で機能を発揮する、生体にとって重要な物質である「糖鎖」の異常(糖鎖の材料となる物質の異常も含む)によって発症する病型(糖鎖異常型)もあり、日本の小児期筋ジストロフィーで2番目に多くみられ、発症率は3万人に1人とされる福山型筋ジストロフィー(FCMD)などが知られている。
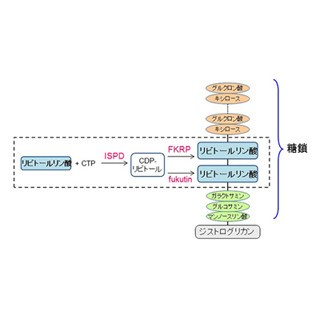
FCMDに代表される糖鎖異常型筋ジストロフィーは、1998年にFCMDの原因遺伝子「フクチン」が戸田教授らによって発見されて以降、研究が盛んに進められるようになった。そして2001年に糖鎖異常が発見されて以降、糖鎖異常型筋ジストロフィーの原因遺伝子が次々と同定されるようになり、2016年には糖鎖の中から新規化合物「リビトールリン酸」と、その生合成に関わる酵素(フクチンならびにフクチン関連タンパク質(FKRP))、およびリビトールリン酸の材料となる物質であるCDP-リビトールとその合成酵素ISPD(イソプレノイドドメイン含有タンパク質)の発見が今回の研究グループによってなされたともあり、近年、治療法の開発が世界的に進められるようになってきたという。
こうしたさまざまな研究から現在、糖鎖異常型筋ジストロフィーの原因遺伝子は18種類以上が同定されているほか、筋肉細胞の表面にあるジストログリカンという糖タンパク質が重要であることまで判明。糖鎖異常が生じると、細胞外基底膜と細胞膜上に存在するジストログリカンが担っているこれらの連携が、細胞膜と基底膜がやや剥がれた状態となり、筋肉の収縮作用による物理負荷によって膜安定性が低下し、結果として筋生理機能が低下。最終的には筋細胞が壊死し、筋ジストロフィーが引き起こされるということまで分かるようになってきたとする。
しかし、有効な治療法の開発までには至っておらず、その開発が国内外から求められていたという。
そこで今回、研究グループでは、糖鎖異常型筋ジストロフィーの発症メカニズムの解明と治療法の開発を目指して、筋肉中のISPD遺伝子を欠損するマウス(ISPD欠損マウス)を作出。
同マウスはヒト患者と同様の筋ジストロフィー様の所見を呈すことが確認されたほか、筋肉に含まれるCDP-リビトール濃度が低く、筋力も弱く、体重も軽く、20週齢までにすべて死去することが確認され、結果として糖鎖異常が生じており、これらの異常が発症要因であることが示されたという。