熊本大学は2月2日、腎臓の高次構造を作る3種類の前駆細胞のうち、これまでに多能性幹細胞から誘導することに成功していた「ネフロン前駆細胞」と「尿管芽」に続き、残りの1つである「間質前駆細胞」をマウスES細胞から誘導する方法を開発したと発表した。
同成果は、熊本大 発生医学研究所の谷川俊祐講師、同・田中悦子大学院生、西中村隆一教授らの研究チームによるもの。詳細は、英オンライン科学誌「Nature Communications」に掲載された。
現在、日本における腎不全による人工透析患者数は、33万人を超えているとされている。腎不全は急性の場合は治療が可能だが、慢性の場合は機能を回復させることが難しいため、腎移植しか治療法はなく、その機会は限られてしまっているため、人工腎臓の活用が求められている。しかし、腎臓は多数に分岐する管の周囲に濾過を司る装置が配置された複雑で高次な構造を持つ臓器であり、人工的に作り出すのは難しいとされている。
この高次構造はネフロン前駆細胞、尿管芽、間質前駆細胞の3つの前駆細胞から作り上げられており、研究チームは2014年にマウスES細胞およびヒトiPS細胞から、ネフロン前駆細胞の誘導法を確立し、ネフロンを含む腎臓組織の作製に成功しているほか、2017年には多能性幹細胞から尿管芽を誘導する方法も発表している。
今回の研究は、残る多能性幹細胞から間質前駆細胞を誘導する方法を確立し、ネフロン前駆細胞および尿管芽と組み合わせることで、多能性幹細胞から高次構造を有する腎臓を作ることを目指したものだという。
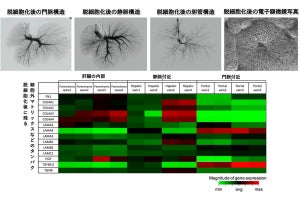
具体的には、胎児期のマウス腎臓を用いて、間質前駆細胞に特徴的な遺伝子群やその発生メカニズムを同定することからスタートした後、間質前駆細胞の起源である「後方中間中胚葉」と呼ばれる組織を抗体を用いて単離する方法と、それを間質前駆細胞まで誘導する培養条件を確立。そして、これらを基にしてマウスES細胞から後方中間中胚葉を経由して間質前駆細胞を誘導する方法を開発したという。
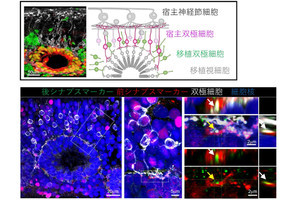
この誘導された間質前駆細胞を、同じくES細胞から誘導されたネフロン前駆細胞および尿管芽と組み合わせて試験管内での培養を行ったところ、多数に分岐する集合管の周囲にネフロンが配置された腎臓本来の高次構造を作ることに成功したとする。
また、実際にマウスに移植してみたところ、血管が進入してさらに成熟し、濾過機能に重要な「メサンギウム細胞」や血圧調節を担う「レニン産生細胞」など、特殊な間質細胞もES細胞から分化することが確認されたという。
今回の研究成果は、腎臓という複雑な臓器本来の高次構造を試験管内で多能性幹細胞から構築することに成功したことを意味するものであり、ヒトあるいは他臓器への応用が期待されると研究チームでは説明している。分岐する管構造の周囲に機能ユニットが配置されるという高次構造は腎臓に限ったものではなく、肺や肝臓、膵臓など多くの臓器に共通していることから、今回の原理を応用することで、他臓器でも同様の高次構造を試験管内で作れるようになる可能性があるともしている。
なお、間質前駆細胞の誘導法をヒトのiPS細胞に適用すれば、高次構造を持つヒト腎臓を作れるようになるはずだともしており、今回の成果は、将来の移植可能な腎臓作製に向けた重要な技術基盤になるとするほか、より本物に近い腎臓を作ることで、病態の再現や創薬への貢献も期待されるとしている。