東京大学(東大)と日本医療研究開発機構(AMED)は1月26日、腸管内腔に分泌されるリン脂質分解酵素の1つである「IIA型分泌性ホスホリパーゼA2」(sPLA2-IIA)が、腸内細菌叢のバランスを変えることによって、皮膚がんや乾癬(かんせん)などの皮膚疾患に影響を及ぼすことを発見したと発表した。
同成果は、東大大学院 医学系研究科の村上誠教授、慶應義塾大学(慶大) 薬学部の有田誠教授、慶大 先端生命科学研究所の曽我朋義教授、医薬基盤健康栄養研究所の國澤純プロジェクトリーダーらの共同研究チームによるもの。詳細は、生物学および疾患の治療に関連する分野を扱う学術誌「JCI insight」にオンライン掲載された。
sPLA2-ファミリーは、細胞外に分泌されるリン脂質分解酵素の一群で、そのうちの1つであるsPLA2-IIAは1980年代後半に発見され、長年の研究から、ヒトにおいては、炎症時にさまざまな組織中に発現誘導されることが知られており、その機能として、発現局所において脂質メディエーターの産生を介して炎症に関わる可能性や、感染細菌の膜リン脂質を分解することで生体防御に関わる可能性などが提唱されてきた。また、例外的にヒトの腸管には炎症の有無に関わらずsPLA2-IIAが常に高発現しているが、その生理的意義は不明だったという。
特定のタンパク質の生体内での機能を調べるために、その遺伝子を欠損(ノックアウト:KO)させたマウスが良く用いられるが、中でもC57BL/6系統のマウスは広く用いられている。しかし、C57BL/6系統のマウスはsPLA2-IIA遺伝子に先天的な変異を持ち、sPLA2-IIAを発現していないことから、sPLA2-IIAの生体内機能の解析には、sPLA2-IIA過剰発現(トランスジェニック)マウスが利用されてきた。
今回、研究チームが着目したのは、正常のsPLA2-IIA遺伝子を持つBALB/c系統のマウスで、この系統を用いてsPLA2-IIA遺伝子のKOを実施したところ、多くの組織でsPLA2-IIAの発現が見られるヒトとは異なり、野生型のBALB/cマウスでは、sPLA2-IIAは腸管(小腸>大腸)にほぼ限局して発現していることが確認されたという。
こうした組織分布に関する動物間種差はしばしば問題となるが、見方を変えれば、このノックアウトマウスは、腸管に恒常的に高発現しているsPLA2-IIAの機能を調べるのに向くツールとして考えられるという。また、村上教授らはこれまで、sPLA2-ファミリーのすべての分子種のKOマウスを網羅的に作製し、表現型の比較解析を進めてきており、その過程で、sPLA2-IIAKOマウスでは皮膚がんができにくい一方で、乾癬が悪化しやすいことを見出していたという。
-

(A)BALB/cマウスにおけるsPLA2-IIA(Pla2g2a-/-)の発現分布。(B)皮膚化学発がんモデルにおいて、sPLA2-IIAKOマウスでは野生型マウス(WT)と比べて皮膚がんの形成率および出現率が低減する (出所:東大プレスリリースPDF)
しかし、開発されたBALB/cマウスではsPLA2-IIAは腸管のみに発現しており、皮膚や免疫系を含む、腸管以外の組織では痕跡程度しか検出できないため、なぜ皮膚に表現型が顕在化するのかは謎であったという。
小腸において、sPLA2-IIAはさまざまな抗菌ペプチドを分泌するパネート細胞に発現しており、抗生物質の投与によりその発現が低下することから、sPLA2-IIAは腸内細菌成分により発現誘導され、抗菌ペプチドの1つとして腸内細菌の膜リン脂質を分解して腸内細菌叢のバランスを変えることで、二次的に皮膚に影響を及ぼしている可能性が想定された。
実際に、sPLA2-IIAKOマウスと野生型マウスの腸内細菌叢の比較解析を行ったところ、KOマウスでは属レベルで一部の腸内細菌(Helicobacter、Ruminococcus、Lachnospira属など)に明らかな相違が見られたという。
-

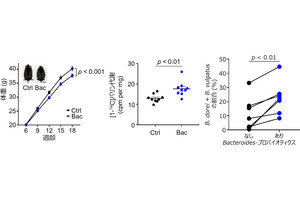
(A・B)腸内細菌叢の解析。(C)皮膚がんモデルにおいて、別居飼育した野生型マウスはKOマウスと比べて腫瘍数が多いが、同居飼育群では皮膚がんの発症が低下し、KOマウスのレベルに近づく。(D)野生型マウスとsPLA2-IIAKOマウスの小腸における遺伝子発現の網羅的プロファイリング。(E)腸内細菌叢の違いを反映して、sPLA2-IIAKOマウスの小腸では野生型マウスと比べて免疫グロブリン(抗体)遺伝子の多くが発現増加している(赤色で表示されている) (出所:東大プレスリリースPDF)
そして、sPLA2-IIAKOマウスと野生型マウスに対し、出生時から同居飼育が行われたところ、互いに食糞する結果、両群の腸内細菌叢に違いが見られなくなり、野生型マウスとKOマウスの皮膚の表現型の差が消失することも確認されたとするほか、KOマウスの小腸では腸管の免疫や上皮バリアに関わる遺伝子群の発現に変化が見られ、特に腸内細菌叢の違いを反映して免疫グロブリン(抗体)遺伝子の発現が変化していたことも確認されたという。
さらに、KOマウスは野生型マウス比で19の血漿成分に有意な変化が見られ、その中には免疫調節やがん化に関わるものも含まれていることも確認。糞便中の脂質を網羅的に分析した結果、KOマウスでは宿主ではなく腸内細菌に固有に存在する脂質成分が有意に減少していたという。
-

代謝物の解析。sPLA2-IIAKOマウス(Pla2g2a-/-)と野生型マウス(Pla2g2a+/+)を比較すると、血中の水溶性代謝物(A)や糞便中の脂溶性代謝物(脂質)(B)に違いが見られる (出所:東大プレスリリースPDF)
加えて、よりクリーンな飼育環境での飼育が行われたところ、野生型マウスの腸管においてHelicobacterやRuminococcusなどの腸内細菌が減少し、その結果、sPLA2-IIAの発現量が低下することで、野生型マウスとKOマウスの間で腸内細菌叢に違いが見られなくなり、それと同時に皮膚の病態に差が認められなくなることが確認されたという。
これらの結果を受けて研究チームでは、小腸パネート細胞から分泌されるsPLA2-IIAは腸内細菌叢の調節に関わり、この経路が遮断されると腸内細菌叢に変容が生じ、二次的に遠隔の皮膚に表現型が顕在化するとの結論に達したとする。
今回の研究成果は、sPLA2-IIAの腸管における機能を明らかにしたものだが、腸管にはsPLA2-IIA以外のsPLA2-分子種も発現していることから、これらも同様に腸内細菌叢の制御を介して遠隔臓器に影響を及ぼしている可能性があり、今後はこれを証明し、理論を一般化することが必要だと研究チームでは説明する。また、ヒトとマウスではsPLA2-IIAの発現分布に違いがあるが、腸管に高発現している点については共通していることから、ヒトにおいても腸管のsPLA2-IIAは腸内細菌叢の調節に関わっていることが予想されるとしており、腸管のsPLA2-IIAを標的とした創薬は、皮膚疾患の新たな診断や治療に役立つ可能性が期待できるとしている。