金沢大学は1月6日、「非アルコール性脂肪性肝疾患」(いわゆる脂肪肝)の進行の原因として、細胞の遊走を促すタンパク質の一種であるケモカイン分子「CCL3」が重要な役割を果たしていることを明らかにしたと発表した。
同成果は、金沢大 医薬保健研究域医学系の長田直人講師らの研究チームによるもの。詳細は、ヒトの代謝の側面に関連する全般を扱う学術誌「Metabolism」に掲載された。
脂肪肝とは、肝臓に中性脂肪が蓄積して障害されている疾患であり、その原因の1つとしてアルコールの飲みすぎが知られているが、近年の研究から、ほとんどアルコールを飲まないにもかかわらず、肥満などの生活習慣病に伴って生じる「非アルコール性脂肪性肝疾(NAFLD)」が増加していることが確認されるようになってきたという。
NAFLDには脂肪蓄積しか認めない単純性脂肪肝と、さらに進行して炎症と線維化も生じる「非アルコール性脂肪肝炎(NASH)」があり、NASHから肝硬変や肝がんに進行することも知られている。NAFLDの進行には、病原微生物の感染部位に白血球をはじめとする免疫細胞を呼び込み、免疫反応を促進させる作用を持つタンパク質であるケモカインが関与しているとされるが、その数は現在、約50種ほどが知られており、NAFLDにおいてはどれが疾患の進行に本質的な役割を果たしているのかはよく分かっていなかったという。
そこで研究チームは今回、ケモカインの一種でマクロファージによって作り出される「CCL3」に注目。マクロファージ炎症タンパク質の「MIP-1α」としても知られており、多形核白血球の浸潤や活性化、好中球による活性酸素種の生産に関わり、急性炎症を誘導すると考えられている。
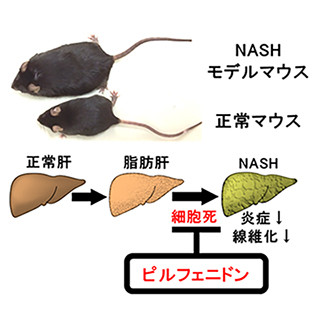
今回の研究では、NASHモデルマウスを用いて、さまざまな重症度のNAFLD患者の肝病理像と血液中のCCL3濃度の比較・検討を実施。その結果、研究チームが着目した通り、NAFLDの進行において、CCL3が重要な役割を果たしていることが判明したという。
またCCL3欠損マウスでは、対照の野生型マウスと比べ、高脂肪・高コレステロール食によるインスリン抵抗性と脂肪肝炎(肝臓の脂肪蓄積・炎症・線維化)が軽減されていることが確認されたことから、肝臓における炎症反応の主役である肝内マクロファージの性質を調査したところ、CCL3欠損マウスでは炎症性M1マクロファージが少なく、常在型M2マクロファージが多い状態であることが確認されたという。
さらに、マウス腹腔マクロファージをCCL3とともに培養したところ、M2よりM1の性質が示されることも判明。これにより、CCL3がマクロファージに直接作用し、炎症を増大させる可能性があることが示されたとするほか、NAFLD患者の血液中のCCL3濃度はNAFLDの重症度に従って増加することを見出したとする。
なお、今回の研究成果から、CCL3ケモカインの作用を阻害することが、NAFLDの有効な治療方法になる可能性が示されたことから、今後のCCL3受容体阻害薬開発につながることが期待されるとしている。