北海道大学(北大)は10月8日、福山大学、九州大学(九大)との共同研究により、「免疫賦活剤(アジュバント)」である糖脂質の成分と結合する「C型レクチン受容体」の「Mincle(Macrophage inducible C-type lectin)」や「MCL(Macrophage C-type lectin)」の立体構造をX線結晶構造解析により明らかにし、ほかの類似受容体では見られない疎水性領域が存在することを突き止め、その領域が糖脂質との結合に重要である可能性が示唆されることを発表した。
成果は、北大大学院 薬学研究院 生体分子機能学研究室 博士研究員の古川敦氏(科学技術振興機構(JST)所属)、同・前仲勝実教授(同所属)、同・岡部由紀氏、同・学生の藤司亜也 氏、同・学生の神田諒氏、同・尾瀬農之 准教授、福山大薬学部の上敷領淳 講師、九大生体防御医学研究所 幹線ネットワーク研究センター 分子免疫学分野学生の森大輝氏、同・学生の豊永憲司氏、同・三宅靖延助教、同・山崎晶教授らの共同研究チームによるもの。研究の詳細な内容は、日本時間10月8日付けで米科学雑誌「米科学アカデミー紀要(PNAS)」に掲載された。
免疫細胞に発現し、カルシウム依存的に糖に結合するタンパク質群のC型レクチン受容体は「パターン認識分子」の内の1つであり、主に病原体表面に特異的に存在する糖や糖を含む物質(糖脂質など)を認識する。パターン認識分子とは、自然免疫と獲得免疫に大別される免疫系において、元来ヒトなどの動物が病原体(ウイルス、細菌、寄生虫など)を認識するために発達させた自然免疫のシステムのことだ。病原体が持つ共通部分(=パターン)を認識して免疫を活性化する作用を持つ。
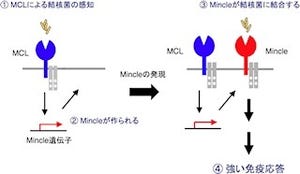
そのC型レクチン受容体の1種であるMincleやMCLは、免疫細胞の表面に発現するタンパク質だ。MincleやMCLは結核菌ワクチンとして知られているBCGに含まれ、免疫活性化効果のある結核菌由来の糖脂質「TDM(trehalose dimycolate)」(画像1)と結合した後に免疫活性を引き起こし、病原体排除に関与することが知られている。TDMは糖と脂質部分からなる分子で、これまでの研究により、糖と脂質部分両方がMincleとの認識に必要であることが示されている。TDMは別名「コードファクター」とも呼ばれ、ワクチンに免疫賦活剤として含まれる重要な分子だ。
MincleやMCLは前述したようにC型レクチン受容体に分類されるが、これまで知られているほかのC型レクチンでTDMに結合するものはなく、なぜMincleやMCLがTDMを認識するのか、その分子メカニズムは不明だった。そこで研究チームは今回、X線構造解析を行い、MincleやMCLの立体構造を明らかにすることで、その特異性やメカニズムを明らかにすることを目指したのである。
MincleとMCLのタンパク質単結晶のX線結晶構造解析が実施され、両タンパク質の立体構造が決定された後、TDMがMincleやMCLとどのように結合するのかについての結合モデルが構築された。次に、その結果に基づいてMincleの糖脂質認識に関わると考えられるアミノ酸残基に変異を導入したタンパク質を発現する細胞が作製され、TDMとの結合を「レポーターアッセイ」系による評価が実施されたのである。なおレポーターアッセイとは、ある刺激によってその刺激がタンパク質の発現や表現型のアウトプットとして観察するシステムのことをいう。
まず、MincleとMCLの単結晶が作製され、次に高エネルギー加速器研究機構や理化学研究所が所有し高輝度光科学研究センターが運営する大型放射光施設「SPring-8」でこの単結晶にX線を照射し、構造解析が行われた。その結果、MincleとMCLの立体構造はほかのC型レクチン「DC-SIGNR」に似ていることがわかったが、糖脂質認識部位に違いがあることが判明したのである。
次にMincleやMCLがどのように糖脂質と結合するかを推測するために、モデリングが行われた。モデリングはDC-SIGNRの「マンノース結合複合体」が利用された。その結果、TDMの脂質部位が存在し得る方向に、MincleやMCLで脂質と親和性が高い「疎水性アミノ酸残基」がほかのC型レクチン受容体に比べて多く存在していることがわかったのである。
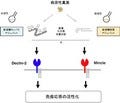
この結果を基に、疎水性残基や糖結合部分に近い重要と考えられる残基に変異を持つMincleを細胞で発現させ、レポーターアッセイ系での評価が行われた。すると、変異導入されたMincleではレポーター活性の減少が観察されたことから、研究チームの予測の正しさが確認されたというわけである。この結果から、Mincleはほかの免疫系受容体とは異なった方法で脂質認識をしていることが明らかになったというわけだ(画像2)。ほかの免疫系受容体の「CD1-β2m」や「TLR4-MD2複合体」などでは疎水性ポケット(溝)があるが、Mincleでは見られず、その代わりに表面の疎水性残基で糖脂質の脂質部分で結合していると考えられるという。
MincleやMCLはBCGに含まれるアジュバントであるTDMと結合するタンパク質だ。ただ、TDMは局所炎症性が高いため、ワクチン投与後も炎症が続くという問題がある。現在、各種ワクチンに必要な成分であるTDMに代わるアジュバント候補が実用化に向けて精力的に研究が進められ、一部は臨床段階にあるが、いずれもこれまで知られている化合物の類似体だ。
今回、アジュバントを認識する重要な受容体の立体構造が明らかになったことにより、この立体構造情報を用いた「in silico解析」(コンピュータを用いた実験)などを含む合理的設計に基づき、より強力な免疫活性化能を持つアジュバントの開発が期待されるという。さらに、Mincleは免疫制御に重要なヘルパーT細胞の1種の「Th17細胞」(不明な部分も多いが、好中球や上皮細胞の活性化をする役割があることがわかっている)の活性化に関与していることが知られており、より効果的な免疫療法開発につながる可能性があるとしている。