物質・材料研究機構(NIMS)と東京医科歯科大学(TMDU)は4月8日、「矯正歯科用骨膜下デバイス」の形状の最適化と新しいコーティング法を共同で開発し、骨との結合が従来のデバイスで3カ月かかるところを1カ月で実現する技術を確立したと共同で発表した。
成果は、NIMS 国際ナノアーキテクトニクス研究拠点 バイオセラミックスグループの菊池正紀 グループリーダー、TMDUの上園将慶 大学院生、同・生体材料工学研究所の高久田和夫 教授、同・医歯学総合研究科 顎顔面矯正学分野の森山啓司 教授らの共同研究チームによるもの。研究の詳細な内容は、現地時間4月2日付けで米医療系科学誌「Journal of Biomedical Materials Research Part B:Applied Biomaterials」オンライン版に掲載された。
咬み合わせの異常などについて治療を行う歯の矯正は、歯に力をかけてゆっくりと顎骨内を移動させるといった治療を行う。この時、現在は奥歯などを固定源にしてほかの歯を移動させるという方法が採られている。そこで利用されているのが、人工歯根などのインプラント材料や矯正歯科用骨膜下デバイスだ。
矯正歯科用骨膜下デバイスは、高い強度を必要とするために金属材料、特にチタンやチタン合金が使用されている。骨の表面を覆っている強靭な線維性被膜の「骨膜」と硬い「骨実質」との間にある骨膜下に円盤状の材料を置き、その下部や周囲に骨組織を誘導して矯正用装置を固定するのである。
チタン系の材料は「オッセオインテグレーション(生体不活性材料の周囲に骨が直接存在している状態を指す)」と呼ばれる能力があり、元来、骨と結合できる能力を持つ。その上でデバイスのチタン系材料の表面には、「水酸アパタイト(HAp)」のコーティング(HApコーティング)処理も施されている。水酸アパタイトは、骨や歯の無機成分とよく似た化学組成(Ca10(PO4)6(OH)2)ならびに結晶構造を有した「リン酸カルシウム」の1種で、骨との親和性が高く直接結合する材料だ。このようにしてデバイスは、骨と十分な強度を持って結合して治療に利用できるまでの時間が短くなるように工夫されているというわけだ。
しかし、デバイスは骨の表面という骨形成に必要な細胞の動員がより困難な場所で骨と結合する必要があるため、これまでの製品ではHApコーティング処理をしても、骨に強固に結合して治療に利用できるまでには、最短でも3カ月程度の待機時間が必要だった。
矯正歯科用骨膜下デバイスのようなオンプラントタイプは生体への侵襲が小さいという点で、ミニプレートやマイクロスクリューなどねじを利用して固定するタイプと比べて優れているが、逆に骨の表面上で骨と結合させるのに時間がかかってしまうという解消すべき点があるのである。なお、この待機期間を4週間程度まで縮めることができれば、生体への侵襲を低く留めたままで早期に治療が開始できるという。そこで研究研究チームは今回、デバイス形状の最適化と新しいコーティング法の開発に挑んだというわけだ。
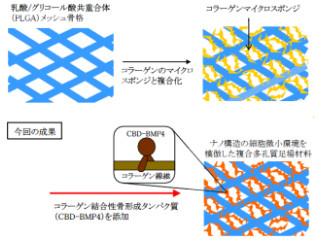
今回開発されたコーティング法は、チタンに「水酸アパタイト/コラーゲン骨類似ナノ複合体(HAp/Col)」を「ディップコーティング」するというものだ。HAp/ColはNIMSがTMDUと共同開発した、コラーゲン線維の上に水酸アパタイトのナノ結晶が向きを揃えて並んでいる骨のナノ構造を世界でも初めて再現することに成功した材料である。またディップコーティングとは、基材をコーティングする材料の懸濁液に浸漬し、乾燥させる手法のことだ。一般にはこの手順を数回繰り返すことが多い。手軽でコーティングする材料の組成や構造の変化を伴わないが、基材とコーティング層の接着強度はほかのコーティング法と比較すると弱いという短所を持つ。
そしてHAp/Colはこのナノ構造を骨内に埋入すると、自分の骨を移植した時と同様な骨リモデリングプロセスによって吸収されて骨に置き換えられていくという仕組みを持つ。すでに多孔体のものについてHOYAが実用化を進めていて、臨床試験の結果では市販の吸収性人工骨材料より高い治療効果を示している。
同コーティング法の有効性は、直径0.5mm、長さ12mmのチタンワイヤーに水酸アパタイトをコーティングした材料(従来処理)や何も処理をしていないチタン金属(未処理)を比較対照として、材料を骨膜下に埋植する動物実験によって確認が行われた。せん断強度試験にて接合強度の測定が行われた結果、画像1に示されているように接合強度が未処理で2.8Nであったものが、従来のHApコーティング法では6.0Nと2倍の改善を見せ、さらにHAp/Colでは16.4Nと従来のコーティング法と比較して2.5倍以上、未処理と比較すると5倍以上の改善が認められたというわけだ。
続いて、これまで市販されている製品との比較が検討されたが、直径7.7mmの円盤形で形状が異なるため、接合強度の単純な比較ができないことがわかった。そこでデバイスの固定性の良否を判断するため、有効な材料表面の「骨被覆率」(60%以上の被覆率が必要と考えられている)の比較が行われることになったのである。骨被覆率とは、デバイスの周囲をどのくらい骨が覆っているかを示す数値で、デバイスの面積(断面では周囲長)に対する骨が覆っている面積(断面では周囲長)の比率である。
オッセオインテグレーションを持つチタンなどの材料の場合、埋入初期(~6カ月)では薄い(100μm以下)線維性の被膜が骨と材料の間に介在していても骨で覆われていると計算することが多く、今回の未処理チタンやコーティングにおいても骨被覆率はそのように計算されている。
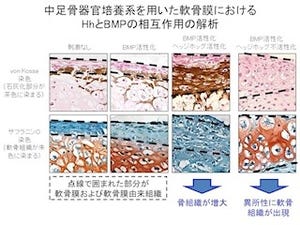
4週の時点でHAp/Colが62.2%、従来のHApコーティングで20%、従来品(オンプラント:文献値)は36.2%と、これまでは3カ月(12週)を要していたのだが、今回の新手法では1カ月(4週)で同程度の被覆率を達成することに成功したという。この数字は平均値だが、臨床的には最悪の場合でも最低限の有効性を保証できるかどうかが重要だ。4週での比較を示したのが画像2で、この時点では従来のHApコーティングや未処理では最悪の場合に骨に接触しない場合もあるのに対し、HAp/Colでは常に安定した骨との結合が実現されている。
また、一般にデバイスの固定に必要な骨との接合強度については、300N以上が必要だという。よって、まだ強度的には十分ではないように見えるが、今回は試験片が単純な棒状で小さいので、デバイスのサイズと形状を最適化することで強度を改善することができるとした。現状の強度のままでもこの強度を達成することはデザイン次第で可能だし、さらに形状を工夫して固定効果を高めるようにできることも確認されている。
HAp/Colコーティングは多くのHApコーティングと異なり、非常に早く吸収が進んでなくなっていくのが特徴だ。この吸収に伴って骨が周囲に形成されていき、チタンのオッセオインテグレーションに速やかに移行していると考えられるという。これは、チタン周囲に骨類似物質であるHAp/Colが存在しているので、細胞がこれを骨と認識して「そこに骨がなければいけない」と判断し、「骨リモデリングプロセス」で骨が早期にチタン周囲に形成されたともいえるとした。なお骨リモデリングプロセスとは、骨表面に骨を吸収する「破骨細胞」が付着して骨吸収が開始され、その吸収された跡に骨を造る「骨芽細胞」が現れて新生骨を形成する骨の正常な代謝機構によるプロセスのことだ。
研究チームによれば、骨リモデリングプロセスをこのように応用したコーティング法はこれまでにないという。実際、人工歯根ではHAp薄膜コーティング材料が実用化されているが、HApコーティングの吸収には1年程度かかるとされており、埋植初期においては一般的なHAp厚膜コーティング材料と同様のHAp表面での骨結合が起こっていると考えられているので、現象は似ているが反応機構はまったく異なるものだ。
いいことずくめのように見える同コーティングだが、唯一短所を上げるとすれば、生体材料グレードのコラーゲンが原材料として含まれているため、水酸アパタイトに比べると材料費が高くなってしまうというところである。ただし、特別に高価な機器を使用するわけではいため、総合的には従来のHApコーティング材料と同程度のコストで作製が可能になることが予想されるという。今後は、実用化を目指して企業との共同研究もスタートする予定で、初期の目的である歯科矯正用骨膜下デバイスだけでなく、人工歯根、人工関節などさまざまな分野での応用が期待されるとも研究チームは語っている。