名古屋大学(名大)は1月30日、山口大学との共同研究により、神経変性疾患の1つである「球脊髄性筋萎縮症(SBMA)」の病変部位選択性のメカニズムの一端を明らかにし、転写因子の「熱ショック因子1(HSF-1)」が病変分布決定に影響していることを見出したと発表した。
成果は、名大学大学院 医学系研究科 神経内科学の祖父江元教授、同・勝野雅央准教授、同・近藤直英研究員らの共同研究グループによるもの。研究の詳細な内容は、英国時間1月29日付けで英国科学誌「Nature Communications」のオンライン版に掲載された。
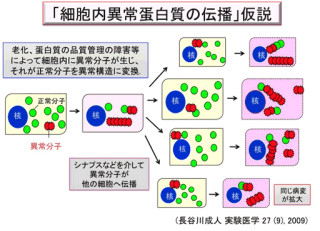
神経変性疾患(アルツハイマー病、パーキンソン病、筋萎縮性側索硬化症など)では、病気の原因となる異常タンパク質は全身の組織に広く発現しているにも関わらず、病気ごとに、ある特定の部位に偏って異常タンパク質が蓄積し、その組織で神経細胞が変性し(弱り)、認知の障害や筋萎縮、筋力低下などを来たすことが知られている。しかしなぜ、特定の場所に異常タンパク質の蓄積が偏るのかはよくわかっていなかった。
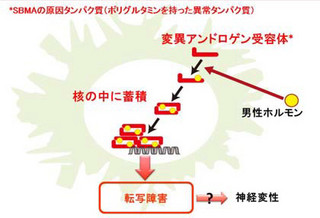
そこで研究グループは今回、神経変性疾患の病変部位の偏りのメカニズムを明らかにするために、SBMAを対象として研究を実施した。SBMAは、全身の筋力低下や食べ物の飲み込みにくさを主な症状とする進行性の病気で、「ポリグルタミン」という異常な構造を持った「アンドロゲン受容体タンパク質」が男性ホルモンと結合することによって、脊髄の運動神経細胞や膵臓、陰嚢の皮膚などに偏って蓄積することが知られている。
今回研究グループは、変性から神経を守る働きがあることが知られている「熱ショックタンパク質(HSP)」の生成を促進するいくつかの転写因子に着目し、SBMAモデルマウスの脳、脊髄およびさまざまな臓器での異常タンパク質とこれらの転写因子の分布の関係を検討した次第だ。
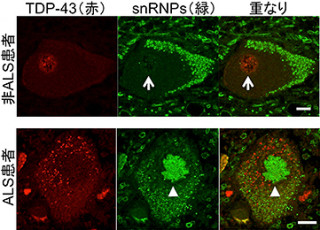
その結果、HSF-1の分布が異常タンパク質の蓄積と裏腹の関係にある、すなわちHSF-1が多く発現している部位では異常タンパク質の蓄積が少なく、HSF-1の発現が少ない部位では異常タンパク質が大量に蓄積していることが判明。この傾向は、SBMAマウスのみならずSBMA患者の病理標本でも同様だった。
次にHSF-1の発現量を減らすことで異常タンパク質の蓄積の分布が変化するかどうかを調べるために、HSF-1遺伝子を一部欠損したマウスとSBMAマウスを交配し、HSF-1を一部欠損したSBMAマウス(AR-97QHSF-1+/-)を作成して、解析が行われた。
すると、このマウスではSBMAマウスでは通常は異常タンパク質が蓄積しない大脳視覚野や肝臓、下垂体に異常アンドロゲン受容体タンパク質の蓄積が認められ、そのほかの脳や脊髄の部位でも異常タンパク質の蓄積頻度が増加したのである。
また、単に異常タンパク質の蓄積が増えただけでなく、HSF-1を一部欠損したSBMAマウスでは神経細胞の変性や肝細胞萎縮、肝機能障害などが認められ、筋力低下の進行や生存率の悪化も来たすことが確認された。
さらに、HSF-1を欠損させたことによる臓器ごとのHSPの発現への影響を検討したところ、脊髄や肝臓ではHSF-1の低下に伴いHSPの発現が抑制されることも明らかとなったのである。
次に、HSF-1を局所的に増加させることで異常タンパク質の蓄積を抑えられるか否かを調べるために、遺伝子を細胞に導入できる運び屋ウイルスの1種「レンチウイルスベクター」を用いて、ヒトHSF-1をSBMAマウスの脳局所へ投与し、異常タンパク質の蓄積や神経細胞の変化の検討が行われた。その結果、HSF-1を投与した部位の周辺では異常タンパク質の蓄積が減少し、神経細胞の変性も抑えられていることがわかったのである。
これらの検討結果から、HSF-1がSBMAの病変部位決定に影響を及ぼしていることが示唆された。また例外的に骨格筋のような臓器ではHSF-1以外の転写因子がHSPの維持に重要であることも同時に判明した形だ。
今回の研究ではSBMAでは脳、脊髄やそのほかの多くの臓器でHSF-1の発現分布および発現量が病変部位決定に影響を与えていることが示され、これまで謎に包まれていた神経変性疾患において病変分布が偏る現象(病変部位の選択性)のメカニズムの一端が明らかとなった。
SBMA以外の神経変性疾患においても病変分布の偏りがあるため、それらの病気でも同様の機序があるのかどうかを研究する必要があると、研究グループはコメント。
また臓器によりHSPを誘導する主役が異なることも判明したため、臓器ごとに主役となる因子を制御し効果的なHSPの誘導を行うことで、将来的にはHSPを利用した神経変性疾患の治療法を開発できる可能性があるという。
ただし臨床応用するためには課題もあり、さらなる研究の蓄積が必要と考えられるとしている。なお、SBMAについては現在男性ホルモンを抑える薬剤の臨床試験が進められている形だ。