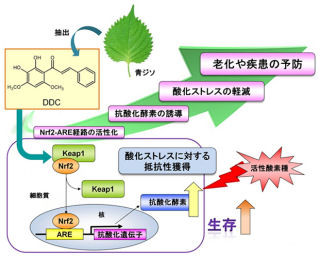
科学技術振興機構(JST)と慶應義塾大学(慶応大)は11月29日、針状に加工した導電性のダイヤモンドを電極(ダイヤモンド電極)として用いることで、がんのバイオマーカーの1つである「還元型グルタチオン(GSH)」の濃度をマウスの生体内で直接測定することに成功したと共同で発表した。
成果は、同大 理工学部の栄長泰明教授、同・医学部の佐谷秀行教授らの共同研究グループによるもの。研究はJST課題達成型基礎研究の一環として行われ、その詳細な内容は、英国時間11月29日付けで英国オンライン科学誌「Scientific Reports」に掲載された。
放射線や化学療法といった従来のがん治療の多くは、がん細胞内に活性酸素種を発生させることでがん細胞を死滅させ、治療効果をもたらすと考えられている。
GSHは、細胞傷害性のある活性酸素種を除去して細胞を保護する働きを持つ抗酸化物質だ。これまでの研究から、がん細胞は正常組織と比較して高濃度のGSHを持ち、がん治療によって発生した活性酸素種を速やかに除去してしまうため、がん治療に対して抵抗性を示すことがわかってきた。
このことから、がん組織のGSH濃度変化を測定できる方法を開発できれば、放射線や化学療法などの治療の効果判定に役立てることができると考えられている。
しかし、従来の動物実験で行われてきたGSHの測定では、生体から組織を採取した後に前処理を行うため、測定までに時間がかかるという問題があった。さらに、専用の光学測定機器を使用する必要があるため、より簡便にGSHの変化をモニターできる方法の実現が期待されている状況だ。
一方、これまでに研究グループは、ホウ素を含んだダイヤモンドを化学電極として用いた時に優れた特性を持つことを発見しており、次世代の電気化学センサとして期待できることを報告していた。なお本来、ダイヤモンドは絶縁体だが、不純物としてホウ素を添加することで導電性を付与することができ、それを応用して電極としたものがダイヤモンド電極だ。
電極材料として従来利用されている炭素電極、白金電極などに比較して、水溶液中での電位窓が広い、バックグラウンド電流が小さいなどの優れた電気化学特性を持つため、センサ、水処理を初めとした応用が期待されているほか、耐久性など、ダイヤモンド本来の物理化学特性も兼ね備えるため、次世代の新しい電極材料としても期待されている。
そこで今回の研究では、マイクロサイズに加工したダイヤモンド電極を作製し(画像1)、これを用いて生体内で直接GSH濃度を測定する方法の確立が目標とされたのである。
酸化電位の高いGSHを電気化学的に酸化しようとすると、カーボン電極、白金電極などの通常の電極材料では酸素発生が優勢となり、GSH自身の酸化は観測されなくなってしまう。しかしダイヤモンド電極は、水が電気分解しにくい特徴を持つため、酸素発生が起こりにくく、2.0V以上の高い電位においてもGSHの酸化に起因する酸化電流を観測することに成功した。
通常の電極材料では、このような高い電位では、酸素発生による電流値と重なってしまうために測定が不可能であったが、今回の研究では、2.3Vにおける電流値の濃度変化をモニターすると比例関係が得られ、GSH測定が可能であることがわかった次第だ(画像2・3)。

|

|
|
GSH濃度測定。画像2(左)は、GSH濃度を変化させた際の「サイクリックボルタモグラム」と、それぞれの濃度における電流値の検量線。画像3は、2.3Vにおける電流値をプロットしたもの。0~10mMの範囲で良好な検量線が得られている |
|
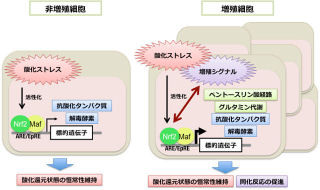
グルタチオンは、グルタミン酸、システイン、グリシンの3つのアミノ酸が結合したトリペプチドであり、生体内で抗酸化作用を担う主たる分子である。細胞内で還元型(GSH)と酸化型の2つの姿で存在し、酸化還元反応で互いに変換されるという特性を持つ。このため、潜在的なGSH量の評価のためには、「酸化型グルタチオン(GSSG)」の量も測定する必要がある。
GSSGをGSHと同様に測定したところ、GSHに比べて酸化電流の立ち上がりが、より高電位側に観測されたが、やはり2.3Vにおける電流値の濃度変化をモニターすると比例関係が得られ、酸化型グルタチオンも測定が可能であることが確認された。
さらに、GSHとGSSGの酸化電位が異なることを利用して、それらの分離検出ができることも判明。すなわち、酸化電位を1.3Vに固定すると、GSHでは酸化電流値が観測されるのに対し、GSSGでは酸化電流値が観測されない、ということが示されたのである(画像4)。
画像4は、GSHの選択的な測定。1.3Vをかけた場合のそれぞれの電流値のプロット。酸化型グルタチオン(GSSG)は電流値が観測されないが、還元型グルタチオン(GSH)では良好な検量線が得られている。この電位ではGSHを選択的に測定できていることがわかる。
生体内(in vivo)測定として、マウスの皮下に作製したがん組織について、ダイヤモンドマイクロ電極を挿入し、1.3Vをかけた「クロノアンペロメトリー」により酸化電流が測定された。
具体的には、「ヒト口扁平上皮」のがん細胞「HSC-2細胞」をマウスの皮下に移植して作製したがん組織と、マウスの正常な皮下組織のそれぞれに電極を挿入し、両者の比較を実施。マウスのがん組織における電流値は、健康なマウスに比べて、3体とも高い値を示し、がん組織が高いグルタチオン濃度を示すことがわかった(画像5)。
画像5は、生体内におけるクロノアンペロメトリー測定。1.3Vをかけた後の電流値をモニターしたもの。がん組織では、健康な組織に比べ、GSH濃度が高いことがわかる。
ヌードマウスの皮下にヒト口腔内がん細胞を100万個移植し、2週間後に増殖した腫瘍組織と、周辺の健康な組織の中のGSH濃度を腫瘍内あるいは正常組織内に針を刺入することでの測定を実施した。
さらに3体の内の2体には、これらがん組織に活性酸素種を発生する放射線を照射し、GSH濃度が測定された。その結果、放射線照射を行わなかった1体については、グルタチオン濃度は変化せず、放射線照射が行われたマウスについては、その照射量に応じてGSH濃度の減少が観測された(画像6)。
このことから、放射線照射後に発生する活性酸素種によりがん組織内のGSHが消費され減少したことが、ダイヤモンドマイクロ電極を用いたGSHの直接測定によってわかったのである。
画像6は、マウスのがんに放射線を照射した際のがん組織内GSH濃度の変化。放射線の線量依存的にがん組織のGSH濃度の減少が認められた。
試験内容は、ヌードマウスの皮下にヒト口腔内がん細胞を100万個移植。2週間後に増殖した腫瘍を持つマウスに放射線(2Gyあるいは6Gy)を照射し、3時間後に照射した腫瘍組織、照射しなかった腫瘍組織、および周辺の健康な組織の中のGSH濃度を組織内に針を刺入することで測定した。
放射線の照射線量依存性に腫瘍組織内のGSH濃度の減少が認められ、放射線照射によって組織内の酸化ストレスが上昇し、GSHが消費されたことを測定することができた。
研究グループによれば、がん治療の効果判定に有用と期待されるGSH濃度、並びにGSH-GSSG比が、がん組織中にて簡便に測定できることから、将来的には実際に患者におけるがん治療後の濃度動態がどのように変化するかを直接モニタリングし、治療効果判定や治療計画の立案に有用な診断法の1つとなることが期待されるという。
また、最近注目されている「がん幹細胞」と呼ばれるがん組織の大本になる細胞は、GSHを多く産生しているために、治療に抵抗性が高いことがわかっており、がんの再発や転移の起源となる。これらがん幹細胞の機能や存在や治療に対する効果を評価する意味でも、この測定法は極めて有用であると考えられるとした。
これまでの研究成果から、ダイヤモンドマイクロ電極は、材料としての安定性に優れ、炭素材料であることから生体適合性に優れている。さらにダイヤモンド構造により、電極表面で物質の吸着も抑えられるという特徴などもあり、次世代の生体計測に欠かせない材料となりえることが従来から期待されてきた。そして今回、このような生体における物質の直接測定に応用できる可能性を示すことができたという次第だ。
さらに、今後は、グルタチオンのみならず、医学生物学的に物質動態の測定が求められるそのほかの物質においても、ダイヤモンドマイクロ電極を用いた測定の可能性を探ることや、超高感度化を目指した電極設計を行っていくことで、さらに「簡易かつ高感度な病態診断法」の開発につながる可能性が期待されると、研究グループは述べている。