東京大学医科学研究所(東大医科研)は3月12日、赤痢菌をモデルにして、「粘膜上皮」に対する病原体の侵入認識機構と、その宿主認識・防御に対抗する赤痢菌の手段を明らかにしたと発表した。成果は、東大医科研の笹川千尋教授と真田真人研究員、兵庫県立大学の水島恒裕教授らの共同研究グループによるもので、理化学研究所が所有する大型放射光施設「SPring-8」が活用された。詳細な研究内容は、英国時間3月11日付けで英科学誌「Nature」に掲載された。
毎年約1500万人が感染症で命を失っており、その中の約200万人は腸管感染症が原因だという。腸管は無数の微生物に常に暴露されているが、微生物の侵入から生体を守るため、自然免疫を中心とする堅固な防御システムが幾重にも備えられている。
一方、赤痢菌やその仲間であるO157といった病原性大腸菌などの腸管病原細菌は、それら防御システムを巧みに回避して生体へ侵入する高度に進化した機能を持つ。赤痢菌の場合は、腸管下部(大腸・直腸)の粘膜上皮(腸管などの管腔状臓器の単層の粘膜状の上皮細胞で、腸管の管腔側で栄養を吸収する役割と共に、微生物の侵入の対するバリアー(防御機構)として重要な役割も果たしている)へ侵入することにより感染を開始し、ついで上皮細胞内で増殖しつつ周囲の上皮細胞へ拡散するが、一方で感染は自然免疫により検知され腸管に炎症が起こる。
しかしながら、病原細菌の腸粘膜への侵入に対する自然免疫応答と、それを病原細菌がどうのようにして回避するか、そのメカニズムはまったく不明であった。
今回判明したことをさらに具体的に説明すると、まず「粘膜上皮に対する病原体の侵入認識機構」については、細菌が細胞侵入する時に形成される「葉状突起(ラッフル膜、マクロピノサイトーシス)」を危険信号として認識する仕組みとして、葉状突起に局在する「ジアシルグリセロール(DAG)-TRAF6-NF-κB」に依存した炎症シグナル経路が重要であることを明らかにしたということだ。
なおジアシルグリセロールとは、グリセリンに 2つの脂肪酸がエステル結合を介して結合した分子のこと。宿主細胞膜に局在してセカンドメッセンジャーとして作用する。
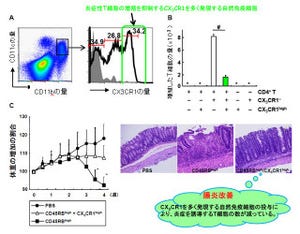
そしてもう1つの「その宿主認識・防御に対抗する赤痢菌の手段」は、赤痢菌の対抗手段として菌から分泌される「OspI」を同定し、そのタンパク質の立体構造(画像1)および生化学的性状を解明したということである。
OspIの結晶化は、赤痢菌から「III分泌装置」(多くの病原細菌が保有する特殊な病原因子(エフェクター)分泌複合体)を介して行われた。その結晶構造解析をSPring-8のビームラインの1つで、生体超分子複合体の高精度のX線回折データの測定を目的とした「BL44XU」で行い、2.0Å分解能でのOspI立体構造解析に成功した。それにより、OspIは4個の「β-ストランド」(赤)、7個の「α-ヘリックス」(青)、1個の「310ヘリックス」(青)からなる構造を持つことが判明したのである。
OspIの立体構造を、すでに報告されているさまざまなタンパク質の一次配列と立体構造との比較も行われた。その結果、OspIのアミノ酸の一次配列と類似するタンパク質は見出せなかったが、OspIの立体構造は、「シュードモナス‐シリンゲ」(赤痢菌と同様にIII分泌装置を持つ植物病原細菌)の病原因子として知られる「AvrPphB」と類似性が認められた。
AvrPphBタンパクも、OspIと同様に「システイン(Cys)」、「ヒスチジン(His)」、「アスパラギン酸(Asp)」からなる活性中心を持つプロテアーゼ酵素である。これを手掛かりに、OspIの示す酵素「UBC13」に対する脱アミド化活性に関わるCys-His-Aspの3アミノ酸残基の重要性を、各アミノ酸置換変異体を作製して明らかにしたというわけだ。
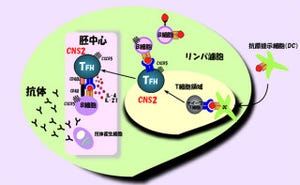
その2つの結果から、OspIは、前述の炎症シグナル経路の制御に重要なTRAF6の活性化に必要なUBC13に結合性して、UBC13の100番目のグルタミンを脱アミド化する「新規な脱アミド化酵素である」ことが発見された(画像2)。
赤痢菌が上皮細胞に侵入すると、葉状突起が菌周囲に形成されるが、菌は葉状突起を破壊して最終的には細胞質へと移行する。また細胞に目をやると、上皮細胞の側底面に葉状突起が形成されるとジアシルグリセロールが葉状突起に局在化する仕組みだ。
そのジアシルグリセロールは、プロティンキナーゼC(PKCs)によるシグナルのセカンドメッセンジャーとして働き、その結果CMB(CARD-MALT1-BCL10)複合体-TRAF6-NF-κB経路が活性化され、「抗菌性ペプチド」(ペプチドはアミノ酸が連なった分子)、「炎症性サイトカイン」(サイトカインは、)や「ケモカイン」の産生が誘導される。
炎症性サイトカインは、情報伝達に関わるさまざまな生理活性を持つタンパク質の総称であるサイトカインの1種だ。また、ケモカインも低分子のタンパク質の1種で、この2種類は病原体の侵入や自己の異物を認識してその信号を周囲の細胞や組織に知らせ(炎症を起こす)、免疫系を活性化させる役割を持つ。これらによって、炎症部位に好中球など血球系細胞が呼び寄せられる仕組みだ。
赤痢菌はこれを回避して細胞質で生存・増殖を行うために、細胞侵入時にIII型分泌装置よりOspIエフェクターを分泌する。OspIは、UBC13に特異的に結合して、UBC13の100番目のグルタミンを脱アミド化してそれをグルタミン酸へと改変する。
その結果、UBC13は失活。UBC13はTRAF6の活性化因子であり、UBC13の活性化が失われるとTRAF6の活性化が阻止され、その下流のNF-κBシグナル経路も働かなくなるという流れだ。このようにして、赤痢菌は感染の開始早々に、宿主の炎症・「自然免疫」(ヒトが生まれた時から備えている免疫系)応答を抑制する。その結果、赤痢菌の粘膜上皮内への感染が促進するというわけだ。
画像2は、英語なので少しわかりにくいが、こうした赤痢菌の上皮細胞への侵入とその中での反応などを図示したものである。
こうした腸管における微生物と宿主の攻防の中で自然免疫は、生体防御の中心的な役割を担う。病原体は、腸管へ侵入後、粘膜上皮で増殖して定着するまでの総ての過程において自然免疫により監視され、その結果、前述した炎症性サイトカインやケモカインの発現が誘導され、病原体が無防備であれば排除されてしまう仕組みだ。
従って、感染初期の自然免疫応答は生体防御に極めて重要だが、これまでは主にマクロファージを中心とする免疫応答の研究が主体であった。また、細菌の上皮細胞への感染における自然免疫応答およびこれに対抗する病原細菌の戦術に関して、多くが感染の後期における情報が蓄積されてきたが、感染初期の免疫応答に関する情報は乏しかったのである。
一方、多くの病原細菌は粘膜上皮細胞を足場として感染し下痢を初めとするさまざまな炎症性疾患を引き起こす。従って、病原細菌はさまざまな戦略によって炎症・自然免疫応答を適切に制御することが感染・定着に必須であることが知られてきた。しかし、感染開始時の腸粘膜における自然免疫応答と、それに対抗する病原細菌の戦術に関する知見は皆無だったのである。
これまでも赤痢菌を初めとする腸管病原細菌は、III型分泌装置によって、エフェクターと称する一群の病原因子を宿主細胞に分泌し、抗菌性ペプチド、炎症性サイトカイン、ケモカインの発現を抑制することが知られていた。今回、研究グループは赤痢菌のエフェクターの中に、菌が宿主侵入時に炎症応答を阻害するエフェクターを分泌していることを見出し、その立体構造と生化学的性状の解析を手掛かりとする以下の発見が導きだされた次第である。
研究内容は大別して6点に及んだ。まず、「プロテオミクス解析」(タンパク質の発現動態を網羅的に定量的に解析する、生化学的およびインフォマティクス的な解析手法)によって、赤痢菌のIII型分泌装置から分泌される新規タンパク質の探索を行った結果、菌のIII型分泌装置によって分泌されるタンパク質の中に未同定のOspIが存在することが見出されたこと。
次に、「マイクロアレイ解析」(細胞内の遺伝子発現動態を網羅的かつ定量的に測定する解析手法で、DNAアレイはその一例)を用いて、赤痢菌の上皮感染におけるOspIの役割について検討がなされた。
野生型およびospI欠損赤痢菌を感染させた上皮細胞について、遺伝子の発現量の変化をマイクロアレイ解析によって網羅的に比較したところ、ospI欠損株感染細胞において一連のケモカイン(IL-8など)と炎症性サイトカイン(TNFαなど)の顕著な発現量増加が認められたのである。すなわち、OspIは「炎症抑制作用」を持つことが示唆されたというわけだ。
さらに、NF-κBの活性化経路は宿主の初期免疫応答すなわち、炎症性サイトカイン・ケモカイン産生誘導に必須であることから、NF-κB経路の活性化におけるOspIの作用についての解析が行われた。
宿主細胞への赤痢菌侵入に伴い、侵入部位にジアシルグリセロール(DAG)の集積が認められることを見出し、DAGの集積が、その下流のDAG-CBM(CARDs-BCL10-MALT1)複合体-TRAF6-NF-κB経路の活性化の引き金となることを示した形だ。さらに、OspIはDAG-CBM複合体-TRAF6-NF-κB経路を抑制する活性を有することも示している。
そしてOspIは、細胞内でTRAF6の自己ユビキチン化を抑制することによって、TRAF6の活性化を抑制する働きがあった。さらに、OspIによるTRAF6活性化の抑制分子機構についての検討が行われた結果、OspIはTRAF6(ユビキチン転移酵素)のE2(ユビキチン結合酵素)であるUBC13を標的としていたのである。
OspIは、UBC13の100番目のグルタミン残基を脱アミド化修飾してグルタミン酸に変換する脱アミド化酵素であることも判明。事実、OspIによって脱アミド化修飾を受けたUBC13のE2活性は、顕著に低下していることが明らかになったのである。
また今回の研究と平行して、水島教授はOspIの結晶化に成功し、SPring-でOspIの結晶構造の解析を実施。その結果、OspIはシステインプロテアーゼ様の立体構造を持ち、システイン(C)、ヒスチジン(H)、アスパラギン酸(D)からなる活性中心「C-H-D triad」を持つ新規なタンパク質であることが明らかとなったというわけだ。
最後に、OspIの立体構造による知見に基づきC-H-D triadの点変異解析を行った。その結果、C-H-D triadの各点変異体は、OspIによるUBC13の脱アミド化に必須であることが示され、立体構造解析から予測された結果と完全に一致したのである。
今回の研究によって得られた病原体と宿主側の知見に関して研究グループは、炎症性腸疾患の新たな治療標法の開発に繋がることが期待されるとコメントした。また、下痢関連疾患に関わる腸管感染症の病原細菌に対するワクチンの開発や発症予防法にも貢献すると思われるとしている。