京都大学は、理化学研究所(理研)との共同研究により、培養条件を整える補助的な役割を持つ「フィーダー細胞」を使わず、ヒトのiPS細胞から培地内で浮遊させ増殖させる浮遊培養のみで「ドーパミン神経前駆細胞」に誘導することに成功したと発表。さらに、同細胞をパーキンソン病モデルのカニクイザルの脳内に移植して6カ月にわたってドーパミン神経細胞(神経伝達物質としてドーパミンを放出する神経細胞)が生き残っていること、移植細胞の増殖や機能の解析をMRI(核磁気共鳴画像法)やPET(ポジトロン断層法)、免疫組織学的手法(抗原抗体反応を利用して組織中の特定の抗原であるタンパク質や糖鎖分子などを染色する方法のこと)、行動試験などで複合的に行い、霊長類における評価系を確立したことも合わせて発表した。
研究はiPS細胞研究所の菊地哲広研究員と再生医科学研究所/iPS細胞研究所/医学研究科の高橋淳准教授らの研究グループによるもので、成果は「Journal of Parkinson’s Disease」オンライン版に2011年12月29日に掲載された。
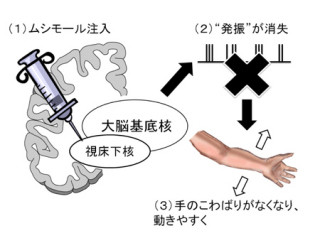
パーキンソン病は、脳の中(中脳黒質)でドーパミン神経細胞が減る(変性する)ことでドーパミン量が減り、手足が震える、体がこわばって動きにくいなどの症状が出る進行性の神経難病だ。これまでの薬物や電極を用いた治療法では、症状は改善できてもドーパミン神経細胞の減少を食い止めることはできておらず、根本的な治療法が見つかっていないのが現状である。
そこで、細胞移植によって神経細胞を補い、新たな神経回路の形成を促して機能を再生させるという、より積極的な治療法に期待が寄せられており、ヒトiPS細胞もその移植細胞の候補となっている状況だ。
これまで、マウスやヒトのiPS細胞から作製したドーパミン神経細胞は、パーキンソン病のラットモデルで症状改善効果が確認されてきた。しかし、ヒトiPS細胞から誘導した神経前駆細胞の挙動が霊長類の脳で調べられたことはなく、臨床応用を目指すためにも、霊長類のパーキンソン病モデルを用いて、ヒトiPS細胞から誘導した神経前駆細胞の効果と安全性を厳しく検証する必要があったのである。
今回の研究では、フィーダー細胞を用いることなくヒトiPS細胞を浮遊培養し、培養14日目に2種類の「サイトカイン」(さまざまな細胞から分泌され、特定の細胞の働きに作用するタンパク質のこと)を加えてさらに2週間培養し、28日目からは神経栄養因子などを加えてドーパミン神経細胞へと分化させた(画像1)。
この細胞塊を培養皿に接着させると神経突起を伸ばし、多くの細胞がドーパミンを合成する酵素「TH」で染まり、ドーパミン分泌も確認できた形だ。このことは、今回の研究で確立された方法で、ヒトiPS細胞から成熟したドーパミン神経細胞を誘導できることを示している(画像2)。
次にカニクイザルに薬剤を投与してパーキンソン病のモデルを作製し、ヒトiPS細胞から分化させた神経前駆細胞が移植された。移植細胞は培養後28日または42日、サイトカインの有無など培養条件の異なるものが準備され、MRI、PET、免疫組織学的手法で解析を行って最適な移植細胞についての検討が行われた次第だ。
まず、MRIを用いた解析の結果、移植後6カ月まで移植細胞は生き残っていることが確認された(画像3)。特に42日間培養した細胞の方が、移植片が小さいことが判明。またPETを用いた解析によって、42日間培養した細胞の方がよりドーパミン神経細胞として機能していることが示唆された(画像4)。
さらに脳切片の免疫組織学的解析で、42日間培養した細胞の方が、より多くのドーパミン神経細胞に分化していることが確認されたのである(画像5)。また、ビデオ撮影やスコア判定を利用した行動の解析も実施された。

|
|
画像5。免疫組織学的解析によるドーパミン神経細胞の数の比較。ドーパミンを合成する酵素(TH)を示す白い細胞が28日間よりも42日間培養した細胞の方が多くみられ、ドーパミン神経細胞がより多く生着していることが確かめられた |
今回の研究で確認された事実や確立された手法は、ヒトiPS細胞由来神経細胞の移植の効果と安全性を確かめる前臨床試験に役立つ成果でもある。ただし、今回はカニクイザル1頭のみで移植細胞の評価系を検討したものなので、この成果からパーキンソン病の症状の変化について議論することはできないという。そのため研究グループでは、今後は頭数を増やした前臨床試験で細胞移植によりどの程度症状が改善するのか、安全性に問題がないのか、それぞれ詳細に解析する必要があると述べている。