慶應義塾大学(慶応大)と筑波大学は、記憶が作られ失われるメカニズムの一端を明らかにしたと共同で発表した。慶應義塾大学医学部の柚﨑通介教授、筑波大学大学院人間総合科学研究科の金保安則教授らの研究グループによるもので、成果は米国東部時間1月12日に米科学誌「Neuron」オンライン速報版に掲載された。
シナプスを介して互いに結合して神経回路を形成している神経細胞は、神経活動に伴って興奮することで、主要な興奮性神経伝達物質である「グルタミン酸」を放出する。そのグルタミン酸が、ほかの神経細胞に存在するタンパク質「グルタミン酸受容体」に結合することによって、次々と神経細胞の興奮がシナプスを越えて伝達されていくという仕組みだ。
近年の研究によって、学習によりグルタミン酸受容体の数が増減することが脳における記憶の形成と消去過程の基礎過程であることがわかってきた。それにより、シナプスの伝達効率が変化すると考えられているが、グルタミン酸受容体の数が増減する分子メカニズムについてはよくわかっていなかった次第だ。
記憶・学習は、神経伝達効率という分子レベルの変化に変換されてシナプスに貯えられると考えられている。生体から取り出した脳切片や培養神経細胞においても、神経活動を一定期間活発にすることによって、神経伝達効率が長期的に増加=長期増強「LTP」あるいは低下=長期抑圧「LTD」が確認済みだ。例外はあるが、LTPとLTDはそれぞれ記憶形成と消去過程に相当すると推測されている。
また、現時点でLTDが引き起こされる理由として考えられているのが、シナプスにおける情報伝達を司る「AMPA型グルタミン酸受容体(AMPA受容体)」が、「クラスリン依存性エンドサイトーシス」によって神経細胞内に取り込まれることだ。クラスリン依存性エンドサイトーシスとは、クラスリンを骨組みとしたサッカーボールのような、かご構造を形成し、細胞表面のタンパク質などを細胞内へと取り込む仕組みである。
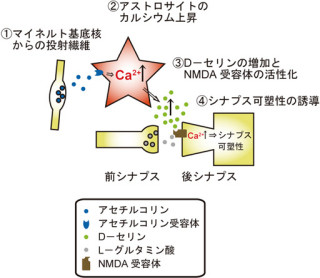
さらに、エンドサイトーシスには、「NMDA型のグルタミン酸受容体(NMDA受容体)」の活性化が必要であることも明らかにされている(画像1)。NMDA受容体は情報伝達にはほとんど関与しないが、神経活動が亢進した時にのみ活性化し細胞内にカルシウムを流入させ、シナプス可塑性を司っていると考えられているものだ。
ただし、神経活動が活発になった後に、どのようにクラスリン依存性エンドサイトーシスが引き起こされるのかについては、これまでまったく明らかにされていなかったのである。
研究グループは、記憶形成において重要な役割を果たす脳の部位の1つである海馬に着目して研究を進めた。マウスの海馬から神経細胞を取り出し、神経活動を一定期間活発にさせると、グルタミン酸受容体の数が低下し、それに伴ってシナプス伝達が長期的に低下するLTDを引き起こすことができる。このモデルを用いて、グルタミン酸受容体が存在するシナプス後部を調査した。
クラスリン依存性エンドサイトーシスはアダプタータンパク質「AP-2」にクラスリンが結合することが必須だ。AP-2は、受容体などが細胞膜から細胞内へ取り込まれる際の装置の1種で、4つのタンパク質からなる複合体タンパク質だ。そしてこのAP-2が集積するためには、一般的に細胞膜上でリン脂質「ホスファチジルイノシトール4,5-二リン酸(PIP2)」が存在する必要がある。
そこで研究グループでは、PIP2を合成する酵素である「ホスファチジルイノシトール4-リン酸5-キナーゼ(PIP5K)」が、LTD誘導時に活性化するのではないかという仮説を立て、研究を進めた。
PIP5Kには、構造が少し異なる3種類のタンパク質(これらをサブタイプと呼ぶ)がある。その内の「PIP5Kγ661(ピップファイブケイ ガンマ661)」というサブタイプが、さまざまな脳部位の神経細胞に発現し、シナプス後部では通常リン酸化されていることが判明した。
マウスの培養海馬神経細胞に、LTD誘導刺激を与えたところ、PIP5Kγ661は急速に脱リン酸化されることも確認。脱リン酸化されたPIP5Kγ661はAP-2と結合しやすくなり、AP-2と結合することによってPIP5Kγ661が持つ酵素活性が高くなったのである。
その結果から、シナプスでPIP2が合成され、逆にPIP2によってAP-2がより集積しLTDを引き起こす引き金となると推測されるに至った。実際にPIP5Kγ661の脱リン酸化やPIP5Kγ661とAP-2との結合を阻害すると、AMPA受容体がエンドサイトーシスされず、LTDも誘導されなくなることが明らかになり(画像2)、神経活動によるPIP5Kγ661の活性制御こそがLTD誘導の引き金として必須の働きを持っていることが証明された。
今回発見したPIP5Kγ661の機能は、ヒトにもあてはめられると考えられ、ヒトの記憶・学習過程の理解に有用な知見を提供しうると、研究グループでは期待している。また、記憶・学習のキーとなる酵素が明らかになったため、この酵素の活性を人為的に制御する方法が発見されれば、記憶や学習の制御に繋がっていく可能性も考えられている。さらに、将来的にはアルツハイマー病に代表されるような、記憶・学習能力が低下する疾患の治療や、逆に不要な記憶・精神的トラウマの除去といった臨床面への応用も期待されるとしている。