そこで、同マウスを用いて、筋ジストロフィー病変が発症した後でも治療可能かどうかを調べるために、ISPD遺伝子をアデノ随伴ウイルス(AAV)ベクターに搭載して、同マウスに投与する遺伝子治療として投与したところ、筋肉中のCDP-リビトールの濃度が上昇し、糖鎖の回復に加え、体重の増加、筋力の増加、筋重量の増加などが確認され、治療可能であることが示されたとする。
ただし、実際にCDP-リビトールの投与を行うためには、複数のリン酸基や水酸基を含み、細胞膜透過性が悪く、また分解を受けやすく、生体内の安定性が悪いことから、これらの弱点を克服する化合物を創出する必要があると判断。プロドラッグ化合物を複数種作成し、糖鎖回復を指標に薬効の評価などを行うことで、最終的に、糖鎖回復活性が認められ、毒性がない(低い)アセチル基を4つ結合したCDP-リビトール(TetA)が選択され、これを長期投与することで糖鎖の回復ならびに病態の重篤度を評価するいずれのパラメータでも改善が確認されたとする(プロドラッグ化)。
また、ヒト線維芽細胞でも糖鎖を効率的に回復できることも確認。ヒトでも効能を発揮することが期待されるデータを得ることができたとしており、これにより遺伝子治療法やプロドラッグ療法など、筋ジストロフィー治療薬開発に向けた臨床応用につながる成果が示されたと研究グループでは説明する。
特に、今回の研究成果は、CDP-リビトールと関連するISPDが欠損されたマウスが用いられたが、フクチンやフクチン関連タンパク質もCDP-リビトールを基質として用いるものであるため、プロドラッグの投与により筋細胞内のCDP-リビトール濃度が増加すれば変異酵素の活性が増大し、糖鎖回復ひいては治療につながると考えられるとしており、1つの薬で3つの症例の治療が期待されるようになるとする。
-

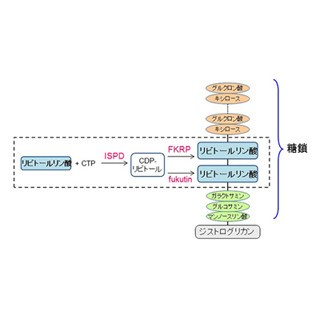
ISPD変異の場合、CDP-リビトールを作ることができない。また、FKRPやフクチンの場合、その100%が変異があるわけではないので、大量のCDP-リビトールを投与することでリビトールリン酸を補うことができるとする (資料提供:愛媛大/東大/神戸大)
なお、今回の成果に関してはすでに特許出願済みとのことだが研究グループでは、国際出願に向け、バックアップしたい企業があれば、手を挙げてもらいたいとしているほか、遺伝子治療についても興味を持っている企業があれば協力していきたいともしている(共同研究先の1つであるオランダの研究チームはプロドラッグに注目しているという)。