川崎市産業振興財団 ナノ医療イノベーションセンター(略称:iCONM)と東京科学大学(科学大)の両者は、「アデノ随伴ウイルス(AAV)ベクター」を搭載したナノマシンを用いることで、「中和抗体の産生」や「肝毒性」といった、AAVベクターを用いた遺伝子治療における課題の克服をマウスで実証したと、2月26日に共同発表した。
同成果は、科学大 総合研究院化学生命科学研究所の本田雄士助教(iCONM主任研究員兼任)、同・長尾周平大学院生(現・研究員)、iCONMの喜納宏昭副主幹研究員、科学大 総合研究院化学生命科学研究所の西山伸宏教授(iCONM主幹研究員兼任)らの共同研究チームによるもの。詳細は、米国化学会が刊行するナノサイエンス/テクノロジーに関する全般を扱う学術誌「ACS Nano」に掲載された。
遺伝子治療は、疾病の治療を目的として、遺伝子を直接または遺伝子を導入した細胞を人体内に投与する治療法である。そのための遺伝子導入方法として研究が進むのが、ウイルスの毒性を取り除いた上でその細胞に感染する機構のみを利用するウイルスベクターだ。AAVはその代表であり、さまざまな細胞種に遺伝子を導入できる。長期的に遺伝子発現が継続することから、脊髄性筋萎縮症、デュシェンヌ型筋ジストロフィー、血友病などの難治性疾患に対してすでに臨床応用されている。
しかし課題も存在しており、その1つが、成人の大半がAAV中和抗体を免疫として自然に獲得しているという点だ。そのため、一度AAVを投与すると、中和抗体が産生されてしまうことから、投与可能な患者および複数回の投与が制限されてしまっている。また、高容量のAAV投与は肝臓・腎臓への毒性が示されており、臨床試験においては死亡例も確認されている。
このような治療の課題に対して、ウイルスベクターのカプシドを高分子化合物「ポリエチレングリコール」(PEG)で修飾するアプローチや、脂質二重膜による小胞体構造の「リポソーム」などの送達担体にAAVを内包する試みもあるが、ウイルスベクターの細胞内取り込みを阻害してしまい、その結果、遺伝子導入効率の低下を招いてしまっていた。
つまり、AAV送達システムには、主に以下の3点が求められる。
- 血液中の中和抗体からAAVを回避させる
- 肝臓への集積を抑える
- 標的細胞への遺伝子導入を制御できる
そこで研究チームは今回、その開発に挑むことにした。
ワインや茶に多く含まれるポリフェノールの1種であるタンニン酸は、疎水性相互作用や水素結合を介して、タンパク質やウイルスベクターなどの生体分子と相互作用し、複合体を形成する。天然由来成分であり、生分解性や生体適合性に優れている点から、医薬品の素材としても注目されている。
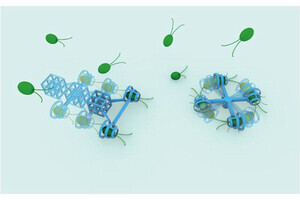
まず(1)について、これまで本田助教らは、タンニン酸とエステル形成するフェニルボロン酸導入精密合成高分子を組み合わせた生体分子送達ナノマシンの研究をしており、今回はそこにAAVを搭載したナノマシンが開発された。
本田助教らが開発したナノマシンは、水中で搭載したい分子とタンニン酸、精密合成高分子を混合するだけで簡単に形成する点が大きな特徴だ。そして、細胞内の酸性pHで搭載分子を放出する仕組みを有しており、十分な活性を示すことができることがわかっている。今回は、このナノマシンにAAVを搭載させ、AAVの活性を損なうことなく、治療における課題(中和抗体、肝毒性)を解決することをめざした。
全身投与されたAAVセロタイプ9型(AAV9)は、AAV中和抗体存在下のマウスにおいて、脳および肝臓などでの遺伝子導入効率が5〜15%に低下する。それに対し、AAV9をナノマシンに搭載して全身投与した結果、脳および肝臓での遺伝子導入効率は約50〜60%であることが確認された(3)。AAV9単独投与よりも、活性低下を顕著に抑えることに成功したのである。
また(2)については、このナノマシンは肝臓への影響を10%以下に抑え、高用量投与したAAV9の肝毒性の抑制にも成功した。このように、遺伝子治療用ウイルスベクターの課題を克服した上に、このナノマシンの脳における遺伝子導入はAAV9単体と同等であり、AAVの活性を下げる従来の送達担体の課題も解決することができており、十分な遺伝子治療効果が期待できることが明らかにされた。
さらに、マイクロバブル-集束超音波照射を組み合わせることで、脳への遺伝子導入選択性を6倍にまで増やすことにも成功((3))。医用デバイスを組み合わせることで、さらなる高機能化を達成できることも明らかにされた。
今回の研究成果は、中和抗体によって適応患者が制限されているウイルスベクター治療に対する新たな治療アプローチとして応用が期待されるとしている。