東京大学(東大)は8月23日、周囲の溶液の濃度勾配によって動く液滴の作製と、液滴に自発的に取り込まれるDNAの構造変化を介した液滴の速度制御を実現したことを発表した。
同成果は、東大大学院 総合文化研究科の柳澤実穂准教授(東大 生物普遍性連携研究機構/東大大学院 理学系研究科兼任)、同・古木智大学部生(研究当時)、同・作田浩輝特任助教(東大 生物普遍性連携研究機構兼任)、同・柳沢直也特任助教(同・総合文化研究科付属 先進科学研究機構兼任)、同・嶋本大祐大学院生、東大大学院 理学系研究科 物理学専攻の田渕辰悟大学院生(研究当時)、同・加茂あかり大学院生らの研究チームによるもの。詳細は、米国化学会が刊行する材料と界面プロセスを扱う学術誌「ACS Applied Materials & Interfaces」に掲載された。
固体、液体、気体などの相が他の相と接する際、境界で接するその二相の表面積が可能な限り小さくなろうとまとまる性質のことを「界面張力」といい、よく知られた水の表面張力もその一種である。液体の蒸発や表面を覆う分子の不均一さにより、界面張力が空間的に不均一になると、界面張力が小さな方から大きな方へ液体が流れる「マランゴニ対流」が生じることが知られている。同対流は界面張力差由来の対流であり、それが液滴周りに生じると、液滴は自発的に運動する。
医薬品材料としても用いられる「ポリエチレングリコール」(PEG)と「デキストラン」(DEX)をある濃度以上で混合させた水溶液は、「液-液相分離」(均一な溶液が、濃度や温度の変化により複数の液相に分離する現象)により、PEG溶液中にDEX液滴が形成されるが、ごく最近、PEG濃度が不均一である時、液滴が低濃度側へ並進運動する現象が報告されていた。しかし、液滴が運動する原理解明や運動制御は実現されていなかったという。そこで研究チームは今回、液滴内外の対流と濃度勾配を定量評価したとする。
今回の研究では、細長いチャンバーを用いることでPEG濃度勾配を長時間保持すると共に、蛍光ラベルしたPEG・DEXを添加することで、液滴内外の対流と濃度勾配の定量評価が行われた。すると、液滴運動の起源がマランゴニ対流であることが示されたという。
-

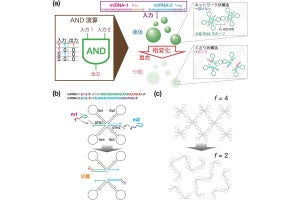
(a)細長いチャンバーを用いてPEGの濃度勾配を設けると、DEX液滴は低濃度側へ移動。(b・c)液滴の運動方向にはPEGの濃度差が生じており、それに起因した液滴表面での界面張力差によりマランゴニ対流が生じる(矢印は対流が示されている)。液滴外の流体は、PEG濃度が低い方から高い方へ流れる一方、液滴はその反作用で低濃度側へ運動(出所:東大Webサイト)
また、レオメーターを用いた液体の「動粘度」(液体のねばりの度合を示す粘度を密度で割った値)の測定から、液滴の運動速度が、濃度勾配に起因する対流による駆動力と、粘性抵抗のバランスで決定されることが明らかにされた。
さらに、ランダムに広がったCoil状態DNAを取り込んだ液滴の運動速度が、DNAなしの場合と比べて約半分に遅くなることも見出された。この速度低下は、塩化マグネシウム(MgCl2)の添加によるDNAの構造転移(Coil-Globule転移)により制御でき、DNAをCoil状態から凝縮したGlobule状態へ変化させることで、DNAなしの場合と同様の運動速度へ戻ることも確認された。
今回の研究により、液滴を駆動させる液滴表面に働く界面張力は、DNAの取り込みや構造転移により変化しない一方、粘性抵抗を生むDEX相の動粘度は、Coil状態のDNA共存時のみ顕著に大きな値を持つことが判明した。Coil状態のDNAはDEX液滴内に広がって対流する一方、Globule状態のDNAは液滴後方に凝集して対流しないことから、Coil状態のDNAを含むDEX液滴の大きな動粘度が、液滴の運動速度低下の原因であると結論付けられた。
-

DNAおよびMgCl2を添加した際の、(a)液滴の規格化速度(半径で規格化した運動速度)、(b)液滴表面に働く界面張力値、(c)液滴を構成するDEX溶液の動粘度の変化。(d)Coil状態とGlobule状態のDNAを内包した動くDEX液滴の顕微鏡画像、紫色蛍光がDNAを示している(出所:東大Webサイト)
DNAの構造は、多価イオンなどの添加によって可逆的に変化させることが可能だ。そのため、今回作成された動く液滴は、外部からの刺激による速度変化が可能であり、これを生体内で薬物輸送する微小ロボットとして活用することが期待されるという。また研究チームは今回の発見について、近年注目される細胞内での液-液相分離により形成される液滴が、細胞質対流や不均一な濃度場下で示す振る舞いの理解へも貢献するとしている。