北海道大学(北大)は2月20日、手のひらサイズのマイクロ流体デバイスを用いて、mRNAワクチンに用いられている薬物送達システム(DDS)用のカプセル「脂質ナノ粒子」(LNP)を大量製造する手法を開発したことを発表した。
-

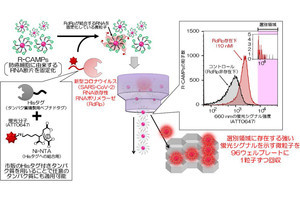
(上)マイクロ流体デバイスを基盤とした核酸搭載脂質ナノ粒子大量生産システム。(下)モデルナ社製COVID-19ワクチン「Spikevax」およびファイザー社製同ワクチン「Comirnaty」のLNPのルシフェラーゼ発現活性(出所:北大プレスリリースPDF)
同成果は、北大大学院 工学研究院の真栄城正寿准教授、同・渡慶次学教授、同・大学院 総合化学院の岡田悠斗大学院生(研究当時)、信越化学工業の安藤雅郎氏、同・山崎裕之氏、同・竹内正樹氏らの共同研究チームによるもの。詳細は、材料科学および材料工学に関する学際的な分野全般を扱う学術誌「Applied Materials Today」に掲載された。
LNPは、核酸や薬剤などを内部に搭載できるカプセルであることから、薬物送達システム(DDS)として利用するための研究が世界中で進められており、新型コロナ(COVID-19)ワクチンでも利用されている。その利用が広がる中、LNPの大きさ(粒径)は生体内動態に影響すると報告されていることから、粒径を精密に制御する技術の開発が求められている。そして現在注目されているのが、マイクロ流体デバイスを用いたLNP作製法だという。
しかし、一般的にマイクロ流体デバイスは流路幅が数百μmと微小であるため、一度に大量の原料を導入できず、大量生産に向けては課題を抱えていた。そこで研究チームは今回、同チームが独自に開発し、現在は北大発ベンチャーのライラックファーマから市販されている、LNPの粒径を10nm単位で制御可能なマイクロ流体デバイス「iLiNP」の改良を目指したとする。
市販のiLiNPはシリコーンゴム製であるのに対して、今回は耐圧・耐薬品性に優れた合成石英ガラスを基板とし、それを5枚積層化したiLiNPが開発された。その後、同デバイスのmRNAワクチン作製への応用可能性を検証するため、ファイザー社およびモデルナ社のCOVID-19ワクチンと同じ脂質組成(モデル脂質として「POPC」を使用)で、内部にmRNAを搭載したLNPの作製性能評価が行われた。
その結果、ガラス製iLiNPデバイスは、LNPの粒径を20~120nmまでの範囲で原料溶液の流量依存的に制御できることが確認された。つまり、基板をガラスに変更しても従来のiLiNPの性能が保たれており、そして高い剛性および耐薬品性を持つことが証明された。