大阪大学(阪大)は1月18日、細胞が自分自身を分解する機能である「オートファジー」によって、骨を作る細胞である「骨芽細胞」が活性化するメカニズムを明らかにしたと発表した。
同成果は、阪大大学院 医学系研究科の吉田豪太大学院生(研究当時)、阪大大学院 医学系研究科/生命機能研究科の吉森保教授(遺伝学/細胞内膜動態研究室)らの研究チームによるもの。詳細は、「Autophagy」に掲載された。
骨芽細胞は、基質タンパク質を生成・分泌することで、骨の石灰化に働き、骨の形成に関わることが知られている。一方、骨の吸収を担当している破骨細胞の存在も知られている。こうした細胞による骨の再生と破壊のバランスは加齢とともに崩れやすくなり、破壊ばかりが進むと、骨量が減り「骨粗鬆症」の状態となる。骨粗鬆症は日本に約1000万人ほどいるといわれているが、症状が進行しても痛みなどがないため、骨折を検査して初めて気がつくということも少なくない。
また、骨芽細胞の機能を活性化させているのが、オートファジーであることはこれまでの研究から分かっていたが、具体的にどのようなメカニズムで活性化させているのかについては良く分かっていなかったという。
すでに骨折の危険性が高い骨粗鬆症に対して広く使用されている骨形成促進薬として骨芽細胞をターゲットとした「副甲状腺ホルモン製剤」が知られているが、副甲状腺ホルモン製剤は使用期間が限定されているという課題が存在していた。
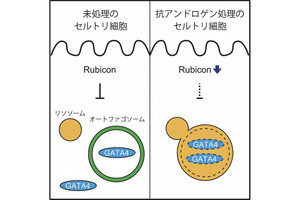
吉森教授らの研究チームがこれまでの研究で発見したのが、加齢に伴って増加するオートファジー抑制タンパク質「Rubicon(ルビコン)」で、いくつかのモデル生物で同タンパク質を抑制するとオートファジーが活性化し、老化現象の抑制と寿命の延伸が確認されている。
今回の研究では、ルビコンを欠損させたオートファジー亢進マウスの中でも骨芽細胞に特異的なルビコン欠損マウスを作成して調査を実施。この骨芽細胞特異的オートファジー亢進マウスの海面骨は増骨性の変化を示したほか、骨粗鬆症モデルの骨粗鬆症が改善したことが確認されたという。
これまでの研究から、神経や血管などの分化過程で働く遺伝子調節経路「NOTCH経路」が、骨芽細胞分化に抑制性に機能していることが報告されておいたが、今回の研究では、NOTCHシグナル下流のNICDの分解が促進していることが確認されたことから、NICDが減少することでその下流に位置する増骨性の転写因子(Runx2、Osterix)が増加し、骨芽細胞の分化が亢進しているということが判明したとする。
なお、研究チームでは、今回の成果を活用していくことで、新たな骨芽細胞をターゲットとした創薬につながることが期待されるとしている。