大阪大学(阪大)と日本医療研究開発機構(AMED)は8月6日、これまで十分に理解されていなかった「セルトリ細胞」による精子形成や維持に関わるメカニズムについて、同細胞のタンパク質「Rubicon」がオートファジーを制御し、精子形成を維持していることと、その背景にあるメカニズムを明らかにしたと発表した。
同成果は、阪大大学院 医学系研究科 遺伝学の山室禎研究生(研究当時、現・ハーバード大学博士研究員)、同・中村修平准教授(阪大大学院 生命機能研究科 細胞内膜動態研究室/高等共創研究院兼務)、同・吉森保教授(阪大大学院 生命機能研究科 細胞内膜動態研究室兼務)、阪大 微生物病研究所の伊川正人教授らの研究チームによるもの。詳細は、生物学、遺伝学などを扱う学術誌「PLOS Genetics」にオンライン掲載された。
男性の生殖細胞である精子は、大元となる「精原幹細胞」が自らを無数に複製し、その一部が「精母細胞」→「精子細胞」→精子の順に分化することで、複数の段階を経て形成されることが分かっている。
この精子形成を物理的に支え、さまざまなサイトカインによって内分泌的に支えているのが、精巣内に存在する大型の体細胞(生殖細胞以外の細胞)である「セルトリ細胞」で、精原幹細胞から始まる精子形成の維持・分化に重要な働きをしていると考えられている。
またセルトリ細胞は精巣血液関門を形作り、血液中の有害物質から生殖細胞を守ってもいることも分かっており、その機能を発揮するためには、転写因子「GATA4」が必須であることもこれまでの研究から分かっていたが、具体的にGATA4がセルトリ細胞でどのように制御されているのはわかっていなかったという。
研究チームは長年にわたって細胞内の不要物を分解・除去する仕組みである「オートファジー」の研究を進めてきた。オートファジーが誘導されると、「隔離膜」という扁平な膜構造が出現し、細胞にとって不要な構造物を包み込みながら「オートファゴソーム」を形成。これが消化酵素を含む「リソソーム」と融合することで中身を分解・除去する仕組みとなっている。
研究チームの吉森教授らが2009年に発見したのが、オートファジーの抑制因子のタンパク質である「Rubicon(Run domain Beclin-1 interacting and cysteine-rich containing protein)」で、PI3Kという酵素複合体に結合し、オートファゴソームとリソソームの融合を負に制御していることを報告。2019年には、Rubiconを欠損させてオートファジーを高めると、腎臓や神経系の加齢性疾患が改善すること、ならびに脂肪組織においては、Rubiconを欠損させると糖尿病や脂肪肝が引き起こされることなどを発見しているが、まだRubiconについては不明な点も多く、今回の研究対象である精巣や生殖腺の老化における役割や機序は未解明であったという。
そこで研究チームは今回、全身でRubiconを欠損させ、オートファジー活性を増加させたマウスの精巣を調査。その結果、このマウスでは精巣重量が減少し、精子形成が低下していることが判明したほか、精子運動能や妊孕性が低下していることも見出されたとする。
ただし、正常なマウスでは、Rubiconは精巣内のいずれの細胞にも存在していたため、どの細胞のRubiconが精子形成に重要なのかがわからなかったことから、精巣の遺伝子発現の解析を実施。全身でRubiconを欠損したマウスでは、セルトリ細胞に関わる遺伝子の発現のみ低下していることが明らかとなった。
-

マウス精巣のヘマトキシリン・エオジン染色(HE染色)像。*は精子の枯渇した箇所が示されている。野生型と比較し、全身でRubicon遺伝子を欠損させてオートファジー活性が増加させられたマウスでは、精子形成が低下しているといえるとした (出所:阪大Webサイト)
,A@男性不妊|
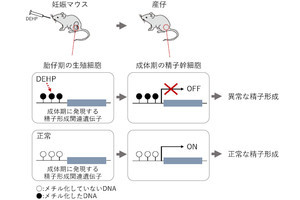
そこでセルトリ細胞のRubiconのみを欠損させたマウスを調査したところ、精子形成が低下し、精原幹細胞の数も減少していることが確認されたほか、Rubiconを欠損させたマウスでは、セルトリ細胞に必須の転写因子であるGATA4が、オートファジーによって分解されていることが判明。また、男性ホルモン「アンドロゲン」の働きを阻害する薬剤が投与されると、精巣内のRubiconやGATA4が減少することが確かめられたとする。
-

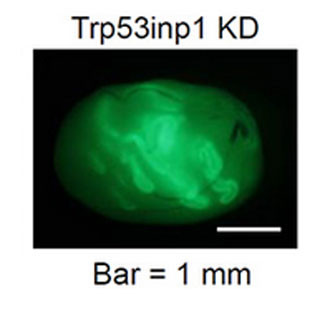
マウス精巣のPLZF染色像。PLZFは精原幹細胞のマーカーだ。矢印は精原幹細胞が示されている。コントロールと比較し、セルトリ細胞のRubicon遺伝子を欠損させたマウス(RubiconAmh-/-マウス)では、精原幹細胞が減少しているといえるとしている (出所:阪大Webサイト)
これらの結果から、アンドロゲンが精巣内のRubiconを一定に維持し、セルトリ細胞におけるGATA4のオートファジー分解を制御している可能性が示唆されたという。子育て中の雄ではアンドロゲンが低下することが知られており、オートファジーがGATA4を分解することであえて妊孕性を低下させ、子育てに集中させる仕組みが備わっている可能性があるという。
-

セルトリ細胞におけるGATA4の制御機構。(左)未処理のセルトリ細胞では、RubiconがGATA4のオートファジー分解を負に制御していることが、今回の研究によって明らかとなった。(右)抗アンドロゲン薬を処理したセルトリ細胞ではRubiconが減少し、リソソームとオートファゴソームが融合、GATA4のオートファジー分解が進行してしまう (出所:阪大Webサイト)
日本では、不妊の原因の約半数は男性にあるとされているが、そのおよそ半分は原因不明だとされており、研究チームでは、今回の成果がその原因不明とされている一部に関わっている可能性があるとして、今後の男性不妊の診断・治療に役立てられることが期待されるとしている。